一种感温型凝胶暂堵剂颗粒的制备与性能研究
赵文锦,张定军,吴彦飞,鲜彦博,陈振斌
(1.兰州理工大学 材料科学与工程学院,甘肃 兰州 730050;2.兰州理工大学 省部共建有色金属先进加工与再利用国家重点实验室,甘肃 兰州 730050)
随着油藏地层开采中的注水工艺进行到后期,地层中的含水量迅速升高,地层岩芯中出现大缝隙或形成高渗透通道,使得油井深处内部矛盾加剧,进而影响采油率[1-5],丙烯酰胺类暂堵剂是众多水溶性暂堵剂中使用率最高的一类堵剂[6-8]。虽然这类暂堵剂有良好的粘性和溶解性能,但其耐矿化度及耐温性能较差,在矿化度或温度较高的情况下使用时其粘度和抗剪切性能都会明显下降[9-10]。
我们以丙烯酰胺(AM)和丙烯酸(AA)为共聚单体,海藻酸钠(SA)为辅助单体材料,将微流体技术和物理包覆方法相结合,制备出一种感温型暂堵剂凝胶颗粒P(AA-AM)@SA,研究了其在模拟地层不同环境(时间、温度、矿化度)下的暂堵性能,并以吸水率为指标研究了暂堵剂凝胶的暂堵性能。
1 实验部分
1.1 试剂与仪器
丙烯酸(AA)、丙烯酰胺(AM)、氢氧化钠、过硫酸钾、硝酸铝、液体石蜡、氯化钠、氯化钙、海藻酸钠(SA)、无水乙醇均为分析纯;去离子水,自制。
HH-1型电热恒温水浴锅;KH-45A真空干燥箱;FT-Raman傅里叶变换红外光谱仪;Q600 V8.0热重分析仪;CP225D型电子天平。
1.2 P(AA-AM)@SA凝胶颗粒的制备
P(AA-AM)暂堵剂凝胶颗粒球的制备流程见图1。采用我们实验室改进的微流体技术制备P(AA-AM)凝胶颗粒球。
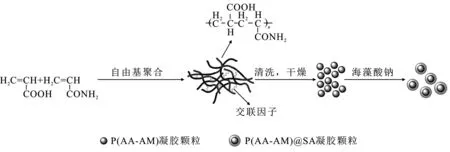
图1 P(AA-AM)@SA凝胶颗粒制备流程图Fig.1 Flow chart of preparation of P(AA-AM)@SA gel particles
称取0.9 g丙烯酸(AA)于50 mL的烧杯中,加入2 g蒸馏水,搅拌均匀后,加入一定量的氢氧化钠,得到中和度为60%的AA水溶液。加入0.891 g的丙烯酰胺(AM)固体、一定量的交联剂硝酸铝和引发剂过硫酸钾,超声,使溶液体系反应完全。用移液枪将溶液逐滴滴入装有液体石蜡的5 mL的离心管中,置于90 ℃水浴锅中保温10 min,制得暂堵剂凝胶P(AA-AM)小球,用无水乙醇洗涤数次,干燥,装袋备用。
配制不同质量浓度(0.5%,1.0%,1.5%,2%,3%)的SA溶液,将P(AA-AM)暂堵剂凝胶置于SA溶液中,静置几分钟后,PAM基暂堵剂凝胶表面包覆一层海藻酸钠膜,将其放入质量浓度为5%的CaCl2溶液中,固化5 min后,取出,真空干燥24 h,即得 P(AA-AM)@SA凝胶球,分别记为SA-1,SA-2,SA-3,SA-4,SA-5。
1.3 测试与表征
1.3.1 红外表征 通过溴化钾压片法对制备的P(AA-AM)以及P(AA-AM)@SA暂堵剂凝胶颗粒进行红外吸收光谱测试。
1.3.2 吸水倍率的测试 以包覆不同浓度海藻酸钠的水凝胶为测试单位,用游标卡尺测其初始直径,记为D0。然后将其放入不同温度的(20,30,40,50,60 ℃)蒸馏水中测其吸水率。即在不同温度下,每隔一段时间取出凝胶颗粒,测其直径,记为D,直至其达到溶胀平衡。计算凝胶颗粒的吸水率。
1.3.3 热重 (TGA) 测试 分别准确称取 5~10 mg 干燥的P(AA-AM)凝胶微球和P(AA-AM)@SA凝胶微球,于流速50 mL/min的氮气保护氛围下,采用热重分析仪对其进行热稳定分析测试,其中升温范围为 25~800 ℃,升温速率为10 ℃/min。
2 结果与讨论
2.1 暂堵剂凝胶微球的FTIR及形貌表征
图2为凝胶微球的红外谱图与形貌图。
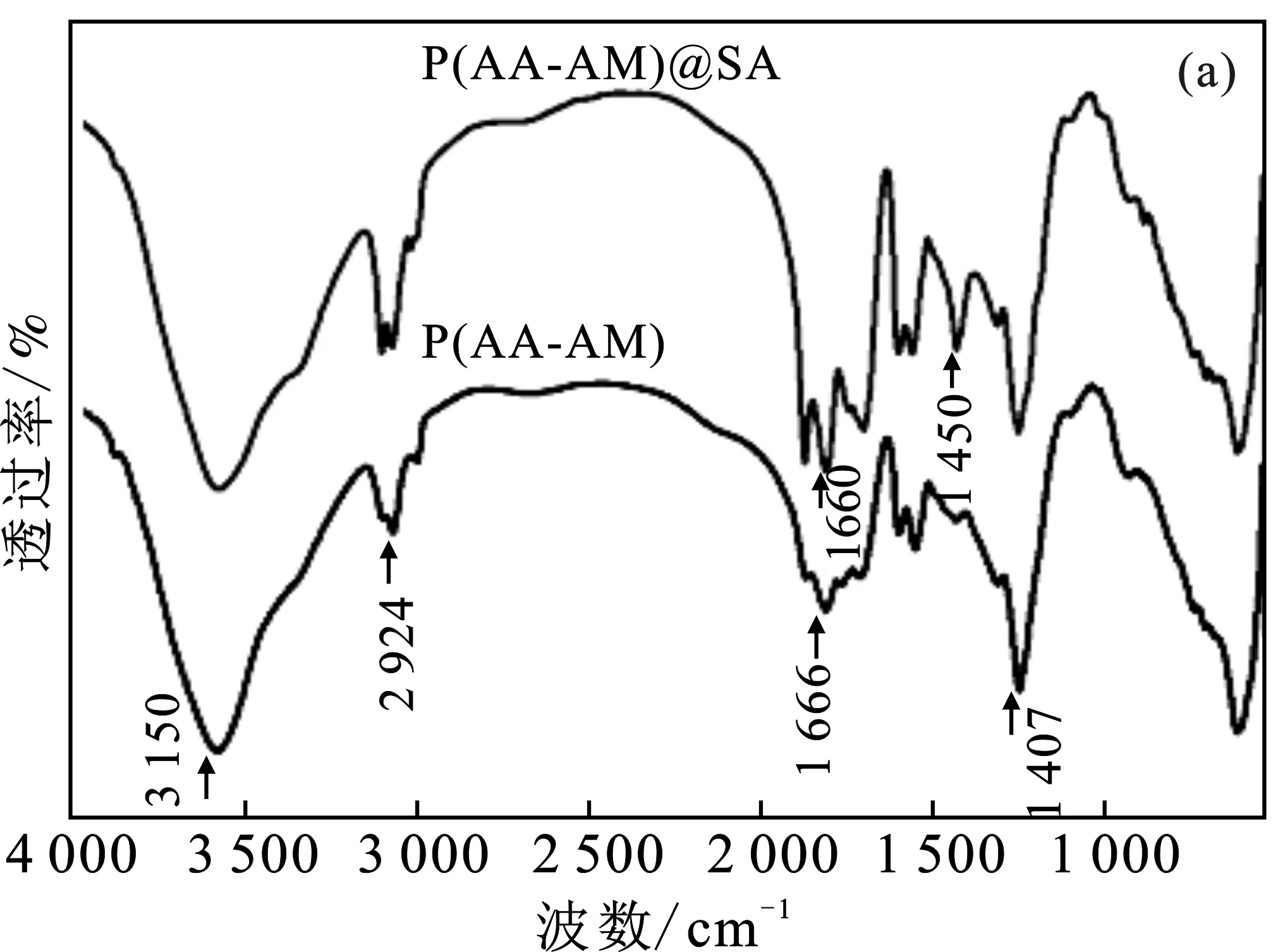
图2 凝胶微球的红外谱图与形貌图Fig.2 Infrared spectrum and morphology of gel microspheres

2.2 制备条件对暂堵剂颗粒吸水性能的影响
2.2.1 不同温度下SA用量对吸水性能的影响 图3为模拟油藏地层环境不同温度下SA用量与凝胶颗粒吸水倍率的关系曲线图。
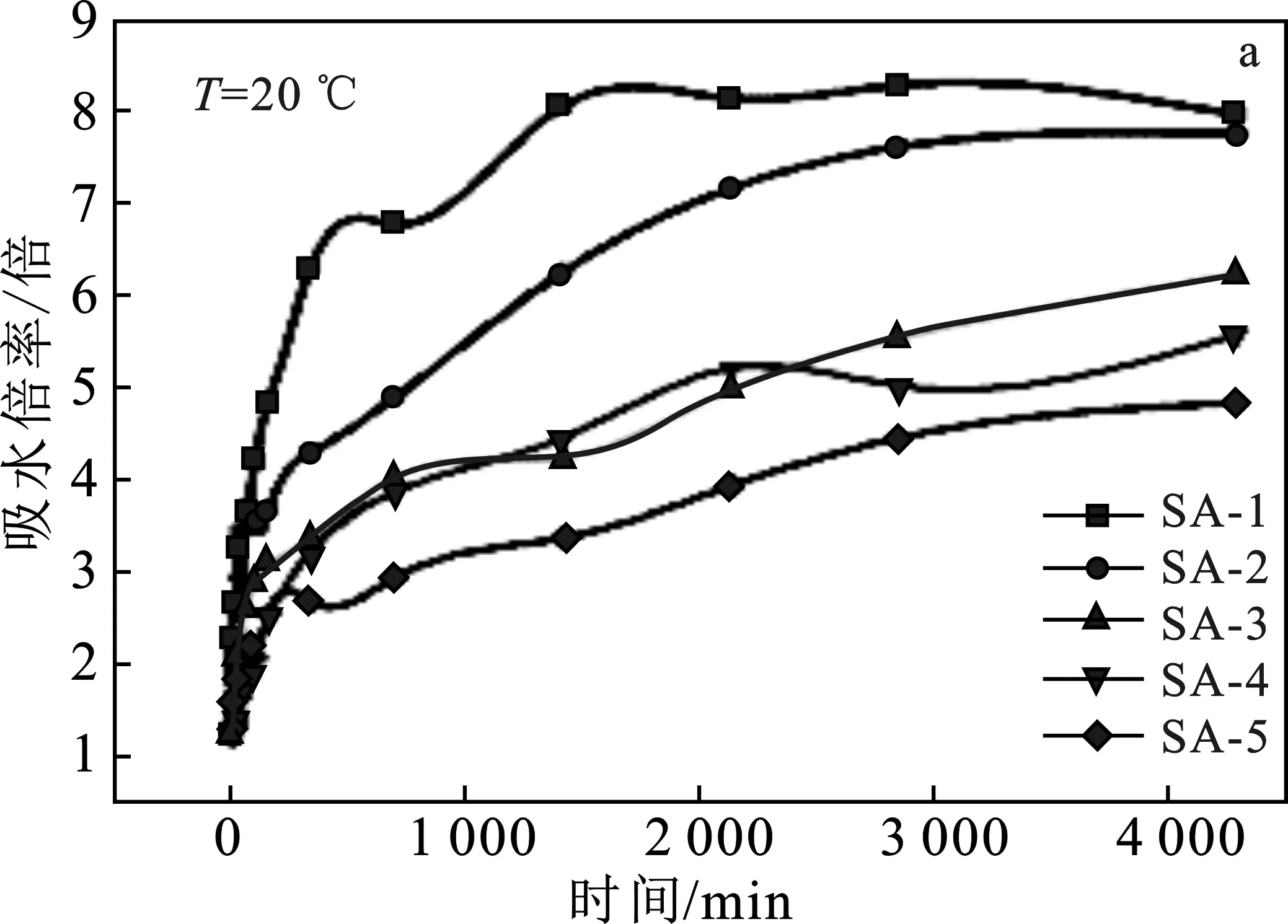
图3 不同温度下SA用量与水凝胶颗粒吸水倍率的关系曲线图Fig.3 Thc relationship between SA dosage and water absorption rate of hydrogel particles at different temperatures
由图3可知,在不同的温度下,凝胶颗粒在前500 min内均快速吸水,然后随着时间的延长,吸水速率减缓,直至最大吸水率后趋于平缓。其中当海藻酸盐的浓度为2%时,P(AA-AM)@SA凝胶颗粒在低温时吸水速率较慢,当温度升高至50 ℃和60 ℃ 时,其吸水速率明显加快。分析其原因,因为海藻酸钠与钙离子发生螯合作用交联形成网状大分子。当海藻酸钠浓度较低时,即溶液中海藻酸钠分子数目较少,分子间距离相对较大,交联网络少,形成的海藻酸钙薄膜不致密,容易发生破碎,所以SA-1,SA-2,SA-3形成的薄膜在常温时经过一段时间后即可发生破解,从而其感温性不够明显。当海藻酸钠浓度够大时,海藻酸钠与钙离子之间形成的交联点增多,交联密度变大,形成的交联网络更加致密,从而膜厚增加,薄膜不易破解,导致其在不同温度下的吸水速率都较缓慢。
2.2.2 温度对吸水性能的影响 图4为模拟油藏地层环境中凝胶颗粒吸水倍率随温度变化的曲线图。图4(a)、(b)分别对应不同温度下P(AA-AM)凝胶颗粒与P(AA-AM)@SA凝胶颗粒的吸水倍率随时间的变化曲线图,图4(c)、(d)分别对应P(AA-AM)凝胶颗粒与P(AA-AM)@SA凝胶颗粒在0~340 min内的吸水倍率随时间的变化曲线图。
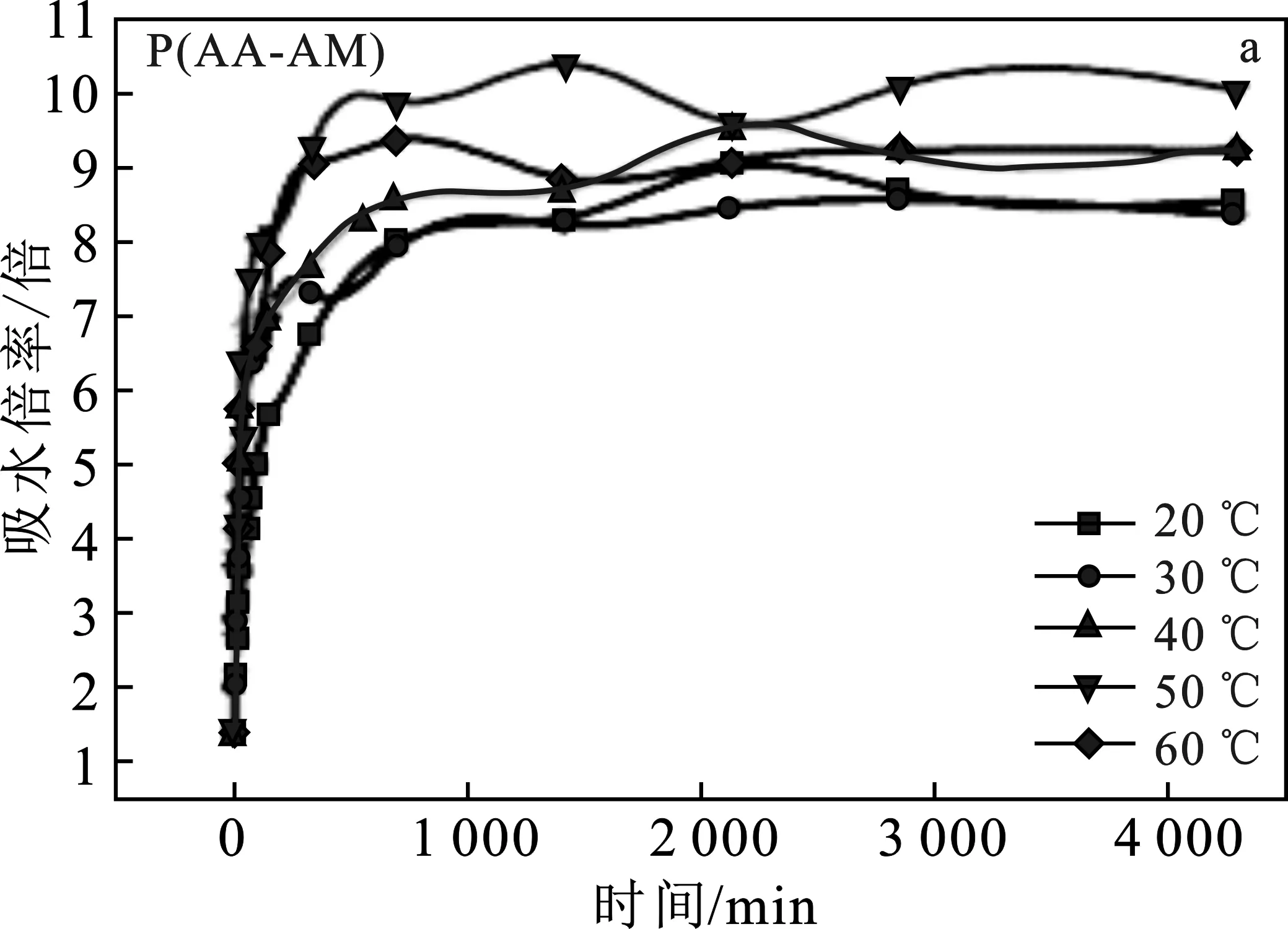
图4 温度与凝胶微球吸水性能的关系曲线图Fig.4 The relationship between temperature and water absorption of gel microspheres
由图4(a)、(b)可知,在不同温度下,P(AA-AM)@SA和P(AA-AM)凝胶颗粒在前500 min内均快速吸水,然后随着时间的延长,吸水速率减缓,直至最大吸水率后趋于平缓。且可以看出,P(AA-AM)@SA凝胶颗粒较P(AA-AM)凝胶颗粒有较好的感温性能,即P(AA-AM)@SA在低温时吸水速率较慢,高温时有较快的吸水速率。这主要是因为P(AA-AM)@SA凝胶颗粒表面包覆有海藻酸钠与钙离子螯合作用形成的海藻酸钙薄膜,温度较低时,海藻酸钙薄膜抑制了P(AA-AM)凝胶颗粒的吸水速率,温度较高时,海藻酸钙薄膜处于高温环境中,海藻酸钙薄膜里的海藻酸钠分子与Ca2+之间的化学键由于温度升高遭到破坏,所以,高温环境下,海藻酸钙膜被破坏,导致其有较快的吸水速率。
由图4(e)可知,P(AA-AM)和P(AA-AM)@SA凝胶颗粒的吸水倍率随温度的升高而增大。但是相较于P(AA-AM),P(AA-AM)@SA在低温时的吸水倍率较低,当温度升高时,其吸水倍率逐渐增大,即包覆的海藻酸钙薄膜能够延缓P(AA-AM)水凝胶颗粒的吸水速率,但不影响其最终的吸水倍率。
2.2.3 矿化度对吸水倍率的影响 图5(a)、(b)分别为不同矿化度下,P(AA-AM)和P(AA-AM)@SA暂堵剂凝胶微球吸水倍率的曲线图。
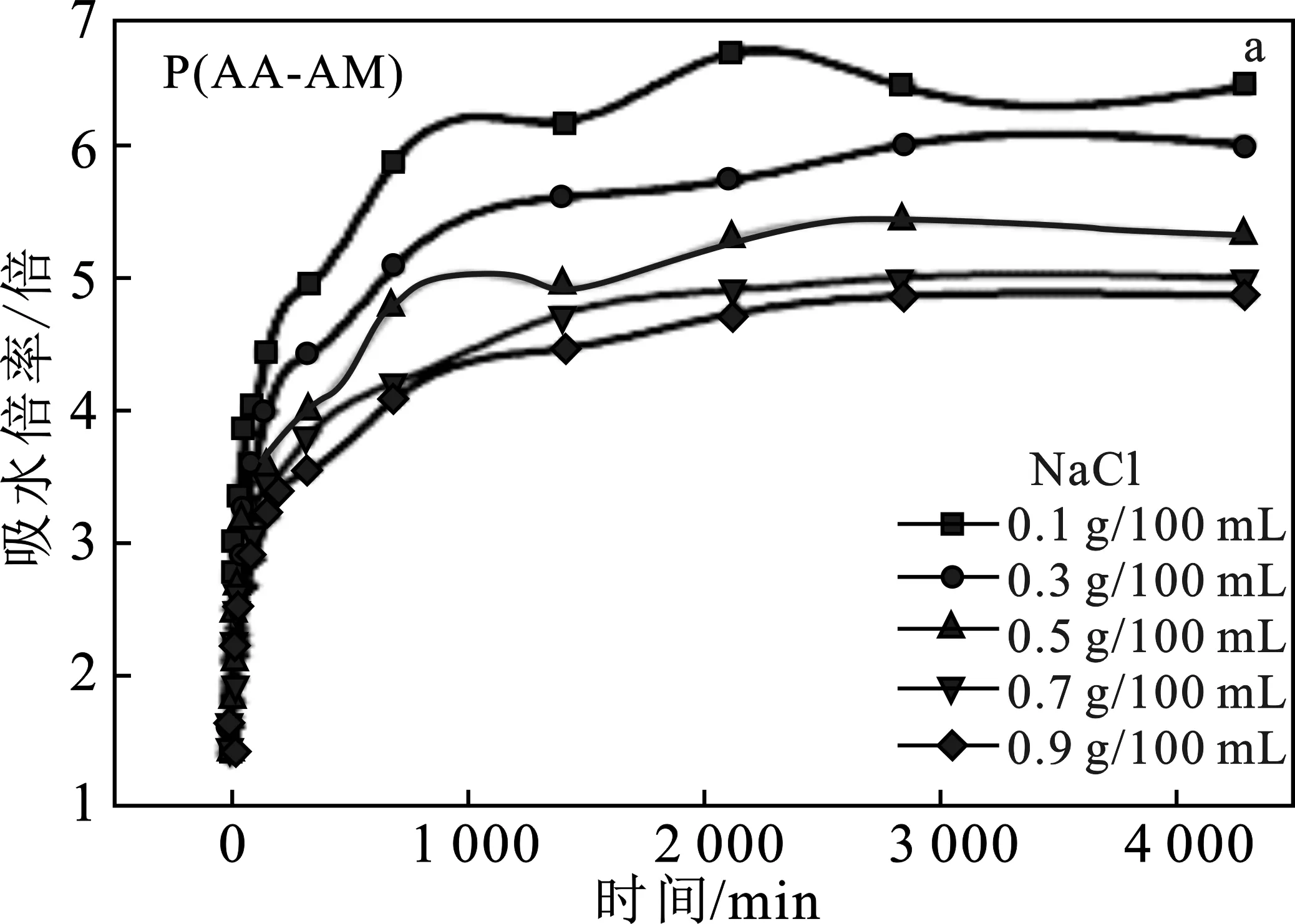
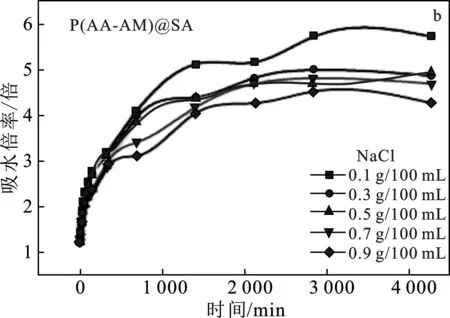
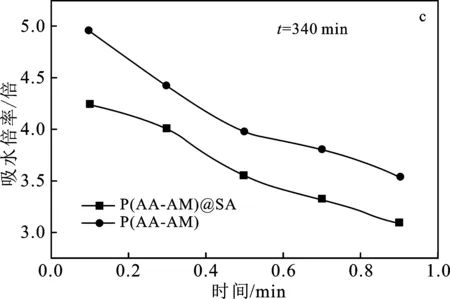
图5 不同矿化度与凝胶微球吸水倍率的关系曲线图Fig.5 Curve diagram of the relationship between different mineral content and water absorption of gel microspheres
由图5可知,P(AA-AM)、P(AA-AM)@SA凝胶微球的吸水倍率随着溶液中NaCl浓度的增大而降低,这是因为随着NaCl浓度的增大,溶液中的离子浓度越大,聚合物分子内外的渗透压降低,使得水分子很难进入微球内部,导致其吸水倍率降低[13]。图5(c)为矿化物浓度与暂堵剂凝胶颗粒在时间为340 min时吸水倍率之间的关系曲线图。因为在吸水时间为340 min时,P(AA-AM)@SA凝胶颗粒表面包覆的海藻酸钙薄膜破裂,P(AA-AM)凝胶暴露在NaCl的水溶液中,见图5(b),虽然前期P(AA-AM)@SA在NaCl的溶液中的吸水倍率较低,但是随着时间的延长其吸水倍率增大。从而说明包覆的海藻酸钙膜并不影响P(AA-AM)@SA在NaCl溶液中的吸水倍率,从而说明制备的凝胶颗粒有一定的耐盐能力。
2.2.4 复合凝胶颗粒热稳定性的评价 图6为制备的凝胶微球的热重曲线。
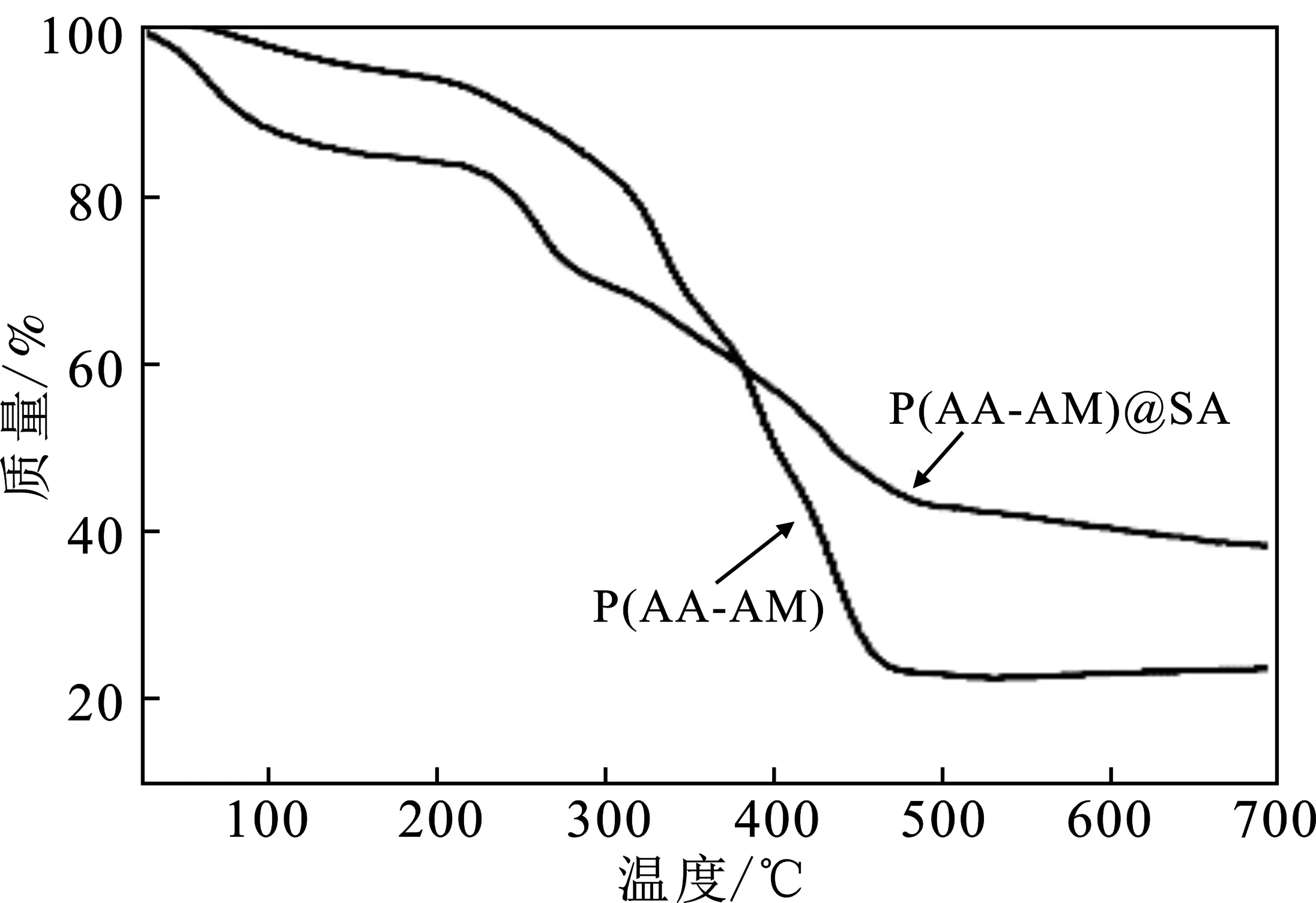
图6 暂堵剂凝胶微球的热重曲线Fig.6 Thermogravimetric curves of temporary plugging agent gel microspheres
由图6可知,P(AA-AM)和P(AA-AM)@SA凝胶颗粒的热分解均可分为3个阶段,240 ℃以下的失重均是凝胶颗粒中吸收的水分的损失。P(AA-AM)凝胶颗粒中246~450 ℃的失重是因为PAM的分解和结晶过程中水分的损失。P(AA-AM)@SA凝胶颗粒在240~500 ℃的失重,归因于海藻酸盐中多糖碳链侧链羧基等基团的分解,以及海藻酸钙的骨架碳环发生开环分解反应,分解成为H2O、CO2、CH4等,样品质量继续下降[14-15]。
3 结论
采用微流体技术及物理包覆方法制备出包覆海藻酸钠疏水膜的PAM基暂堵剂凝胶微球P(AA-AM)@SA,当海藻酸钠浓度为2%时,暂堵剂凝胶微球的性能最佳,具有较好的感温性能,即其在较低的温度时,有较低的吸水速率和吸水倍率。随着温度的升高,其吸水倍率和吸水速率逐渐增大,从而在地层的运输过程中能起到延迟吸胀的作用,不至吸水过快堵塞地层,提高其在地层中的运移能力。且在模拟地层不同矿化物浓度的条件下,暂堵剂凝胶微球具有一定的耐盐能力,有较好的热稳定性。

