分散固相萃取增强型去除脂技术结合超高效液相色谱串联质谱法测定塑料包装焙烤食品中12种抗氧化剂和紫外吸收剂
黄宇锋 温少楷 王莉 冼燕萍 郑慷 王斌 梁明 吴玉銮 胡均鹏 陈荣桥
摘要建立了QuEChERS EMRLipid技术结合超高效液相色谱串联三重四极杆质谱(UPLCMS/MS)同时检测塑料包装焙烤食品中4种抗氧化剂和8种紫外吸收剂的方法。样品经乙腈丙酮(1∶1,V/V)提取,QuEChERS EMRLipid技术净化,BEH C18 色谱柱分离,甲醇10 mmol/L乙酸铵梯度洗脱,串联质谱电喷雾正、负离子扫描,多反应监测(MRM)模式检测,采用外标法进行定量分析。结果表明,12种目标物在一定的浓度范围内线性关系良好(R2>0.9978),方法检出限(S/N=3)在5.0~10.0 μg/kg之间(除Antioxidant 2246的检出限为150.0 μg/kg外),回收率为80.3%~118.5%,日内精密度RSD(n=6)为1.7%~9.8%,日间精密度RSD(n=5)为4.5%~9.9%。本方法前处理简单快速、净化效果好、灵敏度高,适用于塑料包装焙烤食品中抗氧化剂和紫外吸收剂的检测。
关键词抗氧化剂; 紫外吸收剂; 焙烤食品; 超高效液相色谱串联质谱法
1引 言
为了提高塑料包装制品的抗氧化性能、延长使用寿命,经常会在生产过程中加入抗氧化剂和紫外吸收剂。当塑料制品接触食品时,抗氧化剂和紫外吸收剂可能会向食品尤其是含脂食品中迁移[1,2],长期摄入会危害人体健康[3,4]。许多国家和组织对食品接触塑料制品中一些抗氧化剂和紫外吸收剂规定了严格的特定迁移限量(Specific migration limit, SML)[5]。我国国标GB 96852016《食品安全国家标准 食品接触材料及制品用添加剂使用标准》[6]规定,常用的抗氧化剂2246、425、TH1790和3114以及紫外吸收剂UV0、UV9、UV71、UV329、UV326、UV327、UV234和UV360的SML为1.5~30.0 mg/kg。焙烤食品常用塑料制品包装,为了探究塑料包装材料中抗氧化剂和紫外吸收剂迁移至焙烤食品的情况,开展塑料包装焙烤食品中抗氧化剂和紫外吸收剂的检测分析具有重要意义。
目前, 抗氧化剂和紫外吸收剂的检测方法主要有液相色谱法[7,8]、气相色谱质谱联用法[9]和液相色谱质谱联用法[10,11],研究基质主要为食品接触材料或食品模拟物[1,2,7,8],缺乏焙烤食品基质的检测研究。焙烤食品基质复杂,净化除脂是难点,除脂方法主要有冷冻除脂法[12]、固相萃取法[13]、QuEChERS法[14]等。冷冻除脂和固相萃取法耗时过程较长,QuEChERS法具有快速、准确、灵敏、高效等特点而被广泛应用,其中Enhanced matrix removal lipid(EMRLipid)[15,16]是一种根据油脂类成分及大多数目标分析物结构特点设计的增强型脂质去除净化剂,对脂质具有非常强的选择吸附性,除脂效果好,已应用于高脂肪食品如鲑鱼或者动物组织中PAHs、农残、兽残等[17~19]的检测。
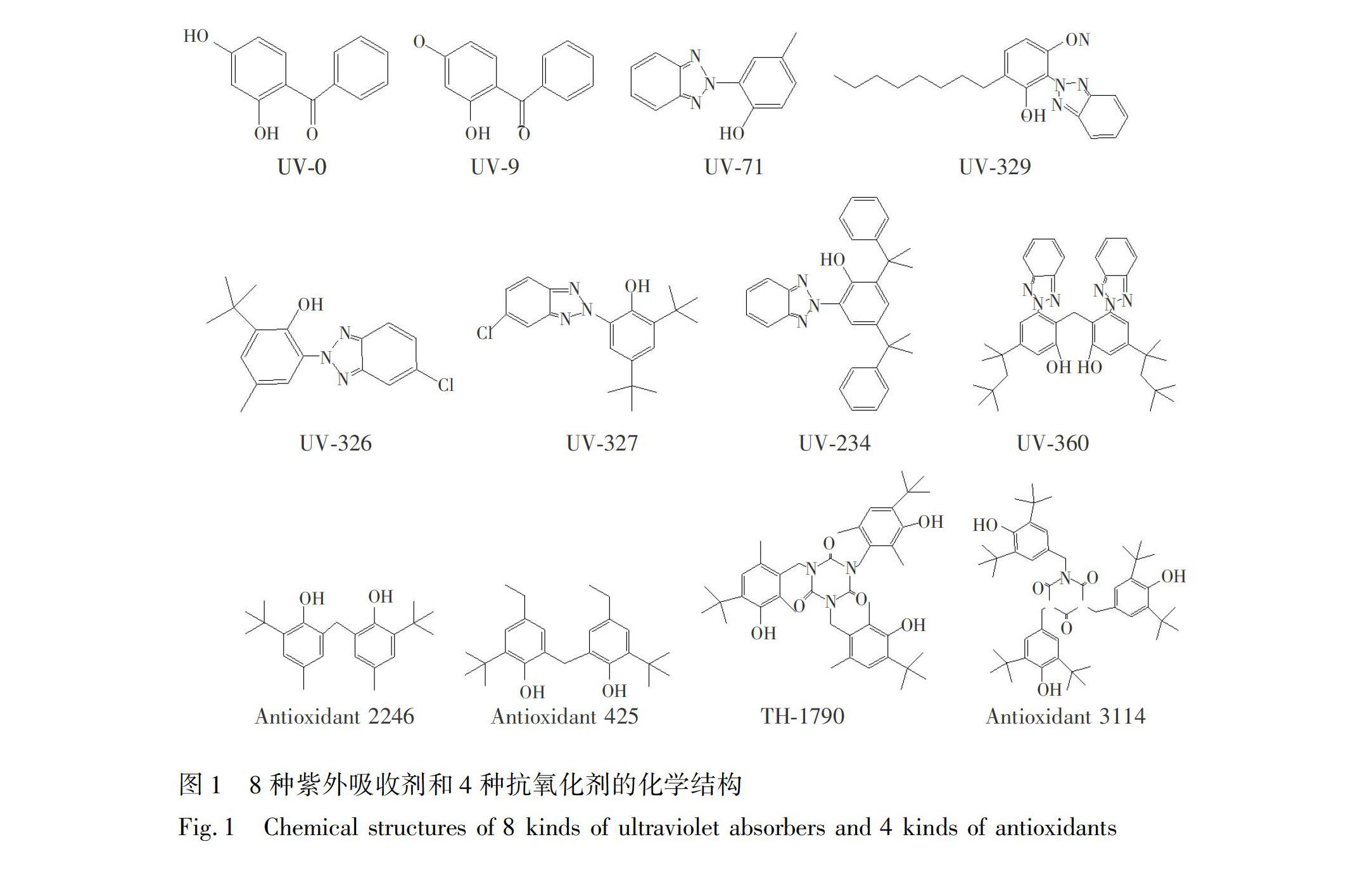
本研究采用QuEChERS EMRLipid技术,针对塑料包装焙烤食品的基质特点进一步优化改进,以达到最佳净化除脂效果,并结合液相色谱串联质谱技术,建立了同时测定塑料包装焙烤食品中12种抗氧化剂和紫外吸收剂(结构式见图1)含量的方法,方法前处理简单、净化效果好,具有较高的灵敏度和选择性,定性与定量分析准确,成功应用于市售塑料包装焙烤食品中抗氧化剂和紫外吸收剂的检测筛查。
2实验部分
2.1仪器与试剂
ACQUITYTM超高效液相色谱仪和Waters XevoTM TQ MS 三重四极杆串联质谱仪(UPLCMS/MS,美国Waters公司); MS3 digital涡旋混合器(德国IKA公司); KDC40低速离心机(安徽中科中佳公司); MilliQ超纯水仪(美国Millipore公司); 3K15高速离心机(美国Sigma公司)。
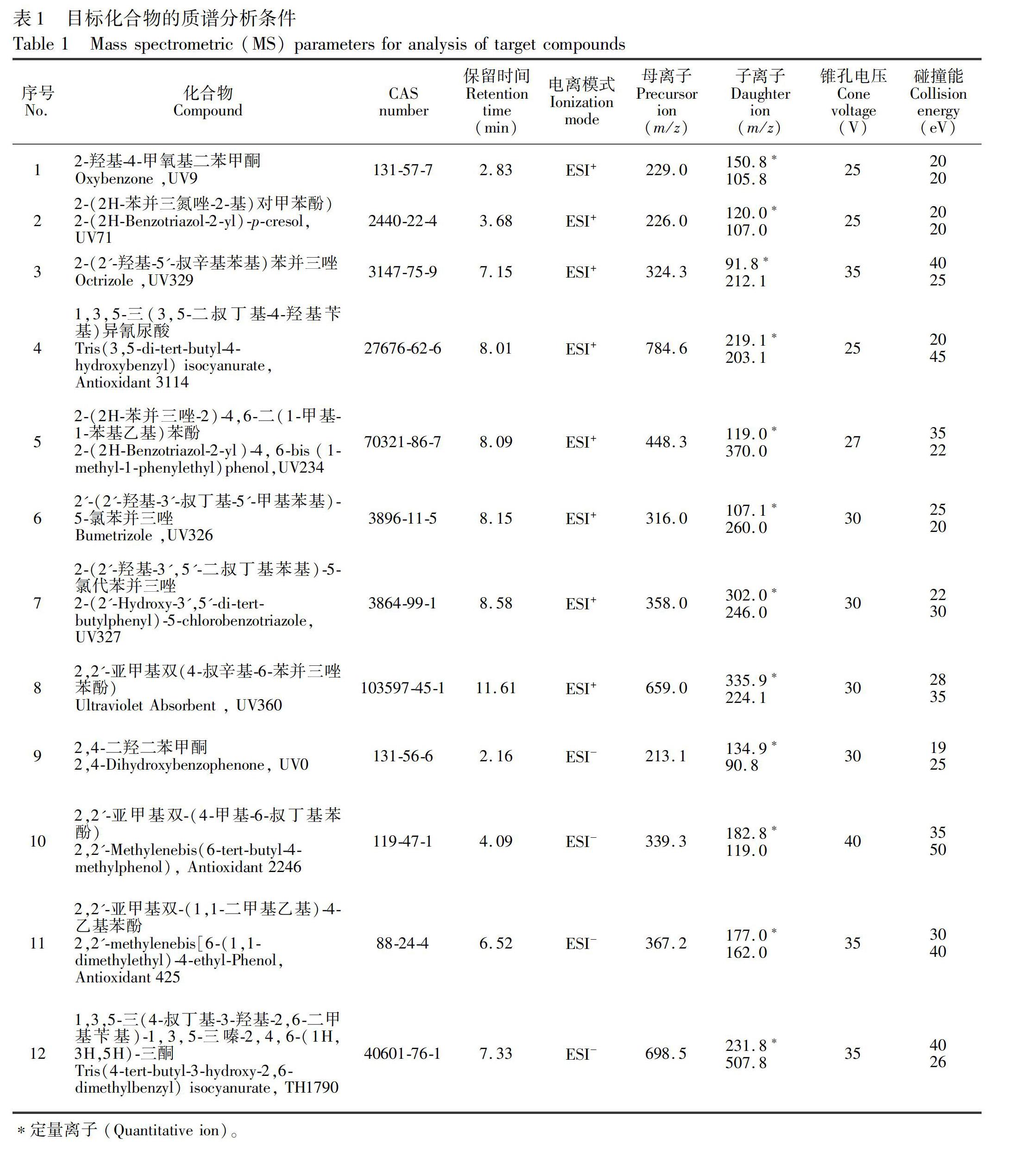
12种目标物(见表1)标准品的纯度均大于98.0%,分别购自上海安谱科学仪器有限公司和瑞士Adamas Reagent公司;乙腈、丙酮、甲醇(色谱纯,美国Fisher公司);乙酸铵(色谱纯,上海安谱科学仪器有限公司);Bond Elut EMRLipid(美国Agilent公司,包括增强型去脂分散净化管(EMRLipid dSPE,1 g,15 mL)和增强型去脂萃取盐管(EMRpolish,无水MgSO4/NaCl,15 mL)。实验用水为超纯水。
标准溶液的配制:分别准确称取标准物质各10.0 mg,配制成1000 mg/L标准储备溶液,于4℃保存。其中, UV0、UV9、TH1790、抗氧化剂2246、抗氧化剂425用甲醇溶解并定容; UV71、UV327、UV329和抗氧化剂3114用少量甲苯溶解,以甲醇定容; UV234、UV326和UV360用少量二氯甲烷溶解,以甲醇定容。使用时,用乙腈稀释成所需浓度的混合标准工作液。
15种塑料包装焙烤食品样品(饼干7种,面包2种,糕点6种)购自广州本地超市。
2.2样品前处理方法
称取已粉碎混勻的焙烤食品样品1 g(精确至0.01 g)于10 mL具塞比色管中,加入5 mL乙腈丙酮(1∶1,V/V),涡旋振荡2 min分散均匀,以2500 r/min离心5 min,取1 mL上清液于预先加入100 mg QuEChERS EMRLipid dSPE管吸附材料的2 mL塑料离心管中,涡旋2 min,13000 r/min离心3 min,上清液过0.22SymbolmA@m滤膜,供UPLCMS/MS测定。
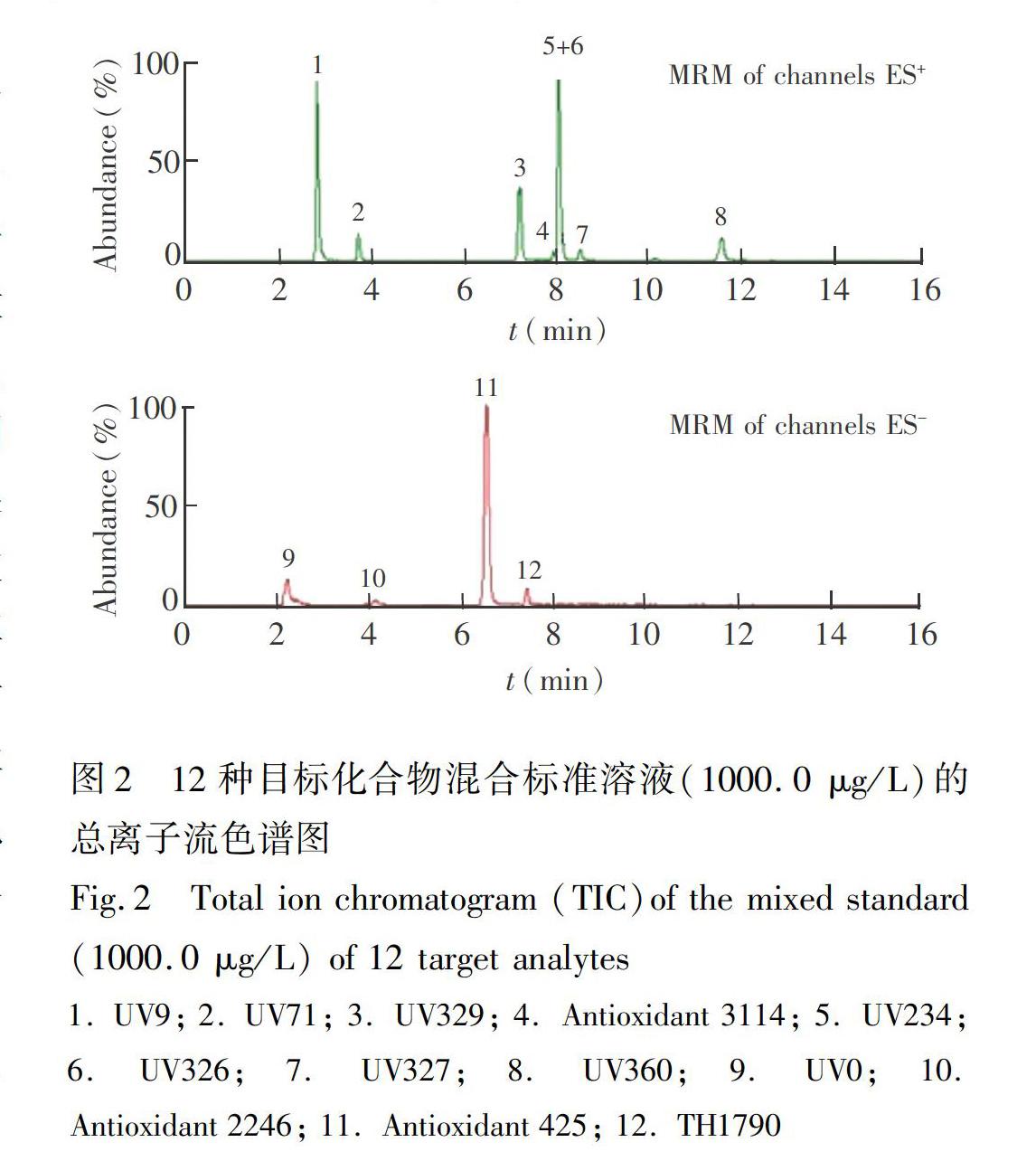
采用串联质谱检测时,样液中的共提取干扰物会与目标化合物竞争电离, 产生基质效应,影响定量分析的准确性[21,22]。本研究采用Matusewski等[22]建立的方法评价基质效应,即将同浓度的阴性基质标准溶液目标物响应值与纯溶剂标准溶液目标物响应值进行比较:比值=1时,表明不存在基质效应; 比值>于1时,表明存在基质增强作用; 比值<1时,表明存在基质抑制作用; 比值介于0.8~1.2时,通常认为基质效应较弱,可以忽略。选取阴性面包、饼干、蛋糕3种试样,以按2.2节处理后的基质样液分别配制浓度为100 μg/L的基质混合标准溶液,与纯溶剂混合标准溶液(100 μg/L)进行检测。结果表明,经EMRLipid净化后的3种样品基质中,12种目标物的比值均在0.9~1.2之间,说明本方法基质干扰较小,基质效应可忽略。
3.5线性关系与检出限
在优化的条件下,测定系列混合标准工作液,以各待测物定量离子对的峰面积为纵坐标(y),以相应的质量浓度为横坐标(x, μg/L),绘制标准曲线,得到各待测物的线性方程。以3倍信噪比(S/N=3)计算仪器检出限(LOD),结合前处理条件的稀释倍数,确定方法的检出限(LOD,S/N=3)和定量限(LOQ,S/N=10)。实验结果见表2,12种待测物在相应的浓度范围内线性关系良好,相关系数均大于0.9978,LOD为5.0~150.0 μg/kg,LOQ为15.0~500.0 μg/kg。
3.6回收率與精密度
选取空白面包、饼干和蛋糕样品,分别进行3个水平(MLOQ, 2×MLOQ, 10×MLOQ)的加标回收和精密度实验(n=6),以中间添加水平连续实验5 d,考察方法的日间精密度。由表3可知, 12种目标物的平均回收率为80.3%~118.5%,日内精密度RSD(n=6)为1.7%~9.8%,日间精密度RSD(n=5)为4.5%~9.9%。
3.7实际样品分析
采用本方法测定了市售15个塑料包装焙烤食品(包括面包、蛋糕和饼干),其中,10个样品检出抗氧化剂Antioxidant 2246,含量为0.2~1.1 mg/kg,低于我国国标对Antioxidant 2246的特定迁移限量(1.5 mg/kg)[6]要求; 其它样品均未检出目标物。在阳性沙琪玛样品中抗氧化剂Antioxidant 2246的TIC图和提取离子色谱图见图5。
4结 论
基于QuEChERS EMRLipid净化技术,建立了超高效液相色谱串联质谱法同时测定塑料包装焙烤食品中12种抗氧化剂和紫外吸收剂的方法。本方法利用EMRLipid中特殊聚合物材料在高脂样品中高效脂质去除的优势,方法溶剂消耗低,净化效果好,操作快速简便,方法的灵敏度和准确度高,适用于塑料包装焙烤食品中抗氧化剂和紫外吸收剂的检测。
References
1WANG ChengYun, LI ChengFa, LIN JunFeng, XIE TangTang, CHU NaiQing. Chinese Journal of Chromatography, 2017, 35(5): 509-519
王成云, 李成发, 林君峰, 谢堂堂, 褚乃清. 色谱, 2017, 35(5): 509-519
2WANG Li, LI ZeRong, CHEN LiWei, YOU HaiYun, WU ChuSen, HAN WanQing, XIAN YanPing, LUO HaiYing. Food Safety and Quality Detection Technology, 2015, 6(12): 4726-4733
王 莉, 李泽荣, 陈立伟, 尤海云, 吴楚森, 韩婉清, 冼燕萍, 罗海英. 食品安全质量检测学报, 2015, 6(12): 4726-4733
3Scholler D,Vergnaud J M, Bouquant J, Vergallen H, Feigenbaum A. Packag. Technol. Sci., 2003, 16(5): 209-220
4Kim J, Isobe T, Ramaswamy B R, Chang K H, Amano A, Miller T M, Siringan F P, Tanabe S. Chemosphere, 2011, 85(5): 751-758
5Commission Regulation (EU) No 10/2011 of 14 January 2011 on Plastic Materials and Articles Intended to Come Into Contact with Food. Off. J. Eur. Union,2011, L372: 14-21
6GB 96852016.Standard for the Uses of Additives in Food Contact Materials and Products. National Standards of the People's Republic of China
食品接触材料及制品用添加剂使用标准. 中华人民共和国国家标准. GB 96852016
7QIU Yue, LI GenRong, LONG Mei, LI YanFei, XIA ZhiNing. Chinese Journal of Chromatography, 2019, 37(9): 990-995
邱 月, 李根容, 龙 梅, 李沿飞, 夏之宁. 色谱, 2019, 37(9): 990-995
8Li C F, Li Y, Chen Z N, Liang F, Chen X H, Wu S J, Li Y T, Sun X Y. Food Anal. Methods, 2014, 7(9): 1755-1762
9Vila M, Celeiro M, Lamas J P, GarciaJares C, Dagnac T, Llompart M. J. Hazard. Mater., 2017, 323: 45-55
10CAI Fa, DUAN XiaoJuan, MOU ZhiChun, WANG ManXia, WANG Yan, XU Qin. Journal of Instrumental Analysis, 2012, 31(z1): 45-49
蔡 发, 段小娟, 牟志春, 王曼霞, 王 岩, 徐 琴. 分析测试学报, 2012, 31(z1): 45-49
11Kim J M, Choi S H, Shin G H, Lee J H, Kang S R, Lee K Y, Lim H S, Kang T S, Lee O H. Food Chem., 2016, 213: 19-25
12WANG GuoQing, WANG ZongYi, CHENG MingJie, ZHAI MengTing, MA MengMeng, HUANG ManQing. Food Science, 2018, 39(8): 282-287
王国庆, 王宗义, 程明捷, 翟孟婷, 马蒙蒙, 黄漫青. 食品科学, 2018, 39(8): 282-287
13Paoloni A, Solfrizzo M, Bibi R, Pecorelli I. J. Environ. Sci. Health B, 2018, 53(5): 327-333
14LI Rong, BO YanNa, LU JunWen, LIN QinBao, HUANG ZhiQiang, CHEN LiSi. Chinese Journal of Chromatography, 2016, 34(5): 502-511
李 蓉, 薄艳娜, 卢俊文, 林勤保, 黄志强, 陈丽斯. 色譜, 2016, 34(5): 502-511
15WU Yan, ZHAO Wei, LIU Yong, JIANG Bing, WEI DongXu, GOU Yue, LI LiLi, HAN Feng, ZU YuanGang. Chinese J. Anal. Chem., 2016, 44(6): 950-957
吴 岩, 赵 伟, 刘 永, 姜 冰, 魏冬旭, 勾 越, 李丽丽, 韩 峰, 祖元刚. 分析化学, 2016, 44(6): 950-957
16Huang Y S, Li C, Hu H Y, Wang Y T, Shen M Y, Nie S P, Chen J, Zeng M M, Xie M Y. J. Agric. Food Chem., 2019, 67: 5017-5025
17Urban M, Lesueur C. Food Anal. Methods, 2017, 10(7): 1-14
18Han L, Matarrita J, Sapozhnikova Y, Lehotay S J. J. Chromatogr. A, 2016, 1449: 17-29
19WANG Fei, MI JieBo, LI ShuJing, CHEN QiYong, WU Hua. Journal of Instrumental Analysis, 2017, 36(2): 272-275
王 飞, 宓捷波, 李淑静, 陈其勇, 吴 华. 分析测试学报, 2017, 36(2): 272-275
20XIAO XiaoFeng, WANG JianLing, CHEN Tong, LIU TingFei, HE Jun, DENG HongYi, YANG JuanJuan. Journal of Instrumental Analysis, 2015, 34(9): 1021-1026
肖晓峰, 王建玲, 陈 彤, 刘艇飞, 何 军, 邓弘毅, 杨娟娟. 分析测试学报, 2015, 34(9): 1021-1026
21CHEN JieFeng, LIANG Ming, XIAN YanPing, WU YuLuan, WEN ShaoKai, WANG Bin, WANG Li, HOU XiangChang, LIU DongHong. Chinese J. Anal. Chem., 2019, 47(8): 1258-1266
陈杰锋, 梁 明, 冼燕萍, 吴玉銮, 温少楷, 王 斌, 王 莉, 侯向昶, 刘冬虹. 分析化学, 2019, 47(8): 1258-1266
22Matuszewski B K, Constanzer M L, ChavezEng C M.Anal. Chem., 2003, 75(13): 3019-3030