钯催化间甲基苯乙酸和布洛芬的间位烯基化反应
焦 博,杜海武,戴振华,王景芸
(辽宁石油化工大学化学化工与环境学部,辽宁抚顺113001)
C-H作为自然界最基本、最普遍的惰性化学键,广泛存在有机分子中。无论对能源还是对可持续发展来讲,直接实现惰性C-H的官能化反应都具有重要的意义。例如,在能源方面,通过CH活化和官能化可以将低碳的化石燃料转化成其他高碳的化学产品,这将是能源和化工产品链接的新纽带。与传统的官能团转化相比,惰性C-H在过渡金属催化下,一步实现官能化反应,避免了试剂浪费和原料预先官能化等步骤,展示出了高的原子经济性、步骤经济性以及环境友好等特点,在药物合成、材料、能源研究中具有重要意义,近年来已发展成为有机化学中最活跃的研究领域之一[1-2]。
近年来,导向基参与过渡金属催化的C-H活化发展迅速[3-7]。通过向底物中引入导向基团可以控制C-H官能化反应的选择性。在此类研究中,过渡金属催化的芳基邻位官能化反应报道较多[8-10]。但是,这种策略大多数实现的是芳烃邻位的C-H官能化,然而定位活化导向基团的间位或对位的芳基C-H官能化反应报道较少,主要是因为反应过程中可能会形成稳定性较差的大环金属过渡态且能量较高,是一项具有挑战性的难题[11-22]。最近,余金权课题组通过对导向基团的设计,在过渡金属催化下,成功地实现了间位C-H官能化反应,为间位C-H官能化反应提供一个新的途径[23-25]。随后,K.L.Tan 课题组[26]、D.Maiti课题组[27]、Li Gang 课题组[29]相继报道了导向基参与的芳烃间位C-H官能化反应。
尽管选择性C-H反应取得了一定进展,但是芳烃类化合物间位的C-H官能团化反应底物的适用范围仍然具有一定局限性。在众多芳烃衍生物中,官能化的苯乙酸类衍生物具有良好的药理活性,如布洛芬、止疼或退热的药物等。另一方面,将烯烃直接引入芳烃类化合物中,具有非常重要的合成意义,因为烯烃是一类重要的有机合成中间体,可以发生许多重要的化学转化[30-31]。本文利用U-型模板导向基的策略,将配位能力较强的嘧啶作为模板,在钯催化下,实现苯乙酸衍生物的间位烯基化反应。
1 实验部分
1.1 仪器与试剂
试剂:乙酸乙酯、石油醚,分析纯,天津市富宇精细化工有限公司;二氯甲烷(DCM)、1,2-二氯乙烷(DCE)、四氢呋喃(THF)、甲醇(MeOH)、六氟异丙醇(HFIP)、异丙醇、三氟乙醇(TFE),分析纯,国药集团化学试剂有限公司;丙烯酸乙酯、醋酸铜(Cu(OAc)2)、醋酸银(AgOAc)、碳酸银(Ag2CO3)、氧化银(Ag2O)、磷酸钾(K3PO4)、三乙胺(Et3N)、5-溴嘧啶、2-羟基苯硼酸、间甲基苯乙酸,分析纯,安耐吉试剂有限公司;氢氧化锂(LiOH,质量分数99.9%)、N-乙酰甘氨酸(Ac-Gly-OH,质量分数99.0%)、N-乙酰-L-丙氨酸(Ac-Ala-OH,质量分数98.0%)、N-乙酰-L-缬氨酸(Ac-Val-OH,质量分数98.0%)、N-乙酰-L-苯丙氨酸(Ac-Phe-OH,质量分数98.0%)、N-乙酰-L-亮氨酸(Ac-Leu-OH,质量分数98.5%),上海柏卡试剂有限公司;醋酸钯(Pd(OAc)2,质量分数99.0%),北京百灵威有限公司。
仪器:ME104E/02电子天平,上海精密科学有限公司;MS-H-Pro+恒温磁力搅拌器,北京欣维尔仪器有限责任公司;RE-52A旋转蒸发仪,上海亚荣生化仪器厂;Agilent Q-TOF 6224 HRMS(ESI)高分辨质谱仪,安捷伦科技有限公司;AVANCE 500核磁共振波谱仪,布鲁克公司;Universal(2440/750/900)超级净化手套箱,米开罗那(中国)有限公司。
1.2 苯乙酸衍生物间位烯基化反应(以3-甲基苯乙酸-2-(5-嘧啶基)酯为例)
1.2.1 原料的合成 在圆底烧瓶中分别加入0.75 mmol 2-羟基苯硼酸(S1)、0.50 mmol 5-溴嘧啶(S2)、0.007 5 mmol Pd(OAc)2、1.00 mmol K3PO4和4.0 mL体积分数50%的异丙醇水溶液,80℃下搅拌12 h,如图1所示。反应结束后,将反应液倒入分液漏斗,加入饱和食盐水,用乙酸乙酯萃取3次,合并有机相,将有机相用无水MgSO4干燥,柱层析分离纯化(V(石油醚)/V(乙酸乙酯)=2∶1),蒸干后得白色固体2(-5-嘧啶基)苯酚(S3),计算分离收率。

图1 2-(5-嘧啶基)苯酚的合成
在圆底烧瓶中分别将2.00 mmol S3和0.75 mmol Et3N加入10 mL的二氯甲烷中,在0℃下缓慢地将2.00 mmol 3-甲基苯乙酰氯滴加到反应液中,搅拌20 min,再将反应温度升至室温搅拌12 h,如图2所示。反应结束后,将反应液倒入分液漏斗中,加入饱和食盐水,用乙酸乙酯萃取3次,合并有机相,将有机相用无水MgSO4干燥,柱层析分离纯化(V(石油醚)/V(乙酸乙酯)=3∶1),即得3-甲基苯乙酸-2-(5-嘧啶基)酯(1a),计算分离收率。
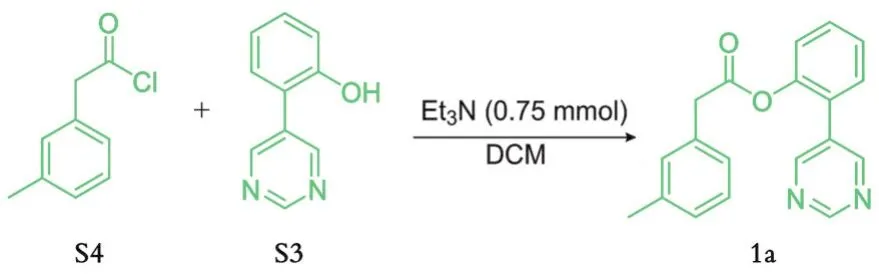
图2 3-甲基苯乙酸-2-(5-嘧啶基)酯的合成
1.2.2 烯基化反应实例 实例1:反应器抽真空通入氮气置换3次,依次加入0.20 mmol 1a、0.30 mmol丙烯酸乙酯(2a)、0.02 mmol Pd(OAc)2、0.04 mmol Ac-Gly-OH、0.30 mmol(82.7 mg)Ag2CO3、1.00 mL HFIP,80℃搅拌24 h,如图3所示。反应结束后,用旋转蒸发仪抽除溶剂,粗产物通过柱层析分离纯化(V(石油醚)/V(乙酸乙酯)=3∶1),即得间甲基苯乙酸间位烯基化反应产物(3aa),计算分离收率。

图3 间甲基苯乙酸酯类衍生物1a间位烯基化反应
实例2:反应器抽真空通入氮气置换3次,依次加入 0.20 mmol布洛芬衍生物(1b)、0.30 mmol丙烯酸乙酯(2a)、0.02 mmol Pd(OAc)2、0.04 mmol Ac-Gly-OH、0.30 mmol Ag2CO3、1.00 mL HFIP,80 ℃搅拌24 h,如图4所示。反应结束后,用旋转蒸发仪抽除溶剂,粗产物通过柱层析分离纯化(V(石油醚)/V(乙酸乙酯)=3∶1),即得布洛芬衍生物间位烯基化反应产物(3ba),计算分离收率。
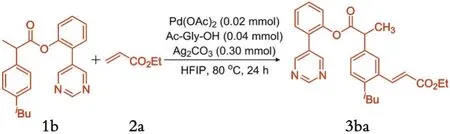
图4 布洛芬衍生物1b间位烯基化反应
1.2.3 导向基的移除及回收 在圆底烧瓶中分别加入0.10 mmol 3aa、0.60 mmol(25.2 mg)氢氧化锂、2.40 mL甲醇、1.20 mL四氢呋喃、0.60 mL H2O,室温下搅拌12 h,如图5所示。反应结束后,将反应液倒入分液漏斗中,加入饱和食盐水,用乙酸乙酯萃取3次,合并有机相,将有机相用无水Mg-SO4干燥,柱层析分离纯化(V(石油醚)/V(乙酸乙酯)=3∶1),分别得到 3-甲基-5-羧甲基肉桂酸(4a)和S3,计算分离收率。
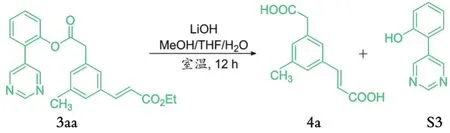
图5 导向基的移除与回收
2 结果与讨论
2.1 间位烯基化反应条件的优化
2.1.1 催化剂和氧化剂对间位烯基化反应的影响
以间甲基苯乙酸间位烯基化反应为模型体系,在底物1a物质的量为0.20 mmol、丙烯酸乙酯物质的量为 0.30 mmol、溶剂HFIP体积为1.00 mL、配体Ac-Gly-OH物质的量为0.04 mmol、氧化剂物质的量为0.40 mmol的条件下,80℃反应24 h,分别考察催化剂Pd(OAc)2对间位烯基化反应的促进作用和不同氧化剂对反应的影响,结果见表1。
由表1可知,当未使用催化剂时,反应几乎没有发生,仅通过硅胶层析法观察到痕量产物的生成,而未得到分离产物;当使用0.02 mmol Pd(OAc)2催化剂时,间位烯基化反应才得以顺利进行,表明催化剂Pd(OAc)2对间甲基苯乙酸的间位烯基化反应起关键促进作用。间甲基苯乙酸间位烯基化反应经历了一步还原消除历程,所以氧化剂是实现该催化体系正常循环的关键。Cu(OAc)2为氧化剂时,反应选择性最好,高达96.8%,但目标产物的收率只有55%;AgOAc和Ag2CO3为氧化剂时,收率显著增加,而产物的选择性也大于95.0%,尤其是Ag2CO3作氧化剂时,可以获得80%的收率。因此,反应的最优氧化剂为Ag2CO3。

表1 催化剂及氧化剂对间位烯基化反应的影响
2.1.2 配体对间位烯基化反应的影响 同样选择0.20 mmol的1a和0.30 mmol丙烯酸乙酯进行间位烯基化反应,在溶剂HFIP体积为1.00 mL、催化剂Pd(OAc)2物质的量为0.02 mmol、配体物质的量为0.04 mmol、氧化剂物质的量为0.40 mmol的条件下,80℃反应24 h,考察配体对间位烯基化反应的影响,结果见表2。

表2 配体对间位烯基化反应的影响
由表2可知,配体对间位烯基化反应活性影响很大,当配体为Ac-Ala-OH、Ac-Val-OH、Ac-Phe-OH、Ac-Leu-OH时,收率均低于50%,当配体为Ac-Gly-OH时,收率和选择性都相对较高。因此,最佳配体为Ac-Gly-OH。
2.1.3 溶剂对间位烯基化反应的影响 在催化剂Pd(OAc)2物质的量为0.02 mmol、氧化剂Ag2CO3的物质的量为0.40 mmol、配体Ac-Gly-OH物质的量为 0.04 mmol、底物 1a物质的量为 0.20 mmol、丙烯酸乙酯物质的量为0.30 mmol的条件下,80℃反应24 h,考察溶剂对间位烯基化反应的影响,结果见表3。
由表3可知,三种溶剂进行的间位烯基化反应选择性接近,均高于95.0%,但活性差异较大;当溶剂为DCE和TFE时,收率仅为39%和68%,而当溶剂为HFIP时,收率可增大至80%。因此,最佳的反应溶剂为HFIP。

表3 溶剂对间位烯基化反应的影响
2.1.4 反应温度对间位烯基化反应的影响 以0.02 mmol Pd(OAc)2为催化剂,0.40 mmol Ag2CO3为氧化剂,0.04 mmol Ac-Gly-OH为配体进行间位烯基化反应,底物1a和丙烯酸乙酯的物质的量分别为0.20 mmol和0.30 mmol,在溶剂HFIP中反应24 h,考察反应温度对间位烯基化反应的影响,结果见表4。

表4 反应温度对间位烯基化反应的影响
由表4可知,当反应温度过低时,反应活性不高,反应不能进行;当温度升高至60℃时,收率增大至37%,继续升高温度至80℃,收率最大可增加至80%;当温度超过80℃时,收率和选择性均开始降低。因此,最佳反应温度为80℃。
2.2 代表性产物的表征
化合物3aa的表征数据见图6。1H NMR(400 MHz,CDCl3) δ 9.14(s,1H),8.71(s,2H),7.64(d,J=16.0 Hz,1H),7.49~7.44(m,1H),7.40~7.35(m,2H),7.26(s,1H),7.21(d,J=8.0 Hz,1H),7.14(s,1H),6.98(s,1H),6.42(d,J=16.0 Hz,1H),4.26(q,J=7.1 Hz,2H),3.68(s,2H),2.34(s,3H),1.34(t,J=7.1 Hz,3H);13C NMR(100 MHz,CDCl3) δ 169.3,166.9,157.6,156.3,147.9,144.2,139.2,135.0,133.1,131.8,131.1,130.6,130.4,128.0,127.8,127.0,126.0,123.2,118.7,60.5,40.9,21.2,14.3;HRMS(ESI):计算值 C24H22N2O4([M+H]+)403.165 2,实 际 值403.165 8。分析结果表明,所得产物与目标产物结构一致。

图6 化合物3aa的表征
化合物3ba的表征数据见图7。1H NMR(400 MHz,CDCl3)δ 9.08(s,1H),8.67(s,2H),7.99(d,J=16.0 Hz,1H),7.48~7.43(m,1H),7.39(d,J=1.2 Hz,1H),7.36~7.33(m,2H),7.13(d,J=7.9 Hz,1H),7.11~7.06(m,2H),6.33(d,J=15.8 Hz,1H),4.28(q,J=7.2 Hz,2H),3.80(q,J=7.2 Hz,1H),2.62(d,J=7.2 Hz,2H),1.88~1.78(m,1H),1.46(d,J=7.2 Hz,3H),1.35(t,J=7.2 Hz,3H),0.93(d,J=6.6 Hz,6H);13C NMR(100 MHz,CDCl3) δ172.4,167.0, 157.5,156.3, 148.0,142.1,140.8,137.1,133.8,131.5,131.0,130.5,130.3,128.5,127.9,126.8,125.4,123.1,119.6,60.5,45.0,42.1,30.4,22.5,22.4,18.3,14.3;HRMS(ESI):计 算 值 C28H30N2O4([M+H]+)459.227 8,实际值459.228 9。分析结果表明,所得产物与目标产物结构一致。
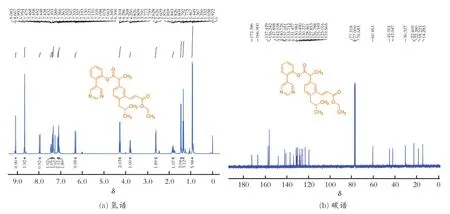
图7 化合物3ba的表征
3 结 论
以Pd(OAc)2和Ag2CO3为催化剂,嘧啶为导向基模板,实现了间甲基苯乙酸和布洛芬的高效和高选择性间位烯基化反应。对反应条件优化结果表明,催化剂、氧化剂、配体、溶剂和反应温度均为苯乙酸衍生物间位烯基化反应的重要影响因素,在最优化条件下,3-甲基苯乙酸-2-(5-嘧啶基)酯和丙烯酸乙酯反应24 h,间甲基苯乙酸间位烯基化反应收率达到80%。

