双重抗神经元抗体阳性自身免疫性脑炎临床特征分析
戴俊杰 石露
自身免疫性脑炎(autoimmune encephalitis,AE)是指一类由自身免疫机制介导的脑炎,多以急性或亚急性起病,以癫痫发作、认知功能障碍及精神行为异常等边缘性脑炎为主要临床表现,部分患者可合并肌强直、肌痛等莫旺(Morvan)综合征表现[1]。AE患病比例占脑炎患者的10%~20%[1]。AE的诊断需通过自身抗体检测、脑电图及头颅MRI、正电子发射计算机断层显像(PET)等检查后,排除感染性脑病和其他自身免疫性疾病[1]。自身抗体阳性是诊断AE的关键因素,AE抗体主要分两类,一类是抗神经元表面抗原抗体,主要包括N-甲基-D-天冬氨酸受体(NMDAR)抗体、γ-氨基丁酸B型受体(GABABR)抗体、富含亮氨酸胶质瘤失活蛋白1(LGI1)抗体、接触蛋白相关蛋白2(CASPR2)抗体、α-氨基-3-羟基-5-甲基-4-异吧恶唑丙酸受体(AMPAR)抗体等;另一类是抗神经元细胞内抗原抗体,如抗Hu、抗Yo抗体等副肿瘤相关抗体[2]。任海涛等[3]报道双重抗体阳性的AE较少。本研究收集了8例双重抗神经元抗体阳性的AE患者,总结其临床特征,以期提高临床医师对该病的认识。
1 对象和方法
1.1 对象 收集2012年12月至2019年11月在宁波市医疗中心李惠利医院诊治的双重抗神经元抗体阳性的AE患者8例,均符合AE确诊标准[1]。
1.2 抗神经元抗体检测方法 根据神经系统抗原谱1检测试剂盒(德国Euroimmun AG公司)说明书,采用基于细胞的间接免疫荧光法(IIF)检测血清和(或)脑脊液中的AE抗体(包括抗 NMDAR抗体、抗 GABABR受体抗体、抗LGI1抗体、CASPR2抗体和抗AMPAR抗体)。稀释后的标本与用含有人靶基因序列的质粒(德国Euroimmun AG公司)转染的人胚肾293细胞反应,异硫氰酸荧光素(FITC)标记的抗人IgG作为第二抗体。根据阳性和阴性对照的细胞质免疫荧光强度确定阳性和阴性反应。采用IIF和蛋白免疫印迹法检测血清和(或)脑脊液中的副肿瘤相关抗体(包括抗 Yo、Hu、Ri、Ma2、CV2、amphiphysin抗体),IIF方法同上述AE相关抗体检测,其试剂盒为DL-1111-2G(德国Euroimmun AG公司)。蛋白免疫印迹法采用副肿瘤相关抗体检测试剂盒(德国 Euroimmun AG 公司),检验条上含有 Hu、Yo、Ri、Ma2、CV2、amphiphysin蛋白抗原条带。检测步骤:滴加待检血清和脑脊液,血清按1∶50稀释,脑脊液为原液,室温孵育60min;冲洗;滴加碱性磷酸酶结合的山羊抗人免疫球蛋白抗体,室温孵育60min;冲洗;滴加显色底物,室温孵育10min;冲洗。阳性判定参照阳性对比和阴性对比条带。
1.3 治疗及随访评估 患者均接受激素冲击和免疫球蛋白治疗,并对癫痫发作和精神症状进行对症治疗,并给予相应支持治疗,确诊或怀疑肿瘤的患者建议其进行针对性肿瘤治疗。每1~3个月通过电话或门诊对患者进行随访,随访截止时间为2019年12月。通过改良Rankin量表(mRS)评估治疗效果和预后:0分为完全缓解,1~2分为显著缓解,>2分为部分缓解,治疗或随访后mRS评分不变、增加或死亡为无效。
1.4 观察指标 评估8例双重抗神经元抗体阳性的AE患者的临床特征、抗体检测结果、脑电图及影像学表现,治疗和随访情况。
2 结果
2.1 抗神经元抗体检测结果 例1、例2、例3患者的血液和(或)脑脊液中检出抗NMDAR抗体和抗GABABR抗体;例4、例5、例6患者的血液和(或)脑脊液都中检出抗GABABR抗体(图1a),其中例4患者血液中还检出抗Yo抗体(图1b),例5、例6患者的脑脊液和(或)血液中检出抗Hu抗体;例7、例8患者的血液和(或)脑脊液中同时检出抗LGI1抗体和抗CASPR2抗体,见表1。
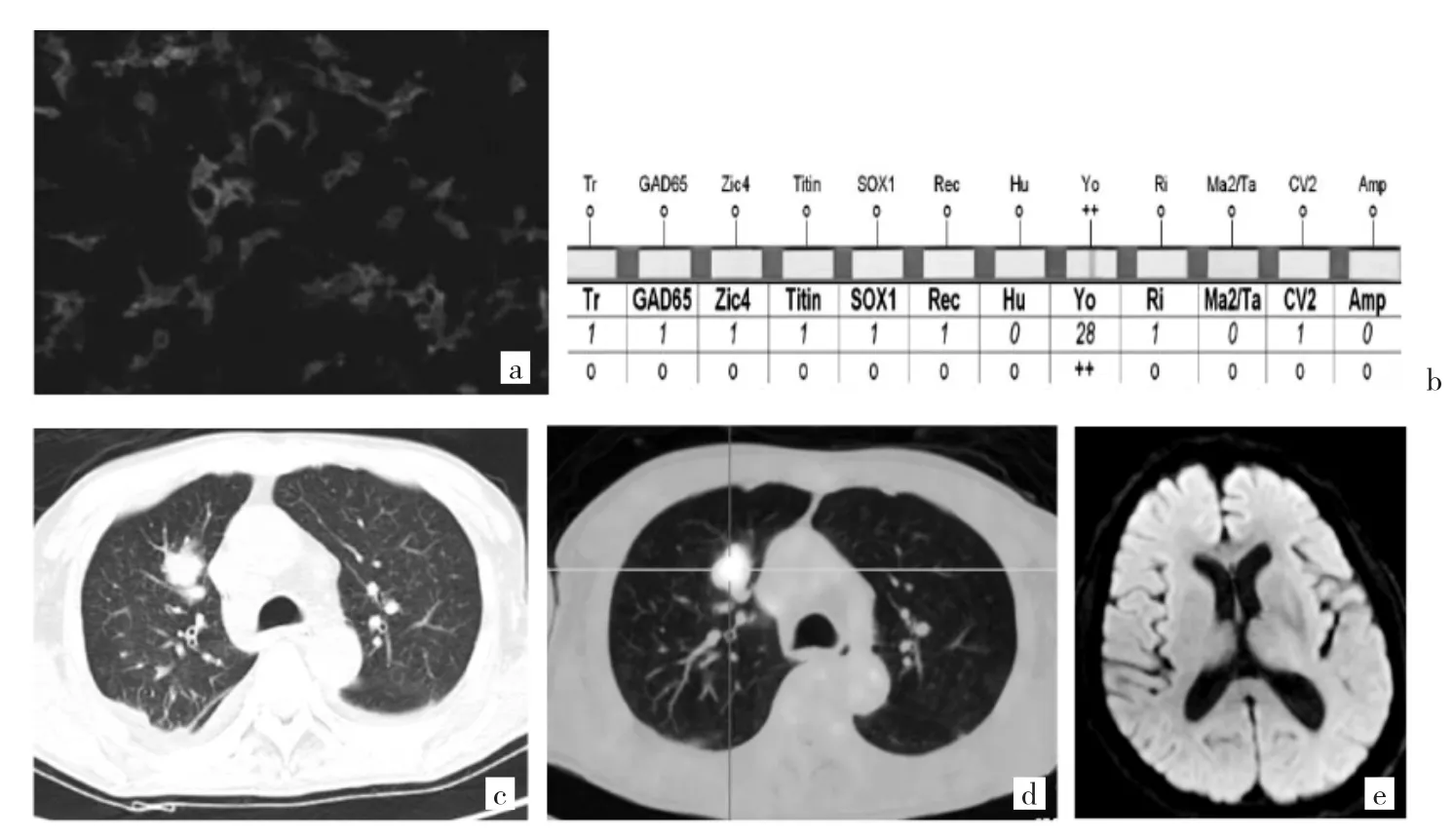
图1 例4,男,69岁。临床表现为癫痫发作、记忆力减退、意识障碍、精神行为异常等(a:血清抗GABABR抗体阳性;b:血清抗Yo抗体阳性;c:胸部CT可见右上肺占位、纵隔及右侧肺门多发肿大淋巴结;d:PET-CT示右上肺上叶占位,右肺门区肿大淋巴结,氟代脱氧葡萄糖代谢均异常增高,伴右肺门转移性淋巴结;e:头颅MRI示左侧丘脑DWI稍高信号)

表1 8例患者的临床表现、抗体检测结果
2.2 临床表现 8例患者中,男3例,女5例;发病年龄35~72岁;病程11~43d。8例患者的主要临床表现均为癫痫发作、认知功能障碍、精神行为异常等边缘性脑炎表现,4例患者合并肺癌,其中例4患者虽未经病理确诊,但其胸部影像学表现支持肺癌诊断(见图1c-d)。例4患者合并有小脑性共济失调,而例8患者合并肌强直、肌痛等Morvan综合征表现,合并肺癌的例4、例5患者合并有低钠血症。
2.3 辅助检查结果 8例患者脑脊液白细胞计数为(10~140)×106/L,均轻度增高[参考范围:(0~8)×106/L];脑脊液蛋白定量为0.430~1.181g/L(参考范围:0.15~0.45g/L),大部分增高。8例患者脑电图均表现为异常慢波,例5同时存在颞叶局灶性痫样放电。头颅MRI表现方面,8例患者中4例(例3、例5~7)出现边缘系统为主的异常信号,呈现为T1加权成像(T1WI)低信号,T2加权成像(T2WI)/液体衰减反转恢复(FLAIR)序列高信号,而例4患者表现为左侧丘脑弥散加权成像(DWI)稍高信号(图1e);余患者未见特异性异常,见表2。
2.4 治疗与预后 8例患者均接受大剂量激素冲击和足量免疫球蛋白治疗,有癫痫发作和精神症状的患者均予以对症治疗。随访mRS评分结果显示,显著缓解4例,部分缓解1例,无反应3例。确诊或怀疑肿瘤的4例患者预后较差,其中3例(例3~5)随访期间死亡。例6患者出院3个月后,遗留记忆力下降。未发现合并肿瘤的4例患者随访期间均显著缓解,预后较好,见表2。
3 讨论
AE中最早发现的是抗NMDAR抗体,之后陆续有其他抗体被发现[4-5]。随着抗体谱系的扩展和确诊患者的不断增多,相对少见的双重抗神经元抗体阳性的现象也越来越受到关注[3]。本研究发现抗神经元细胞内抗原抗体和抗神经元表面抗原抗体两类不同抗体双重阳性及不同抗神经元表面抗原抗体双重阳性的组合方式,这与既往报道基本一致[3,6-7]。前者出现的组合方式较为普遍[3,7],抗神经元细胞内抗原抗体阳性提示AE的副肿瘤属性[1]。文献报道亦发现抗GABABR抗体合并副肿瘤相关抗体阳性最常见[3,7]。本研究发现抗神经元细胞内抗原抗体和抗神经元表面抗原抗体双重抗体阳性组合中,抗神经元表面抗原抗体均为抗GABABR抗体,究其原因,推测可能与恶性肿瘤诱发抗GABABR抗体的产生有关[8-9]。另外亦有抗AMPAR抗体合并抗Hu抗体阳性报道[3],这可能与抗AMPAR抗体相关AE合并SCLC、胸腺瘤等肿瘤有关[8,10]。本研究中出现的双重抗神经元表面抗体阳性的组合方式以抗GABABR抗体合并抗NMDAR抗体阳性及抗LGI1抗体合并抗CASPR2抗体阳性呈现,这在既往研究中亦已有报道[3,6]。一般认为抗NMDAR抗体阳性的男性AE患者合并肿瘤罕见[1],但本研究发现当合并抗GABABR抗体阳性时男性患者有肺癌,可能与GABABR的副肿瘤属性有关[8]。从抗体产生机制而言,本研究例3患者双重抗体阳性可能由病原体感染和肿瘤表达共同参与[11]。本研究中抗LGI1抗体和抗CASPR2抗体双重阳性现象在Morvan综合征患者中并不少见[6],可能与电压门控钾通道(VGKC)复合物为LGI1和 CASPR2共同功能效应器有关[12]。

表2 8例患者其他辅助检查结果、治疗及预后
合并的神经元抗体可导致神经综合征的叠加表现。本研究例4合并了边缘性脑炎和共济失调的表现,可能由抗Yo抗体引起的小脑受累所致[13]。文献亦有报道抗Hu抗体导致抗GABABR抗体阳性边缘性脑炎患者合并感觉性周围神经病表现[3],由此提示合并的副肿瘤相关抗体阳性可叠加副肿瘤相关特异临床表现。另外,不同的抗神经元表面抗原抗体阳性亦可叠加临床表现,LGI1和CASPR2都属于VGKC相关蛋白,LGI1主要分布于中枢神经系统,CASPR2主要分布于周围神经,因此患者中枢神经系统与周围神经系统可同时受累[6]。抗LGI1抗体和抗CASPR2抗体相关AE均可表现为边缘性脑炎,其中抗CASPR2抗体介导的AE周围神经过度兴奋,还可表现为肌强直、肌痛等Morvan综合征的症状[1,7]。本研究中例8患者合并的边缘性脑炎和Morvan综合征表现可予验证,而例7患者未表现周围神经功能障碍,考虑抗CASPR2抗体可能存在变异表现。因此,抗LGI1抗体阳性患者无论是否出现肌肉疼痛、肌肉束颤等周围神经损害,均应注意排除抗CASPR2抗体阳性边缘性脑炎的可能,以免造成误诊或漏诊。
头颅影像学对AE的确诊也具有重要作用[1,10],其MRI多表现为颞叶、海马等边缘系统受累的异常信号改变[1,10,14]。需要注意的是头颅MRI表现无特异异常并不能排除AE可能,且比例不低于MRI表现边缘系统受累的AE[1,15],本研究头颅MRI表现提示该现象在双重抗体阳性的AE患者中亦存在。本研究中例4患者表现为左侧丘脑DWI高信号,而T2WI/FLAIR序列未见明显信号改变,考虑可能与该患者严重癫痫发作有关[16]。AE患者脑电图多表现为弥漫性或多灶分布的慢波节律改变,伴或不伴痫样放电,亦可有δ刷[17-18]对抗NMDAR抗体阳性AE的特异性提示作用,而本研究中3例抗NMDAR抗体阳性的AE患者均未见异常δ刷,可能与合并抗GABABR抗体阳性有关,其发病主导可能为抗GABABR抗体。
抗神经元细胞内抗原抗体相关AE常与肿瘤伴发[1],可合并小细胞性肺癌、乳腺癌、妇科肿瘤及淋巴癌等。该类AE由细胞毒性T细胞介导,而非抗原抗体本身的直接作用,脑组织中有CD8+T细胞浸润,可能会导致进行性不可逆神经元损伤或凋亡[2],因此,对免疫抑制剂治疗的反应较差[8]。本研究8例患者均行激素冲击和免疫球蛋白治疗,4例患者发现合并肺癌,其中例4~6发现合并抗Yo或抗Hu抗体。4例合并肿瘤患者中,2例未行抗肿瘤治疗,均死亡;2例行肿瘤化疗,其中只有1例部分缓解,1例死亡;而4例未合并肿瘤患者免疫调节治疗后得到缓解。提示合并有肿瘤的双抗体阳性AE患者,治疗效果差,若条件允许,需加强肿瘤相关治疗[10]。抗LGI1抗体阳性AE患者合并肿瘤并不多见,但抗CASPR2抗体共同阳性患者合并肿瘤发生率可上升至53.3%[6],需加强肿瘤筛查及处理。
总之,双重抗神经元抗体阳性并存的现象具有一定的指导意义。双重抗神经元抗体阳性AE患者多以边缘性脑炎为主要临床表现,可有周围神经病变、小脑性共济失调等神经元抗体相关临床表现的叠加和变异。双重神经元抗体阳性的患者多合并肿瘤,副肿瘤相关抗体检测阳性可协助明确诊断,合并肿瘤患者预后差。因此,需重视双重抗神经元抗体阳性AE的诊治,加强深入研究。

