CTA和DSA诊断颈动脉狭窄的价值观察
涂 波,潘志华*,刘信东,肖维良,余可斌,刘 嘉
(成都医学院第二附属医院 核工业四一六医院 1.放射科;2.神经内科,四川 成都610051)
颈动脉狭窄系缺血性脑血管病主要高危因素[1],尤其严重颈动脉狭窄患者每年有超过30%可能出现缺血性脑血管病[2]。目前尚未完全明确颈动脉狭窄的确切机制,多认为与高血脂、肥胖、吸烟、高血压等有关[3,4]。早期检出颈动脉狭窄是减少缺血性脑血管发病率及致残率的基础[5]。目前用于颈动脉狭窄筛查的方法包括数字减影血管造影(DSA)、经颅多普勒超声(TCD)、磁共振血管成像(MRA)、CT血管造影(CTA)等,TCD无创、可重复好、经济性高,但对操作者经验要求高,对大脑后循环病变检出率低[6]。MRA适应性广、无创,对血管壁、血凝块及脑组织灌注情况显示好,但检查耗时长,价格昂贵,普及难度大[7]。DSA是目前诊断颈动脉狭窄的金标准,可在确诊动脉狭窄时进行血管内治疗,但存在有创性,技术难度高,且价格昂贵,不适宜作为临床常规筛查项目[8]。CTA则为非创伤性造影技术,时间、空间分辨率高,解剖覆盖广,配合强大的后处理技术,可重建靶血管三维图像,清晰显示血管腔内、腔外及血管壁病变,定量评估病变狭窄程度,明确斑块性质,能全面、准确诊断病变部位,有助于指导颈动脉临床诊治[9]。但对CTA是否可达到与DSA相同的诊断效能尚存在争论。本研究拟对80例行CTA及DSA检查的颈动脉狭窄患者的临床资料展开回顾性分析,探讨CTA对颈动脉狭窄的诊断价值及其与DSA检查的一致性,评估CTA用于颈动脉狭窄诊断的可行性。
1 资料与方法
1.1 临床资料查阅2016年2月-2019年7月我院收治的80例行CTA检查且2周内行DSA的颈动脉狭窄患者的临床资料。入组标准:因心脑血管疾病住院,符合颈动脉狭窄诊断标准[10],存在一侧或双侧颈动脉狭窄;主诉复视、头晕、眩晕、感觉障碍、四肢乏力等;发病48 h内行CTA检查,2周内完成DSA检查;临床及影像学资料完整。排除标准:存在严重出血倾向;哮喘;碘过敏;甲状腺功能亢进;免疫性血管炎;放疗后血管狭窄或主动脉狭窄动脉瘤所致颈动脉狭窄;大动脉炎;心肝肾肺器质性功能障碍;全身恶性肿瘤;心源性脑栓死;血液系统疾病;妊娠或哺乳期女性;临床或影像学资料不全者。其中男49例,女31例;年龄29-84岁,平均(60.61±12.69)岁;病史:高血压62例,糖尿病32例,冠心病47例,高脂血症38例,脑梗死45例;其中有吸烟史41例。
1.2 方法①CTA检查。检查前4 h禁食禁水,安装活动性假牙者检查前取出假牙,提前0.5 h行碘过敏试验,并告知受检者检查按步骤及注意事项,建立静脉通道,肘正中静脉留置套管针,仰卧,肩部自然下垂,采用飞利浦256层Brilliance iCT扫描仪,扫描时叮嘱患者勿移动头部,勿吞咽,平静呼吸,常规定位相确定扫描区域,自主动脉弓扫描至外耳孔,层厚1 mm,管电压100-120 kV,管电流40-60 mA,矩阵512×512,螺距1.2,转速0.27 s,直接行增强CTA检查,肘正中静脉高压注射碘帕醇(国药准字H20053387,上海博莱科信谊药业,18.5 g(I)/50 ml/瓶),剂量为1-1.5 ml/kg,注射速率4-5 ml/s;通过对比示踪软件自动触发扫描,从降主动脉起始处为触发层面,触发阈值120 Hu,注射完毕后应用30 ml生理盐水冲管,延迟15 s后扫描,管电压100 kV,管电流300 mAs,层厚5 mm,进行多平面重建、最大密度投影、容积重组,选定阈值去除软组织、静脉、骨骼,重建强化颈动脉,结合原始轴位图对头颈部动脉斑块分布、形态、性质、钙化、闭塞及狭窄等情况进行观察,测定管腔狭窄程度及斑块性质。②DSA检查。采用西门子Artis Zee Ceiling数字减影血管造影机,经股动脉Seldinger穿刺,高压注射碘海醇(350 mgI/mL),速率15 ml/s,主动脉弓造影剂量20 ml,颈动脉超选择性插管,对比剂剂量6-8 ml,速率4-5 ml/s,行主动脉弓前后位造影,颈总及颈内动脉前后位、斜位及侧位造影。
1.3 颈动脉狭窄程度分级参照北美症状性颈动脉内膜切除术试验协作组标准(NASCET)[11]进行狭窄程度及斑块性质分级。同一血管存在多处狭窄或斑块者选择狭窄最严重部位进行分析,双侧血管同时狭窄则选取严重侧进行分析。狭窄程度=(1-狭窄处直径/狭窄远端正常直径)×100.0%。轻度狭窄:0-50%;中度狭窄:50%-69%;重度狭窄:70%-99%;闭塞:100%。动脉斑块性质:钙化斑块:CT值>130 HU;软斑块:CT值<60 HU;混合斑块:CT值为60-130 HU;易损斑块:斑块形态不规则,表面不平或突入管腔。以上结果均由两名高资历影像科医师进行双盲评估,最终结果取两者均值。
1.4 图像质量评价应用主观评分法[12],4分:造影剂充盈满意,血管显示连续清晰,血管边缘清晰,无运动伪影及边缘脂肪密度影,或移动伪影可通过像素位移纠正,重建图像无阶梯伪影;3分:血管部分节段边缘欠清晰,存在较小伪影及阶梯伪影;2分:血管有伪影,轮廓可见,存在双边征或局部中断错层;1分:血管显示不清,轮廓欠清晰,无法与周围组织鉴别。1分:无法满足诊断;2-4分可满足诊断。
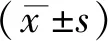
2 结果
2.1 DSA、CTA检查图像质量评分比较80例患者共160条颈动脉,CTA、DSA检查图像评分分级比较差异无统计学意义(Uc=0.661,P=0.507>0.05),见表1。

表1 DSA、CTA检查图像质量评分比较[n(%)]
2.2 DSA、CTA对80例颈动脉狭窄狭窄程度诊断结果比较参照NASCET分级,DSA检出对应CTA检出结果见表2,两者检出一致性Kappa值为0.891有高度一致性。
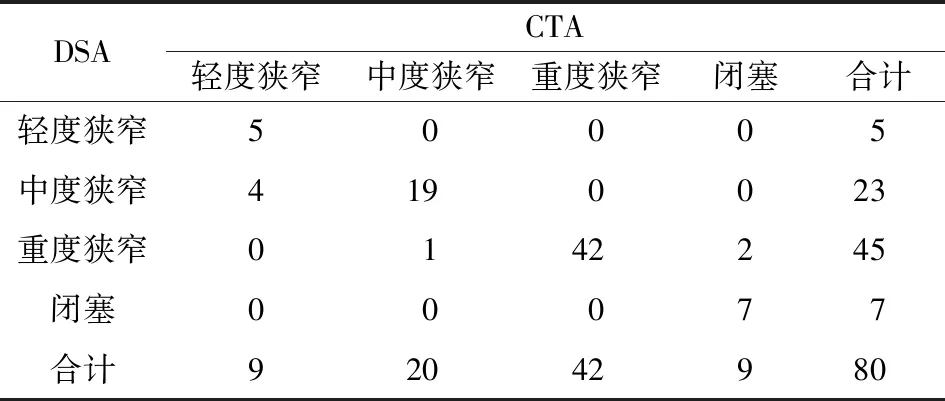
表2 DSA、CTA对80例颈动脉狭窄狭窄程度诊断结果比较(支)
注:CTA与DSA一致性Kappa值为0.891,标准误为0.038,95%CI为0.816-0.965.
2.3 以DSA为金标准CTA检查血管狭窄率为50%、70%效能情况CTA诊断血管狭窄率50% 敏感度为94.67%,特异性为100.00%,准确度为95.00%,与DSA一致性Kappa值为0.689;诊断血管狭窄率70%敏感度为90.38%,特异性为85.71%,准确度为87.65%,与DSA一致性Kappa值为0.755,见表3-表5。
表3 CTA与DSA诊断血管狭窄50%一致性比较
注:Kappa值为0.689,标准误为0.144,95%CI为0.407-0.971.

表4 CTA与DSA诊断血管狭窄70%一致性比较
注:Kappa值为0.755,标准误为0.085,95%CI为0.587-0.985.

表5 CTA诊断血管狭窄50%、70%效能
2.4 CTA与DSA对颈动脉斑块显示情况
CTA可清晰显示斑块大小、数目及性质,80例颈动脉狭窄共发现132处斑块,血管附壁见软斑块20处,呈低密度影,CT值为-20~60 HU;CT显示16处血管壁存在钙化,CT值110-335 HU,大部分为混杂密度;见混合斑块57处,CT值为60-125 HU;易损斑块39处,斑块形态非规则,表面凹凸不平,部分突入管腔;而DSA仅见血管腔狭窄及充盈缺损,无法直接显示附壁血栓密度及形态特点,无法显示管壁钙化灶。
2.5 典型病例分析
见图1,廖某,男,74岁,头-颈部CTA示主动脉、头臂干、右锁骨下动脉、双侧颈总动脉及颈内动脉局部钙化,管腔内见不规则低密度影,左侧总动脉分叉管腔重度狭窄。局麻下行右侧股动脉穿刺,双侧主动脉造影示左侧颈内动脉起始段及末段管壁毛糙,管腔局限性明显狭窄,拟诊急性脑梗塞、左侧颈内动脉起始段重度狭窄,行左侧颈内动脉支架植入术,右侧股动脉穿刺,穿刺成功后置入8F动脉鞘,在8F导引导管内套4F导管,同轴技术将8F指引导管置于左侧颈总动脉远端造影,测量左侧颈内动脉狭窄远端血管直径以及颈总动脉血管直径,计划选择7 mm×40 mm支架,直径5 mm保护伞置于左侧颈内动脉C1段远端,打开保护伞,沿保护伞导丝将5 mm×30 mm球囊送到狭窄部位,扩张狭窄部位,满意后,退球囊,沿保护伞导丝将闭环支架送到狭窄部位,反复调整位置使之覆盖狭窄段然后释放支架。支架释放后造影见狭窄解除,残余狭窄约10%,回收保护伞,内见较硬混合斑块,造影见颅内颅外血管均显示良好,手术过程中的部分血管痉挛解除,推出导引导管。

图1 左侧颈内动脉起始段重度狭窄
a:CT最大密度投影重建示主动脉、头臂干、右锁骨下动脉、双侧颈总动脉及颈内动脉局部钙化,管腔内见不规则低密度影,左侧总动脉分叉管腔重度狭窄;b-d:CTA容积重建示左侧颈内动脉狭窄;e:左侧颈内动脉起始部重度狭窄DSA减影图;f:DSA示左侧颈内动脉起始部重度狭窄,左侧颈内动脉起始段及末段管壁毛糙,管腔局限性明显狭窄;g:支架释放后DSA示狭窄解除;h:DSA示颅内颅外血管均显示良好,支架进一步膨张,残余狭窄约10%。
3 讨论
颈动脉狭窄可引起缺血性低灌注,是造成缺血性脑病的重要原因。已有大量临床证据显示,颈动脉狭窄是造成缺血性脑血管病的独立危险因素[13,14]。统计资料发现,脑梗死中腔隙性梗死约占1/4,其中有超过12%病因为颈动脉病变[15]。而颈动脉狭窄程度则为预估患者是否存在脑卒中风险及评估患者预后的关键标志。NASCET调查发现,颈动脉狭窄超过70%的有症状患者每年脑卒中发生率高达13%,无症状性患者发生率约为2%[16]。谢瑱等[17]进行大样本调查发现,缺血性脑卒中伴颈动脉狭窄病例脑卒中发生率明显高于非颈动脉狭窄者,且随颈动脉狭窄程度上升,卒中发生风险增加。故正确评定颈动脉狭窄患者狭窄程度是指导临床治疗的关键。既往对颈动脉狭窄或闭塞的诊断多依赖于DSA检查,在较长时间段内均作为颈动脉狭窄诊断的金标准,但DSA有创,价格高昂,同时存在一定血管痉挛、穿刺部位血肿、血栓等并发症风险[18]。
CTA作为无创性血管成像技术目前逐渐应用于血管性疾病诊断中,配合三维重组可实现360°旋转,任意角度观察病变血管及血管腔内状况,减少血管重叠干扰,配合后处理技术实现三维重建,清晰显示血管三维解剖空间位置关系,获取精确的诊断信息[19]。国外已有报道证实在颈动脉狭窄筛查中CTA与DSA有较高的一致性[20]。本研究发现,DSA、CTA对颈动脉血管成像质量均较高;以DSA作为金标准,以颈动脉狭窄50%、70%为分界评估CTA诊断效能,发现CTA与DSA一致性达0.689、0.755,表明CTA与DSA诊断颈动脉狭窄有较高的一致性,与朱林[21]结论相同。我们统计发现,以狭窄率50%为分界时,CTA诊断敏感度为94.67%,特异性为100.00%,准确率为95.00%,与Fabian等[22]统计结果接近;以狭窄率70%为分界时,诊断敏感度为90.38%,特异性为85.71%,略低于程锋等[23]统计结论,可能与样本数量造成的统计学偏差有关,但均与DSA呈现较高的一致性,表明CTA对颈动脉狭窄及分级有较高的诊断价值,诊断效能几乎可与DSA媲美,有望作为颈动脉狭窄术前筛查的常规手段。但本组CTA高估5支,低估2支,主要与血管壁内膜钙化有关,当颈动脉血管接近闭塞状态时,血管内血流压力减少,导致远端直径降低,故应用NASCET法可能低估狭窄程度,此时可将球部远端正常血管直径来替代血管远端直径,减少误差。
此外,颈动脉狭窄主要通过斑块脱落或血栓形成而诱发缺血性脑卒中[24]。普遍认为,颈动脉易损斑块是引起卒中的关键原因,但DSA无法评估管壁及斑块内部状态,无法显示钙化斑块,部分钙化斑块在减影片常呈伪影,且造影后导丝、导管通过斑块部位可能导致斑块或栓子脱落,引起脑血管意外[25]。而CTA不仅可清晰显示血管各断面图像,同时可呈现颈动脉管腔情况,通过CT值鉴别斑块性质,测定其厚度及范围,一般斑块内脂质成分含量越高,CT值越低,更易出现溃疡;硬斑块相对稳定,而软性斑块,诸如含出血、细胞碎片或脂质等斑块通常不稳定,更易脱落形成栓塞,需尽快行溶栓治疗或内膜切除术。
总之,CTA成像质量与DSA类似,无创,对颈动脉狭窄程度判定与DSA一致性较高,同时可明确斑块性质,有助于指导临床治疗方案的确定,有望作为颈动脉狭窄术前诊断的依据。后续可考虑通过调整成像参数或技术手段等减少造影剂用量,减少患者受辐射剂量,提高CTA诊断的安全性。

