基于FGF23-Klotho轴探讨肾元颗粒对db/db糖尿病肾病小鼠骨骼的保护作用*
朱国双,王 岚,,邹新蓉,吴文静,,孙 龙,邓丹芳,王小琴**
(1.湖北中医药大学中医临床学院 武汉 430061;2.湖北省中医院 武汉 430061;3.湖北省中医药研究院 武汉 430061)
糖尿病肾病(diabetic kidney disease,DKD)是糖尿病(diabetes mellitus,DM)的主要微血管并发症之一,是导致骨质流失的主要病因之一,也是患者进展为终末期肾脏病(end stage renal disease,ESRD)的首要因素[1]。随着病情的进展,DKD可出现明显的钙磷代谢紊乱,并导致破骨细胞(osteoclast,OC)的活性和相关破骨蛋白表达增加,骨细胞活性降低,新骨形成减少,骨保护素的表达减少,骨质流失增加等一系列骨质代谢紊乱性疾病。因而,预防和治疗DKD患者骨质的流失,是目前亟需解决的问题。
Klotho作为抗衰老基因,主要表达于肾脏中,可与骨分泌的FGF23结合,参与体内的钙磷代谢。前期研究发现[2-4],肾元颗粒可改善链脲佐菌素(STZ)诱导的DKD小鼠的肾功能,增加肾脏Klotho蛋白的表达,减少血FGF23的含量。同时在5∕6肾切除的慢性肾脏病(CKD)大鼠模型中[5],肾元颗粒具有保护骨骼,上调OPG蛋白表达的作用。为进一步探索FGF23-Klotho轴在骨骼中的具体作用机制,本文采用db∕db糖尿病肾病小鼠进行研究,通过观察小鼠骨质流失情况,以及FGF23、Klotho蛋白表达水平,探讨其对骨骼的保护的可能机制。
1 材料与方法
1.1 实验动物
SPF级7周龄db∕db雄鼠30只(许可证号:SCXK(苏)-2015-0001;合格证号:32002100006025),同周龄同窝野生型(wild type,WT)小鼠10只(许可证号:SCXK(苏)-2015-0001;合格证号:32002100006026),购于南京大学-南京生物医药研究院。并饲养于湖北中医药大学SPF级屏障环境动物房。
1.2 材料
肾元颗粒(湖北省中医院院内制剂),购于湖北省中医院,批号:20190906;厄贝沙坦,购于湖北省中医院,赛诺菲(杭州)制药有限公司,批号:8A421。高磷饲料(含磷1.2%、钙1.6%),购自北京博泰宏达生物科技有限公司。试剂:FGF23 ELISA试剂购于Bio-Swamp(货号:MU30742);ALP试剂盒购于南京建成生物工程研究所有限公司(货号:A059-2);钙测试盒购于南京建成生物工程研究所有限公司(货号:C004-2);兔抗小鼠一抗Klotho购于美国sigma公司(货号:SAB3500604);小鼠抗小鼠一抗FGFR1购于英国abcam公司(货号:ab824);兔抗小鼠一抗Osteoprotegerin购于英国abcam公司(货号:ab9986);FITC标记的驴抗兔二抗、Cy3标记的羊抗小鼠二抗购于塞维尔生物技术有限公司(货号:GB21301、GB22403);HRP标记山羊抗小鼠二抗购于塞维尔生物技术有限公司(货号:GB23301)。
1.3 仪器
全自动生化分析仪(深圳雷杜生命科技);TGL-16M型高速冷冻离心机(湖南湘仪离心机设备有限公司);SpectraMax®M2型多功能酶标仪(美国Molecular Devices公司);DYY-5D型电泳仪,Trans-Blot型SD转膜仪,GelDoc XR+型凝胶成像系统(美国Bio-Rad公司);全自动研磨仪(武汉赛维尔生物);石蜡切片机(德国Leica公司);组织包埋机(天津天利航空机电有限公司);激光共聚焦扫描显微镜(德国Leica公司)。
1.4 方法
1.4.1 db/db小鼠糖尿病肾病模型
适应性喂养1周后,对小鼠进行尾静脉采血,测量随机血糖。连续3次随机静脉血糖≥随机静脉16.7 mmol·L-1,尿量大于空白组150%,确定糖尿病造模成功。
1.4.2 动物分组及给药
将30只db∕db小鼠随机分为3组:模型组、肾元颗粒组、厄贝沙坦组,10只WT小鼠作为正常组;肾元颗粒组按6.0 g·kg-1灌胃肾元颗粒配制的药液,厄贝沙坦组按30 mg·kg-1沙坦组-1灌胃厄贝沙坦片配制的药液,3组给药容积均为20 mL·kg-1,各组连续给药12周。
1.4.3 标本采集
腹腔麻醉,行摘眼球取血,取血完成后,置于4,低速冷冻离心机中离心,吸取上清液置于-80℃冰箱中保存。采血完成后,打开小鼠腹腔,摘取小鼠双侧肾脏,小心剔除包膜,将右侧肾脏置于4%多聚甲醛中固定,另一侧立即进行液氮速冻,随即转存于-80℃冰箱中待测。取下小鼠双侧胫骨,将肌肉筋膜剔除干净,右侧放入4%多聚甲醛中固定;另一侧进行液氮速冻,随即转存于-80℃冰箱中待测。
1.4.4 血清FGF23和骨钙盐、ALP活性检测
将冻存的小鼠血清从-80℃冰箱中取出,冰上解冻分装冻存的血清,参照小鼠FGF23试剂盒说明,准备样品和标准品,酶标孔中加入100μL标准品和样品,进行3个复孔,盖上封板膜37℃孵化2 h。小心揭开封板膜,弃去孔内液体,吸水滤纸上拍干。添加100μL生物标记抗体,盖上新的封板膜,37℃孵化1小时。弃去孔内的液体,加入洗涤液200μL,静置2 min并甩干,重复3次后弃去液体。每孔加入显色剂A50μL,再加入显色剂B50μL轻轻震荡混匀,37℃避光显色10 min。每孔加入终止液50μL,终止反应。以空白孔调零,450 nm波长测量每孔的吸光度(OD值)。
将小鼠胫骨从-80℃冰箱中取出,冰上解冻后,进行胫骨组织研磨匀浆,离心取上清液。具体操作参照钙试剂盒。在空白孔中加入10μL去离子水,标准孔中加入1 mmol·L-1钙标准液10μL,测定孔中加入10μL样本液,最后在三者中加入250μL工作液Ⅰ,混匀混匀静置5 min后,波长610 nm测定每孔的OD值。
小鼠胫骨ALP测定,参照ALP测试盒说明书,在空白孔中加入双蒸水5μL,标准孔中加入0.1 mg·mL-1酚标准应用液5μL,测定孔中加入待测样本5μL;同时在空白孔、标准孔、测定孔中依次加入缓冲液50μL和基质液50μL,充分混匀37℃水浴15 min后,在各组中加入显色液150μL,混匀后,波长520 nm,酶标仪测定各孔OD值。
1.4.5 Western blot检测
将小鼠胫骨从-80℃冰箱中取出称重,称取的组织放入液氮预冷的研钵中研磨匀浆,按1∶5的比例加入蛋白裂解液,摇床4℃裂解过夜,4℃12000 r·min-1低温离心30 min,取上清液,考马斯亮蓝法进行蛋白定量,每管蛋白50μg,分装后,-80℃冻存待用。制备分离胶,灌注分离胶,加1 cm的水层,前后震动胶板使胶板水平,室温静置60 min,待分离胶凝固后,配置浓缩胶,去掉水层,灌注浓缩胶,插入梳子,室温静置60 min。待浓缩胶完全固定后,在电泳槽中加入电泳液,将凝胶放入电泳槽中,拿掉梳子。取出样本蛋白和Marker水浴煮沸5 min使蛋白发生变性,样本蛋白上样,电泳电压90 V,待进入分离胶后转为110 V。裁剪PCDF膜5.5 cm×5.5 cm,甲醇充分浸透,海绵垫、滤纸Transfer buffer浸透,取出分离胶,按阴极-海绵-滤纸-分离胶-PVDF膜-滤纸-海绵-阳极顺序排列,放入电转槽中,50 V转模1.5h。取出PVDF膜,TTBS漂洗,按目的蛋白的大小进行裁膜并做好标记,5%脱脂奶粉室温下封闭1 h。配置一抗稀释液,将条带放入一抗稀释液中,4℃冰箱摇床过夜,TTBS清洗10 min三次,二抗室温孵育2 h。TTBS洗膜10 min,滴加A、B发光液(按1∶1比例混合),BIO-RAD凝胶电泳图像分析仪曝光、显影成像,运用Image J进行定量分析。
1.4.6 免疫荧光双标检测
将固定好的肾脏,进行石蜡包埋切片,放入2%双氧水中10 min,室温漂洗10 min,含0.3%Triton X-100室温漂洗破膜,3%双氧水灭活内源性过氧化物酶,血清封闭,分别加入一抗,4,过夜后加入荧光二抗,室温避光孵育1 h,用含有DA磷的封片剂封片,激光共聚焦下观察并拍照。每张切片任选不重复的3个视野,计数双标细胞数,取平均值作为测量值。
1.4.7 统计学方法
采用Graphpad prism 6和SPSS20.0统计学软件进行统计学分析,计量资料以(xˉ±计)表示,采单因素方差分析比较各组之间统计学差异,P<0.05表示两组差异存在统计学意义。
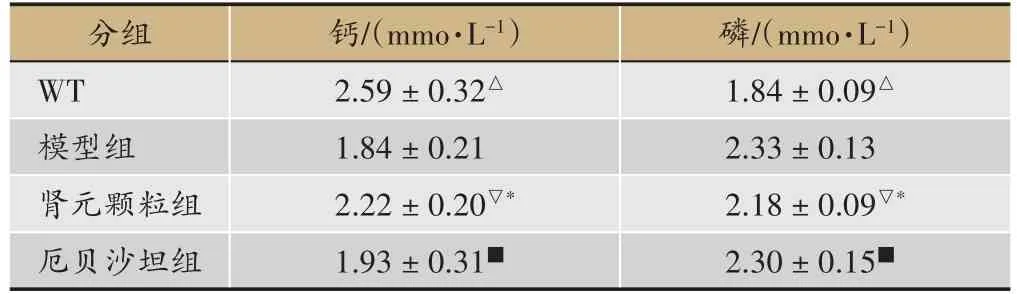
表1 各组小鼠生化指标比较
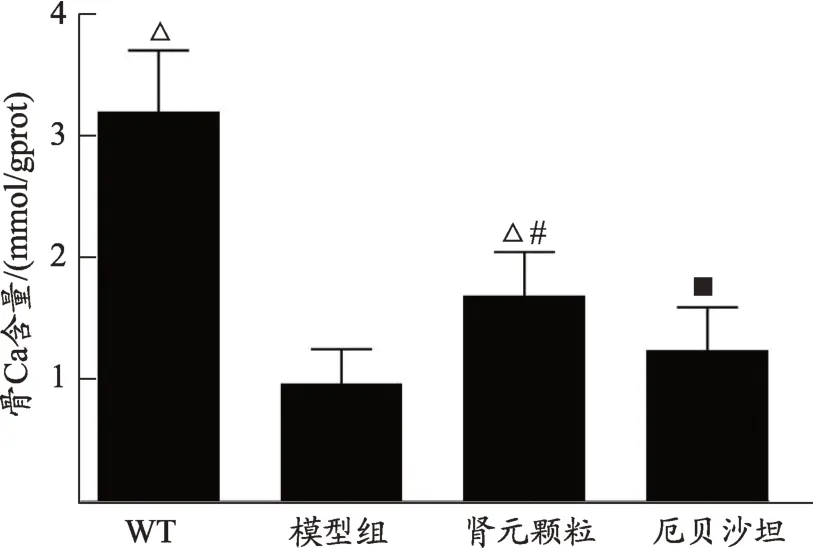
图1 各组小鼠骨钙盐含量
2 结果
2.1 各组小鼠生化指标结果
小鼠生化指标结果(表1):与正常组比,模型组血磷明显升高,血钙降低,且两组差异具有统计学意义(P<0.05),表明db∕db小鼠伴发的肾脏损伤可导致体内的钙磷代谢的紊乱。肾元颗粒组血磷降低、血钙明显升高,与模型组比,差异具有统计学意义(P<0.05),表明通过肾元颗粒干预,小鼠体内钙磷代谢可得到改善。在厄贝沙坦干预组中,小鼠血磷、血钙与模型组比,两组差异无统计学意义(P>0.05),表明厄贝沙坦并不能改善db∕db小鼠钙磷代谢;且肾元颗粒与厄贝沙坦相比,肾元颗粒具有优化钙磷代谢的作用。
2.2 小鼠骨钙盐检测结果
骨钙盐结果提示(图1),模型组骨钙含量低于WT组,与WT组比,差异具有统计学意义(P<0.05),表明db∕db糖尿病肾病小鼠存在骨钙的流失。肾元颗粒组小鼠骨钙流失减少,与模型组比,差异具有统计学意义(P<0.05),表明肾元颗粒具有保护骨钙流失的作用;厄贝沙坦组小鼠骨钙盐流失与模型组比,差异无统计学意义(P>0.05),表明厄贝沙坦对小鼠骨骼钙盐代谢无调节作用;肾元颗粒组与厄贝沙坦组比,两者差异有统计学差异(P=0.014<0.05),表明肾元颗粒对骨钙盐代谢调节作用,优于厄贝沙坦组。
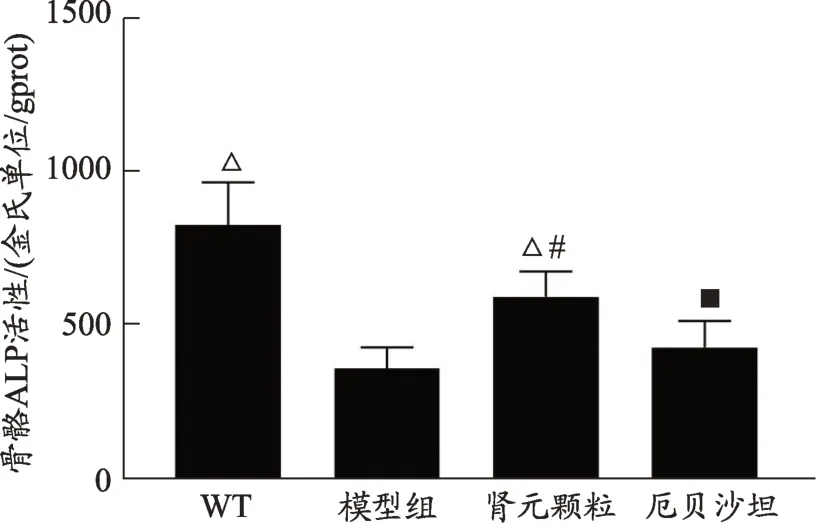
图2 各组小鼠ALP活性检测结果
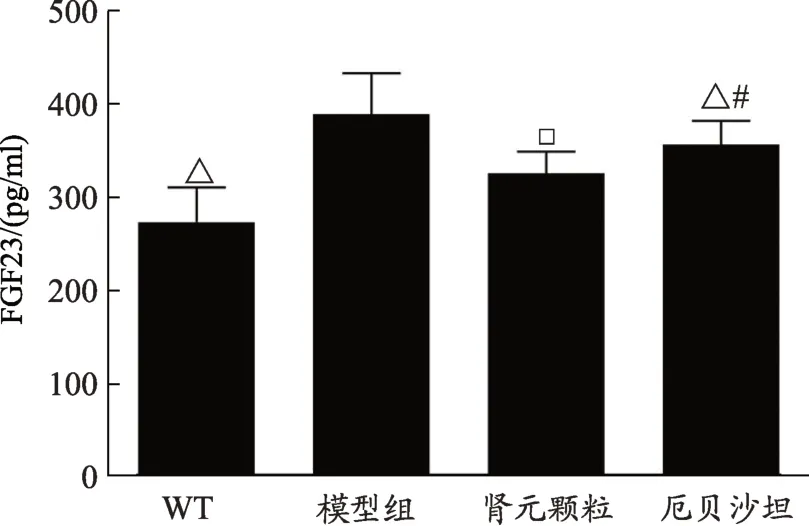
图3 各组小鼠血清FGF23含量结果
2.3 各组小鼠骨骼ALP活性检测
ALP活性结果提示(图2),与WT组比,模型组骨骼ALP活性明显降低,差异存在统计学意义(P<0.05),表明db∕db糖尿病肾病小鼠存在骨骼ALP的活性降低。与模型组比,肾元颗粒可增加骨骼中ALP的活性,两组差异存在统计学意义(P<0.05);而厄贝沙坦组用药后与模型组比,两者差异无统计学意义(P>0.05),这表明厄贝沙坦对于小鼠的ALP活性没有明显的影响;肾元颗粒组与厄贝沙坦组比,两者差异有统计学意义(P<0.05),这表明肾元颗粒增加ALP活性要优于厄贝沙坦。
2.4 各组小鼠血FGF23含量
FGF23含量结果提示(图3),模型组小鼠血FGF23含量明显升高,与WT组比,差异有统计学意义(P<0.05),表明db∕db小鼠伴发的肾脏损伤,可导致体内FGF23的急剧升高;给予肾元颗粒和厄贝沙坦后,两组小鼠血FGF23含量明显减少,与模型组比,差异存在统计学意义(P<0.05),表明肾元颗粒和厄贝沙坦均能有效的降低血FGF23含量;而与厄贝沙坦组比,肾元颗粒组小鼠血FGF23降低程度优于厄贝沙坦组,且两组差异存在统计学意义(P<0.05),表明肾元颗粒在改善db∕db糖尿病肾病小鼠血FGF23含量水平上优于厄贝沙坦。
2.5 各组小鼠骨骼OPG含量结果
各组小鼠OPG结果提示(图4),模型组小鼠骨骼OPG蛋白表达明显降低,与WT组比,差异有统计学意义(P<0.05),这表明db∕db糖尿病肾病小鼠存在OPG表达的丢失;与模型组比,肾元颗粒组小鼠OPG蛋白表达升高,两组差异具有统计学意义(P<0.05),这表明肾元颗粒可增加db∕db小鼠骨骼中骨保护素的表达;模型组与厄贝沙坦组比,两者差异有统计学意义(P<0.05),表明厄贝沙坦能上调OPG蛋白的含量;而肾元颗粒组与厄贝沙坦组比,两者差异具有统计学意义(P<0.05),表明肾元颗粒上调OPG蛋白表达优于厄贝沙坦。
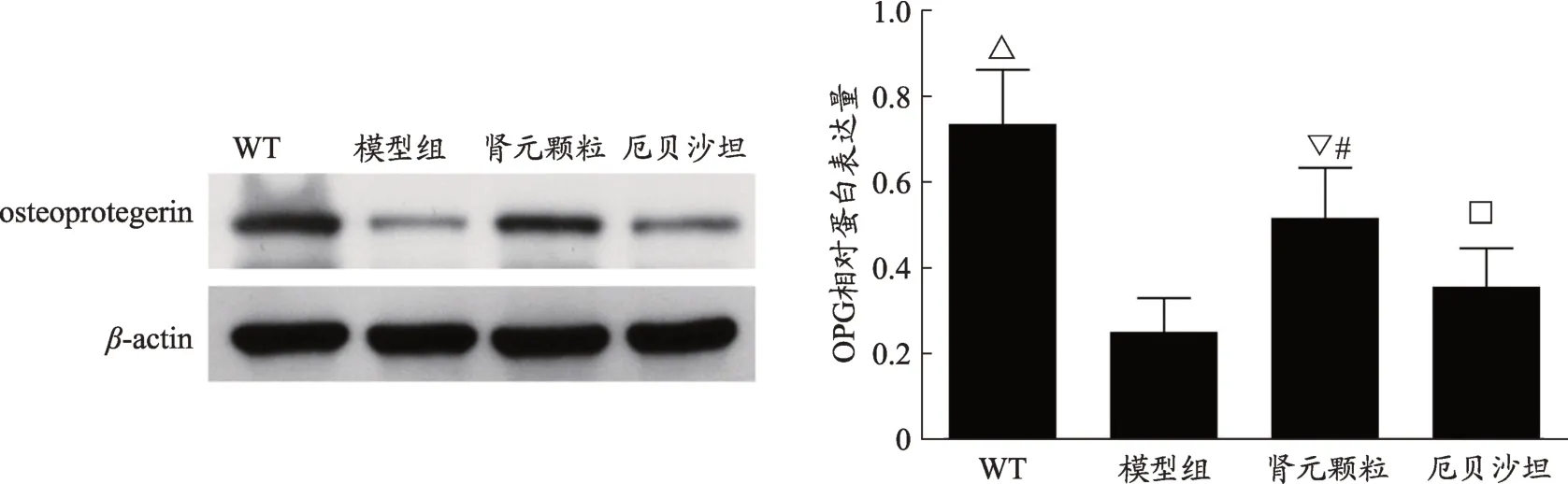
图4 各组小鼠骨骼OPG蛋白含量结果

图5 Klotho和FGFR1免疫荧光激光共聚焦扫描结果
2.6 各组小鼠免疫荧光激光共聚焦扫描结果
免疫荧光双标结果显示,WT组小鼠可观察到完整的肾单位,Klotho集中表达于肾小管上皮细胞中,且分布均匀;模型组肾单位破损最为严重,Klotho表达较少;肾元颗粒组肾单位破损最轻,Klotho表达较多;厄贝沙坦组次之(图5)。
在对阳性细胞表达数的结果中发现,WT组阳性细胞表达数最多,其与模型组比,差异具有统计学意义(P<0.05);与模型组比,肾元颗粒组和厄贝沙坦组阳性细胞表达数均有显著的增加,且差异存在统计学意义(P<0.05);与厄贝沙坦组比,肾元颗粒组小鼠肾脏阳性细胞表达数优于厄贝沙坦组,且差异存在统计学意义(P<0.05)。
3 讨论
db∕db小鼠属于自发性2型糖尿病模型,该小鼠模型属于4号染色体的瘦素受体(Leptin receptor)基因发生突变所致,下丘脑对饱感物质(瘦素)缺乏反应,不能产生饱感,进食增多,体内合成代谢明显大于分解代谢,引起脂肪的堆积而肥胖,而随着病情的进展,出现不同程度的肾脏损伤,诱发DKD[6]。
DKD属于中医“消渴病”范畴;消渴日久,肾体受损,伤阴耗气,气阴两虚,气虚血运无力,出现瘀血、痰浊、热毒等病理产物的产生。肾体受损,肾精不足,骨髓生化乏源,骨骼失去充养,导致骨质的流失。肾元颗粒(原名:肾安颗粒)是根据邵招娣教授多年致力于DKD治疗和研究的新药[7]。以补肾健脾,通腑泄浊为治疗原则,配伍黄芪、淫羊藿和大黄组成肾元颗粒。肾元颗粒方中以黄芪为君,取其补气升阳、托毒生肌、利水除湿之功;淫羊藿为臣,取其温肾健脾、强筋壮骨之效;加之酒制大黄为佐使,化瘀解毒、通腑泄浊。三药合用,可达标本兼治之功。
FGF23-Klotho轴是调控钙磷代谢的主要激素,协同调控血钙磷吸收、尿钙磷重吸收与排泄、骨钙磷沉积与释放,共同维持机体内的钙磷代谢平衡。Klotho主要表达于肾小管上皮细胞中,具有抗炎、抗氧化应激、抗细胞凋亡、抗纤维化、抗肿瘤等多种生物学效应[8-9]。在肾远端小管,Klotho蛋白可与FGFR1相结合,形成Klotho∕FGFR1复合受体[10-11],并特异性的与FGF23结合,增加FGF23与FGFR1之间的亲和力,形成FGF23∕FGFR1∕Klotho三元复合物,激活早期生长反应因子1(Egr1),抑制1,羟化酶活性表达,增加24-羟化酶活性的表达,减少活性维生素D的合成,使其降解增加,减少磷在小肠中的重吸收[12-13]。在近端小管,FGF23-Klotho轴的激活可抑制肾小管上皮细胞中钠磷协同转运子2a(NaPi2a)和钠磷协同转运自2c(NaPi2c)表达的,减少肾小管对磷的重吸收,增加尿磷的排泄[14-17],调节体内钙磷代谢的平衡。
钙、磷为骨矿物质盐的主要成分,参与和调节骨硬度的构成。体内99%的钙以羟磷灰石结晶的方式储存于骨组织中,剩余1%钙存储于体液和软组织中。而体内的磷,86%以磷酸钙形式存储于骨组织中,剩余14%磷则存储于细胞中。可见,骨组织是钙磷储存的重要场所,是维持体内钙磷平衡的重要器官[18]。通过检测骨骼和血清中钙磷的含量,可从直接的角度和间接的角度反应骨质流失的情况。
骨组织骨量及内在的生物力学性能等指标是骨性能判定的重要指标[19]。骨量的减少以及骨质内部结构的改变均能影响骨生物力学,可降低生物力学强度。现代药理学研究表明,OPG作为肿瘤坏死因子受体(tumor necrosis factor receptor,TNFR)超家族成员,其在骨质流失过程发生中有重要意义[20]。OPG与其配体OPGL结合后,可抑制破骨细胞前体细胞分化和诱导破骨细胞生成的关键因子表达,抑制成熟破骨细胞的活性。
此次实验发现,肾元颗粒可明显降低血清中异常升高的FGF23含量,并能明显增加肾脏中Klotho和FGFR1阳性细胞数的表达,使得体内FGF23-Klotho轴得到恢复。随着该轴功能得到恢复,db∕db小鼠体内的钙磷代谢也得到明显改善。通过血磷和血钙水平的观察发现,肾元颗粒能明显降低血磷,增加血钙含量,改善体内钙磷代谢。而这一作用也间接反应肾元颗粒对骨骼的保护作用。为进一步观察肾元颗粒对骨骼的保护作用,此次实验通过检测骨组织中ALP活性、骨钙盐含量以及OPG蛋白的表达情况,直接观察骨组织中成骨细胞的活动和骨骼骨量、骨质流失的情况[21-22]。此次实验结果发现,肾元颗粒可增加骨组织中骨钙盐的含量,上调骨组织中ALP的活性,增加骨骼中OPG蛋白的表达,这表明肾元颗粒具有抑制骨质流失,增加成骨细胞活动,最终达到骨骼保护作用。
综上所述,FGF23-Klotho轴交通着肾脏与骨骼,并将两者联系在一起,这与中医“骨肾同源”理论相合。肾藏精为肾脏的基本生理功能,其所藏之精可充养骨髓,与骨同出一源。通过对FGF23-Klotho轴的研究,有助于从分子生物学角度理解“骨肾同源”的中医基础理论,同时也为揭示中医“肾-精-髓-骨”关联理论的科学内涵和价值提供了有力的证据支持,为DKD的治疗提供新的思路。

