磁共振肠道水成像在机械性肠梗阻中的诊断价值
1.云南省昆明医科大学第二附属医院放射科 (云南 昆明 650101)
2.云南省临沧市第二人民医院放射科 (云南 临沧 677000)
杨冯棱1 郭 立1 杨文秀2
肠梗阻是常见的急腹症。是否存在肠梗阻、肠梗阻部位、病因及是否存在血运障碍对肠梗阻的诊治具有重要的价值。肠道(Magnatic Resonance,MR)水成像是利用重T2加权成像上肠道内的液体呈高信号而使肠腔显像的一种成像技术,在肠梗阻扩张积液时具有常规X线检查和CT检查所不具备的优点。本研究回顾性观察、分析51例临床怀疑肠梗阻的MR表现,探讨MR对肠梗阻的诊断价值。
1 资料与方法
1.1 一般资料 2014年1月~2017年6月临床怀疑肠梗阻到我院进行诊治且行MR检查的51例患者,其中男30例,女21例;年龄20~81岁,平均56.8岁。患者就诊时出现不同程度的腹痛、腹胀、呕吐及肛门停止排气、排便4~9d。51例中有39例于MR检查后12~36小时内行手术(均存在肠梗阻);12例未行手术、但通过临床随访和多种影像检查(消化道钡餐、CT)证实有无肠梗阻(8例存在肠梗阻,4例排外肠梗阻)。
1.2 检查方法 采用Siemens公司Sonata 1.5T超导型MR及体部线圈进行检查。扫描范围自剑突至耻骨联合。所有病例先行常规T1WI、T2WI扫描,再行肠道水成像检查。水成像序列包括:①厚块2D水成像:采用快速自旋回波(TSE)序列进行冠状面及斜冠状面扫描,层厚80 mm;②薄层2D水成像:采用半傅立叶采集单次激发快速自旋回波(half fourier acquisition single shot turbo spin echo,HASTE)序列和真实稳态进动快速成像(true fast imaging with steady state precession,True-FISP)序列进行冠状面、横轴面扫描,扫描层厚2~4mm。
1.3 评价方法 由2名具有5年以上影像工作经验的医师对51例患者的MR图像进行回顾分析,对病变的部位、引起的原因、有无绞窄进行判别(如有意见不符,经协商后达成一致性意见),具体判别标准如下:①是否存有梗阻的判别:梗阻者扫描野内小肠、结肠存在明显扩张(小肠扩张标准>3cm,结肠扩张标准>5cm)且肠管内见积液或积气,见图1~8。②梗阻的部位的判别:在近侧扩张肠管与远端正常或塌陷肠管之间出现“移行带”,“移行带”所在区域为梗阻部位。小肠和结肠梗阻的判别主要是根据病变肠管所处位置和肠管形态(于横断和冠状位定位,结肠位于腹部的周围区域且可见结肠袋显示,小肠位于腹部中心区域且可见小肠的粘膜);空回肠梗阻的判别主要通过肠粘膜的形态、未扩张肠管的位置、长度及其所占小肠全长的比例来进行推断。③引起梗阻原因的判别:肠粘连为“移行带”区见粘连带、肠管成角、肠管鸟嘴状改变、无明确病变者,见图1;肿瘤性梗阻为“移行带”见软组织肿块或局部肠管壁增厚,见图2~3;肠套叠为“移行带”区可见同心圆状结构或彗星尾征,见图6;胆石或粪石性肠梗阻,肠管内可见结石影,见图7;内、外疝为“移行带”区附近见疝囊及疝内容物显示,见图8;肠扭转为“移行带”周围肠袢伴肠系膜血管的走行、分布异常,见图9。④有无缺血的判别:假肿瘤征;肠壁增厚、水肿,肠壁厚度>2 mm;局限性的肠系膜液性渗出、水肿;肠壁或门静脉系见积气;腹腔血性积液或病变周围积液,见图1。
2 结 果
2.1 MR水成像在有无机械性梗阻中的判定 51例患者中有48例均表现为肠管不同程度扩张,[扩张小肠直径为(3.5±0.4)cm,扩张结肠直径为(5.8±0.3)cm],扩张肠管内见积气、积液及液气平面,见图1~8。3例未见扩张肠管的存在(均于MR水成像检查前行胃肠道减压治疗)。51例中47例存有机械性肠梗阻,4例为一过性肠管扩张,积气、积液,通过肠管扩张来判别诊断的准确率为91.48%(43/47)。
2.2 MR水成像对梗阻部位的判定 在经外科手术证实且MR水成像中显示有梗阻的39例患者中,33例(84.6%)定位准确,6例(15.4%)无法定位或定位不准。6例中有5例(4例肠粘连者和1例闭孔疝者)无法通过MR水成像对梗阻部位作出定位,另有1例定位不准(MRI定位梗阻平面位于回肠,手术证实梗阻平面位于空肠)。
2.3 MR水成像对梗阻原因的判别 39例手术证实的肠梗阻中肠粘连18例、小肠肿瘤4例(其中1例肿瘤侵犯邻近肠管,致邻近肠管移位变形者,误诊为肠扭转,见图4-5)、结肠肿瘤7例、肠套叠并结肠脂肪瘤2例(1例仅诊断肠套叠漏诊脂肪瘤)、胆石性肠梗阻1例、腹内或腹外疝3例(其中1例闭孔疝误诊为肠粘连)、肠扭转4例。手术结果对照准确率为92.3%。
2.4 MR水成像对肠管血运障碍的判别 39例手术证实的肠梗阻中手术证实伴有血运障碍14例,25例无血运异常。MR误诊4例,漏诊5例,其诊断的准确率为76.9%。
3 讨 论
腹部立卧位平片是诊断肠梗阻的最常用的方法。但腹部平片获取的是二维投影图像,有时难对梗阻的部位、病因及有无血运的障碍做出较为明确的诊断,不利于肠梗阻及时的诊治以致延误病情,甚至会危及患者的生 命[1-2]。MR肠道水成像是利用重T2WI上液体呈高信号的原理来对肠腔内大量积聚的液体进行成像的,具有常规X线检查和CT检查所不具备的优点(无电离辐射、多参数、多角度成像),有助于机械性肠梗阻病例的发现及病因的诊断。故本研究通过回顾性观察51例临床怀疑肠梗阻病例的MR,探讨MR肠道水成像在判别有无肠梗阻、肠梗阻的部位、病因及是否伴有血运障碍方面的价值。
3.1 MRI水成像在判别有无梗阻上的价值 47例有肠梗阻的患者中,有43例MR水成像显示有肠梗阻的存在,其诊断的准确率为91.48%。肠梗阻病例中有3例患者因行胃肠减压治疗后才行MR水成像检查,此时由于胃肠道内的积液量明显减少、肠管扩张不明显,病变上下游及病变肠管的形态、信号缺乏明显的差别,故无法判断有无梗阻的存在,更难于进一步确定梗阻部位及梗阻的病因。因此,今后对于临床上如怀疑肠梗阻且需行MR水成像检查的患者,应在胃肠减压治疗前进行MR水成像检查。
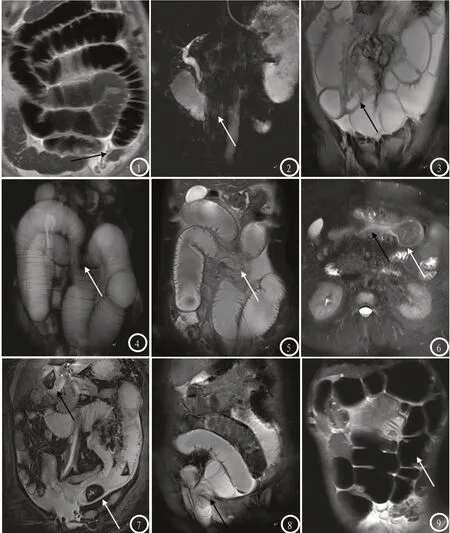
图1 男,57岁,肠粘连所致绞窄性肠梗阻,薄层2D水成像(HASTE序列) 病变肠管见“鸟嘴样”变窄(黑色箭头),其周可见较多液体聚集,病变上游肠管扩张、积气积液。图2 男,50岁,十二指肠水平段腺癌所致肠梗阻,厚块2D水成像(TSE序列) 十二指肠水平段呈截断改变(白色箭头),其上游十二指肠和胃扩张、潴留。图3 女,49岁,回肠末端腺癌所致肠梗阻,薄层2D水成像(True-FISP序列) 病变肠管管壁局限性增厚(黑色箭头),空肠和回肠扩张、积气积液,肠系膜区可见多发肿大淋巴结。图4 男,51岁,小肠腺癌并周围组织侵犯。图4A 厚块2D水成像(TSE序列),小肠肠管扭曲改变(白色箭头),邻近的小肠肠管扩张积液。图5 薄层2D水成像(HASTE序列),病变小肠及系膜结构不清,呈团状软组织影(白色箭头)。图6 男,53岁,结肠脂肪瘤、肠套叠所致肠梗阻,薄层2D水成像(HASTE序列) 横结肠肠腔内见一团块状低信号影(白色箭头),近端肠管呈肠套叠征象(黑色箭头)。图7 女,49岁,薄层2D水成像(True-FISP序列)胆石性肠梗阻。胆囊(黑色箭头)、回肠(白色箭头)内可见多发结石影,结石上游肠管扩张、积气积液。图8 男,54岁,薄层2D水成像(True-FISP序列),腹股沟疝 回肠经深环疝入腹股沟管(黑色箭头),上游肠管梗阻扩张。图9 66岁,女,乙状结肠扭转并闭袢性肠梗阻,薄层2D水成像(HASTE序列) 扩张、积液的肠管呈“C”形改变(白色箭头),。
3.2 MRI水成像在梗阻部位判别上的价值 本组经手术证实的39例中定位准确者有33例,5例则因移行带小或隐蔽而无法作出定位,1例为定位不准,MRI水成像在判别梗阻部位上具有较高的准确性(84.6%)。我们定位的经验是:首先,仔细观察肠管的形态,根据近端扩张的肠管与远端塌陷或正常肠管之间移行带来判断梗阻部位。可先观察有无结肠扩张来判断是小肠梗阻还是结肠梗阻。判断小肠和结肠扩张可根据下面方法区分:①两者分布有一定的空间特征:结肠多位于四周,并且升、降结肠多位于腹膜后,走形平直,位置较为固定;小肠位于腹腔内,梗阻扩张时的肠袢多布满全腹。②扩张小肠和结肠形态上也有一定特征:空回肠扩张管径稍小,可见环形皱襞;扩张的结肠管径较大,可见结肠袋和半月皱襞。在部分完全性小肠梗阻病例中,小肠肠管极度扩张,直径与扩张的结肠管径相似,加之结肠塌陷显示欠佳,时常会将扩张的小肠误认为是扩张结肠而引起梗阻定位的错误。但只要结合多方位图像(横断、冠状、矢状)图像进行定位,并根据能清楚显示出的较长一段肠袢的形态和走形加以辨别,一般判别两者并不困难。此外,因结肠(升结肠、降结肠、直肠)和十二指肠解剖位置相对固定,易于寻找及识别。故在寻找小肠梗阻部位时,可先找到回盲部后向近端查找或从十二指肠向远端查找,这种方法在一定程度上助于查找病变。判断梗阻部位到底是位于空肠还是回肠,则主要根据正常或塌陷的小肠肠管的长度和及其所处的位置来判断。值得注意的是,在一些不完全性肠梗阻的患者中,梗阻两端肠管管径差别不大,我们的经验是应仔细排查肠管的管腔、管壁及周围组织的情况(如局限性的积液等),判断是否为梗阻带。
从MRI水成像技术来看,厚块水成像有利于给观察者一个整体观,初步判别梗阻的部位,但薄层水成像才更利于病变细节的显示和梗阻部位的判断。
3.3 MRI水成像在梗阻原因判别上的价值 引起机械性肠梗阻的原因众多,其中肠粘连为主要原因[1],其次为肠道肿瘤,其它原因包括肠套叠、肠扭转、腹部内外疝等[3-5]。因病因的不同,其在MR水成像上的表现也各具特征。
(1)肠粘连:在MR水成像上,多数病例表现为粘连部肠管牵拉成角、呈鸟嘴状狭窄,肠管移行段肠腔变细而无肿块、炎症等征象,少数病例可见粘连带显示。在诊断此类病变时,我们的经验是“移行带”及其邻近区域未见确切病变者,应高度怀疑肠粘连的存在。因肠粘连多见于曾有手术、腹部感染等病史的患者[1],故询问其病史将有助于本病的诊断。
(2)肠道肿瘤:恶性生长的肿瘤可累及肠壁,引起移行带区肠壁局限性不规则增厚、肠腔狭窄,有时可伴软组织肿块形成,一般不难诊断。部分病例的病变于肠道水成像上的形态和信号与肠内容物相似而不易区分,此时如结合常规MR平扫、增强及弥散扫描可提供病灶的检出率[6]。此外,如肿瘤侵犯周围组织,可使周围组织结构不清,此时需仔细辨识。本组中有1例小肠癌侵犯了邻近肠管及系膜,致使邻近肠管移位、变形,而误诊为肠扭转。
(3)肠套叠:MR水成像上虽不易显示肠套叠时套入部的肠系膜脂肪,但可清楚显示肠套叠时的三层肠壁(最外为鞘部肠壁,第二层为套入部折叠肠壁,内层为套入肠壁及内容物)所呈的“同心圆样”改变。在发现肠套叠时,应仔细观察套叠周围的肠管情况,观察有无引起肠套叠明确的病因,如是否合并肿瘤性病变。本组病例中有2例横结肠脂肪瘤所致肠套叠者,其中1例病变稍小且受MR水成像的限制(重T2成像+脂肪抑制),病变显示欠佳而漏诊脂肪瘤的存在,该病变通过进一步回顾图像得以发现。
(4)胆石性肠梗阻:本组中的1例胆石性肠梗阻,其MR水成像上不仅能清楚显示胆石性肠梗阻,还可清楚显示出胆囊-十二指肠的瘘道及胆道内的积气的聚集。如能发现上述特征性的征象,一般诊断不难。
(5)腹内、外疝:MR水成像可更清楚地显示疝的全貌(疝环、疝囊及疝内容物),及其与肠管之间的关系,通常诊断也不困难。本组病例中有1例闭孔疝者因疝囊较小而显示不清,仅于盆部左份见鸟嘴样狭窄的小肠肠管,再结合其有腹部手术的病史,而误诊为肠管粘连。所以,在一些特殊部位发生的肠梗阻,虽未见确切疝囊,也应想到腹内外疝的可能,并根据解剖结构进行多方位薄层扫描加以明确。
(6)肠扭转:肠扭转可分为小肠扭转和结肠扭转。其中小肠扭转是某段小肠沿其系膜长轴发生旋转移位,呈螺旋形改变,其在True-FISP压脂序列(系膜血管呈高亮信号)显示较佳,有助于病变的诊断。本组病例中有1例小肠癌侵犯邻近肠管及系膜,致邻近肠管移位变形者而误诊为肠扭转。故观察到移位扭曲肠管时,还需对移形区肠管仔细观察,排外肿瘤的存在。另结肠的扭转多见于乙状结肠段[7],本组病例中4例均为乙状结肠扭转。
3.4 有无血运的障碍 绞窄性肠梗阻(即伴有肠壁血运障碍的肠梗阻)常为肠系膜血管受压、血栓形成或栓塞等因素所致。本组手术证实的病例中,MR诊断有无血运的障碍的准确率为76.9%,低于相关文献的报道[8]。这不仅与本组收集病例的病因、种类不同有关,还与影像判别是否存有缺血的标准不同有关(本组是通过肠管管壁的厚度等间接征象进行判别,而非通过血管内的血栓、肠管壁强化程度的减弱等直接征象进行判别)。故在判断肠梗阻有无血运障碍时,肠道MR水成像的作用有限。故必要时应结合MR增强扫描等其他相关检查。
3.5 本研究中的不足 本组病例收集的是临床怀疑为机械性肠梗阻的患者,未对其他类型的肠梗阻(血运性肠梗阻及动力性肠梗阻)的研究。其次,虽然本组中76.5%的肠梗阻病例经过了手术证实,但仍有23.5%的病例仅通过临床或其他影像学方法加以证实,这可能在会影响判别有无梗阻的准确性。此外,本组病例多为临床或其他影像学检查怀疑肠梗阻的病人,故使研究结果在判别有无肠梗阻的准确性方面会高于实际。但本研究最主要目的不是观察肠道MR水成像能否诊断肠梗阻,而是观察该技术在判断肠梗阻发生部位、原因及有无血运障碍方面的能力。
综上所述,MR肠道水成像能直观、准确和全面地显示肠梗阻的存在、梗阻的部位及梗阻原因,并能对有无血运障碍做出一定的判断,有助于肠梗阻的诊治。

