ERAS围术期护理在斜外侧椎间融合术治疗腰椎滑脱症中的效果观察
李盼 黄洁
腰椎滑脱症作为临床较为常见的腰部疾患,多见于中老年人,以退变性和峡部裂性为主。退变性滑脱主要因椎间盘退变、韧带松弛所致,峡部裂性滑脱主要因外伤、积累性老损所致。根据Chan等[1]报道,腰椎滑脱症是引起腰痛的常见原因,其发病率约11.5%,通常经保守治疗无效或症状严重者需采取手术治疗。而传统的开放性手术存在创伤大、出血多、医源性并发症较多的问题,往往无法被老年患者接受。因此,微创脊柱手术为脊柱外科医生常规治疗方法,主要术式有经后路椎体间融合术(PLIF)、经椎间孔椎体间融合术(TLIF)、极外侧椎间融合术(XLIF)以及斜外侧椎间隔合术(OLIF)[2]。OLIF是近年来开展的新型微创椎间融合技术,适用于各种腰椎退行性疾病。然而有研究显示,高龄和合并多种慢性疾病是影响腰椎融合术围术期并发症发生的独立危险因素[3],对患者术后康复造成严重影响。加速康复外科(ERAS)理念,目前广泛在各大医院外科推广应用,其目的在于通过实施一系列经循证医学证实的围手术期优化措施,以最大限度地减少患者并发症的发生,减轻手术创伤应激,促进其术后尽快恢复[4]。因此,本研究将ERAS围术期护理干预应用于接受OLIF治疗的70例腰椎滑脱症患者中,取得了显著的效果,报道如下。
1 资料与方法
1.1 一般资料 采用目的抽样法,将2017年3月至2018年1月本院脊柱外科接受OLIF治疗的68例腰椎滑脱症患者作为对照组,2018年2月至2019年5月收治的70例腰椎滑脱症患者作为观察组。2组患者基线资料比较差异无统计学意义(P>0.05)。本研究符合《赫尔辛基宣言》要求。见表1。
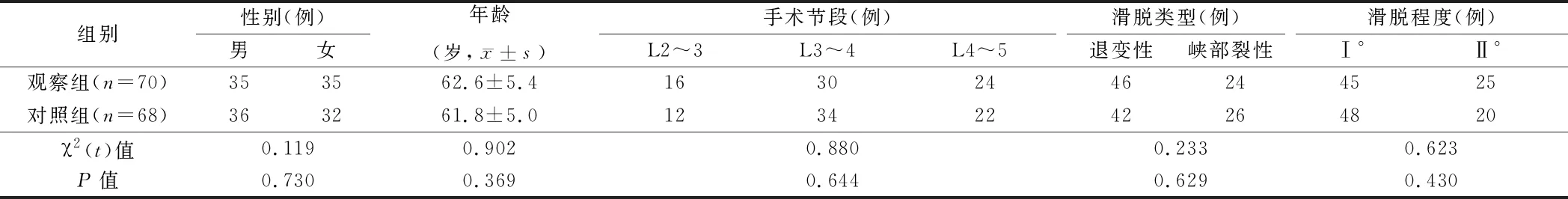
表1 2组基线资料比较
1.2 纳入与排除标准
1.2.1 纳入标准[5]:①年龄≥60岁;②经影像学诊断为腰椎滑脱症,滑脱程度≤Ⅱ°;③临床表现为腰痛或腰腿痛等临床症状,伴或不伴间歇性跛行;④均为首次发病或原发性疾病;⑤保守治疗至少3个月无效,具备OLIF手术指征;⑥对本研究知情同意并签署同意书,能够配合临床资料的采集。
1.2.2 排除标准[6]:①合并严重心、肺、脑等疾病无法耐受手术者;合并多种脊柱疾病;②手术部位感染或有腰椎手术史;③伴有严重的神经功能损伤。
1.3 护理方法
1.3.1 对照组:患者实施常规围术期护理干预:①待患者入院后,护理人员实施护理评估及入院宣教;②完善常规术前检查,做好病房卫生清洁工作,注意通风换气,指导体位训练及床上便器使用方法;③完善术前准备工作,给予积极的心理辅导和术前宣教,告知患者手术相关注意事项;④术前皮肤准备,告知禁食8 h、禁饮6 h,若患者疼痛剧烈可按照医嘱给予依托考昔超前镇痛;⑤患者术后去枕平卧,完全清醒后垫上枕头,4 h后给予少量水及流质食物,实施术后宣教,包括病情观察、管路护理、康复锻炼等。⑥若疼痛剧烈可按医嘱给予静脉镇痛泵或依托考昔,并指导患者进行常规四肢关节屈伸运动。
1.3.2 观察组:患者在对照组基础上实施ERAS围术期护理干预,具体如下。
1.3.2.1 术前宣教:护士可采取多种形式向患者讲解ERAS流程、措施及住院相关注意事项,也可请医师协助改善患者焦虑心理及睡眠状况。
1.3.2.2 术前准备:①肠道准备:采用无渣均衡饮食代替常规机械肠道准备,必要时给予灌肠剂协助排便;禁食时间缩短为术前6 h,全身麻醉诱导前2 h静脉注射10%葡萄糖溶液500~1 000 ml,或温服10%葡萄糖溶液500 ml,糖尿病患者可用平衡液代替。②营养支持:采用营养风险筛查(NRS)2002评分简表评估患者的术前营养风险,总评分≥3分表示存在营养风险,需请营养科医生提供营养支持[7]。③超前镇痛:入院时评估患者是否采取依托考昔镇痛,可于术前1 d给予氟比洛芬酯注射液超前镇痛。④皮肤准备:入院后每日定时采用肥皂水清洁手术部位皮肤。⑤留置尿管:将常规术前病房留置尿管改为硬膜外麻醉后留置尿管,以减轻不良刺激及应激反应。
1.3.2.3 术中措施:①术中保暖:手术室应保持温度在22~25℃,湿度在50%~60%,采用测温导尿管检测患者体温,术中使用保温毯或加热输液装置,注意保暖,维持体温≥36℃,以预防低体温现象的发生。②麻醉方法:用异丙酚和氯胺酮深度镇静,手术结束前予以0.25%布比卡因行伤口局部麻醉。③舒适体位:患者在全身麻醉或硬膜外麻醉后采取俯卧位,腹部悬空,于C臂X线机透视下进行手术。
1.3.2.4 术后干预:①术后镇痛:采用多模式镇痛,患者在自控止痛的基础上,术后3 d内静脉滴注氟比洛芬酯注射液,50 mg/次,2次/d。术后第4天改用口服依托考昔镇痛,剂量及用法严格遵医嘱,并严密观察患者病情变化。②术后进食及营养支持:待患者术后完全清醒后,护理人员需详细评估其吞咽情况、腹部情况及伤口引流情况,若无异常者可给予温开水50 ml,每隔10 min 1次。若无呛咳、误咽情况可开始进食流质或半流质食物,恢复肠蠕动后可正常饮食,若存在营养风险需提供营养支持。③术后保暖:术后返回病房采用厚棉被,必要时加盖毛毯。④液体管理:患者在进食后应尽快减少静脉液体量。⑤术后早期活动及康复锻炼:待患者完全清醒后协助其垫上枕头,每10分钟观察患者反应,协助进行踝泵运动、双上肢屈伸运动及深呼吸运动,手术当日根据患者耐受力决定锻炼时间。术后第1天卧床期间,按脊柱外科卧床患者康复操的流程指导康复锻炼,2次/d,每次时间因人而异;术后早期训练中若体虚可给予能量补充,若切口疼痛则按照医嘱给予非甾体类抗炎药治疗。术后第1天下地活动前,评估患者的肌力情况及神经根是否水肿,结合术后腰椎X线片结果决定是否下床活动,若双下肢无反射痛则协助患者佩戴腰部支具坐于床边,若无晕厥情况则协助其站立于床旁并加以保护。术后第2天视患者情况增加其活动量,可在助行器的保护下尝试行走,以量力而行、循序渐进为训练原则[8]。
1.4 观察指标及评价标准 比较2组患者术后2周内并发症发生情况,术后24、48、72 h的VAS评分,术前及术后1、3个月ODI、JOA评分。(1)VAS总分0~10分,0分表示无痛,10分表示难以忍受的剧痛。(2)ODI总分0~50分,分数越高表明患者功能障碍越严重。(3)JOA总分0~29分,分数越高表明功能障碍越轻微[9]。(4)于术后3个月随访时按照改良MacNab标准评定患者的腰椎功能恢复情况,①优:临床症状完全消失,患者的腰椎恢复至原来的功能;②良:偶尔疼痛,能从事较为轻松的工作;③可:临床症状减轻但仍伴有疼痛感;④差:伴有神经根受压表现,需再次实施手术治疗[6]。

2 结果
2.1 2组术后VAS评分比较 术后24、48 h,观察组患者VAS评分均显著低于对照组(P<0.05);但2组术后72 h的VAS评分差异无统计学意义(P>0.05)。见表2。

表2 2组术后VAS评分比较 分,
2.2 2组手术前后ODI及JOA评分比较 术后1、3个月,2组患者ODI评分均显著低于术前,JOA评分均显著高于术前,且观察组患者ODI评分均显著低于对照组,JOA评分均显著高于对照组(P<0.05)。见表3。

表3 2组手术前后ODI及JOA评分比较 分,
注:与术前比较,*P<0.05;与对照组比较,#P<0.05
2.3 2组术后3个月随访时腰椎功能恢复效果比较 观察组术后3个月随访时腰椎功能优良率显著高于对照组(Z=-2.452,P=0.014)。见表4。

表4 2组术后3个月后腰椎功能恢复效果比较 例
注:与观察组比较,*P<0.05
2.4 2组术后2周内并发症发生情况比较 观察组患者术后2周内并发症发生率显著低于对照组(χ2=4.792,P=0.029)。见表5。

表5 2组术后2周内并发症发生情况比较 例
注:与对照组比较,*P<0.05
3 讨论
随着微创内固定技术发展日益成熟,目前已逐渐取代传统的开放性手术,成为治疗多种腰椎疾病的主要方法。其中,OLIF作为一种新型微创椎间融合术,主要经手术节段上位神经根及腰丛神经前方作为手术入路,具有入路损伤小、融合器体积大、间接减压、在恢复前凸方面效果更佳等优势。但是患者常会发生术后疼痛、恶心、呕吐、应激反应、睡眠障碍、运动障碍等并发症,严重影响其生活质量及工作效率。
既往研究表明,实施围术期护理干预及术后康复训练对接受腰椎融合术的患者具有积极的促进作用[10]。近年来,ERAS理念在全球的应用已逐步扩展至普通外科、骨科、心血管科等领域,均取得了良好的效果,更加符合微创理念。其核心原则在于通过加强多学科协作优化围术期干预措施,以达到减少创伤、减轻应激反应及快速康复的目的。因此,本研究将ERAS围术期护理干预应用于接受OLIF治疗的腰椎滑脱症患者中,以探求其应用效果。
多数腰椎滑脱症患者为老年人,通常合并冠心病、高血压等基础疾病,会对手术效果产生一定影响。因此术前对患者的疾病严重程度进行详细评估,有助于减少术后并发症的发生,及时调整个性化的康复计划。部分患者术前存在不同程度的焦虑、紧张等负性情绪,不仅会间接影响手术的顺利开展,甚至会发生不良应激反应,从而妨碍术后康复进程。因此,术前由脊柱外科的资深护师详细告知患者ERAS相关知识,能够尽量缓解紧张焦虑的情绪,积极地配合护理工作的开展。有研究表明,术前开展营养风险筛查及早期营养支持在围术期护理中尤为重要[11]。Lavernia等[12]认为,患者围术期的营养状态与术后并发症发生率、住院时间及医疗费用均存在密切联系。本研究结果显示,观察组术后2周内并发症发生率显著低于对照组(χ2=4.792,P=0.029)。这与陈少华等[9]的研究结果基本一致。
术中低体温会增加患者的氧消耗,降低动脉血样饱和度,从而引起机体缺氧,还会增加不良反应的发生率。因此,护理人员在术中积极使用保温毯或加热输液装置等措施,能够有效减轻机体的应激反应,显著改善其预后。剧烈疼痛会造成患者惧怕术后功能锻炼,容易导致肌肉萎缩、压疮及下肢静脉血栓等并发症的发生[13]。因此,本科室采取疼痛管理的新模式来代替传统的按需、按时给止痛药,主要实施术前疼痛评估、健康宣教、超前镇痛、多模式镇痛等措施。本研究结果显示,术后24、48 h,观察组VAS评分均显著低于对照组(P<0.05);但2组术后72 h的VAS评分差异无统计学意义(P>0.05)。本研究表明,对患者做好疼痛评估及健康宣教,按照医嘱合理地给予镇痛药物,能够有效提高患者疼痛阈值,减少不良应激反应,积极地配合治疗与护理。此结果与林海燕等[14]的研究结果相似。
ERAS理念提倡患者术后早期下床活动,早期进行功能康复训练[15]。这是由于长期卧床会造成患者肌肉强度减弱、损害肺功能、增加下肢深静脉及血栓的形成。术后早期下床活动并实行功能康复训练有助于改善术后肌肉功能,减少肺部感染的发生,能够显著促进腰背肌力量的恢复。本研究结果显示,术后1、3个月,2组ODI评分均显著低于术前,JOA评分均显著高于术前,且观察组ODI评分均显著低于对照组,JOA评分均显著高于对照组(P<0.05)。观察组术后3个月随访时腰椎功能优良率显著高于对照组(Z=-2.452,P=0.014)。上述结果与张春虹等[6]的研究结果基本一致。
综上所述,将ERAS围术期护理应用于腰椎滑脱症OLIF治疗中,有利于减轻术后早期疼痛,降低术后并发症发生率,促进患者术后尽快康复,显著改善腰椎功能,提高其临床疗效,值得临床广泛推广。

