丁苯酞软胶囊治疗帕金森病及相关并发症有效性的Meta分析
杨 婷,郑晓俊
帕金森病(Parkinson′s disease,PD)是一种中枢神经系统长期退行性疾病,主要影响运动系统。各种症状随着时间推移逐渐出现,如早期的身体摇晃、僵硬、行动缓慢以及行走困难,到中后期出现痴呆、抑郁和焦虑症状等[1]。目前帕金森病尚无治愈方法,治疗的目标是改善症状,保障病人生活质量。目前的治疗方法多采用左旋多巴类药物,同时辅以盐酸多奈哌齐和盐酸舍曲林等药物对帕金森病并发症(如痴呆、抑郁和焦虑等)进行对症治疗[2-3]。但随着病情发展和神经元的持续丢失,这些药物的疗效均会逐渐降低,无法维持病人自主生活能力,生活质量逐步下降。近年来,帕金森病的发病率呈明显上升趋势,其与脑血管病有着密不可分的关系[4]。现有部分临床医生尝试使用丁苯酞软胶囊治疗帕金森病及其相关疾病。为了客观地评价丁苯酞软胶囊与其他药物联合应用治疗帕金森病的疗效,本研究对所有纳入文献进行Meta分析,系统评价丁苯酞软胶囊治疗帕金森病及相关并发症的临床有效性。
1 资料与方法
1.1 文献纳入与排除标准
1.1.1 研究类型 随机对照试验(randomized controlled trials,RCT)。
1.1.2 研究对象 成年(≥18岁)帕金森病病人;根据中华医学会神经病学分会帕金森病及运动障碍学组制定的《中国帕金森病治疗指南》确诊为帕金森病[5];病人种族、国籍、病程不限。
1.1.3 干预措施 对照组病人给予美多芭或多奈哌齐等对症治疗;治疗组在对照组基础上口服丁苯酞软胶囊治疗。
1.1.4 结局指标 统一帕金森病评分量表(Unified Parkinson′s Disease Rating Scale,UPDRS)评分;蒙特利尔认知评估量表(Montreal Cognitive Assessment,MoCA)评分;日常生活活动能力量表(Activity of Daily Living,ADL)评分;汉密尔顿抑郁量表(Hamilton Depression Scale,HAMD)评分;简易智力状态检查量表(Mini-mental State Examination,MMSE)评分;血清神经生长因子-3(neurotrophins-3,NT-3);帕金森病蛋白7(Parkinson disease protein 7,PARK7);C反应蛋白(C reactive protein,CRP)。
1.1.5 排除标准 ①重复发表文献(以数据较新且最完整为准);②无主要结局指标的文献;③研究疾病不符合纳入要求的文献;④非RCT的文献;⑤动物实验研究文献。
1.2 文献检索策略 参考由Cochrane协作网制定的RCT检索策略,在中国知网(CNKI)、维普、万方、中国生物医学文献数据库(CBM)中,以中文帕金森、丁苯酞软胶囊和恩必普为检索词进行检索;在美国国立生物技术信息中心提供的PubMed数据库中,以英文Parkinson′s disease、Butylphthalide和NBP为检索词进行检索,检索时限为建库至2019年6月。
1.3 文献筛选与资料提取 由两位评价员独立筛选文献、提取资料并交叉核对,若遇分歧,须由第三方协助判断,缺乏的文献资料尽量与作者联系予以补充。文献筛选时首先阅读文章标题和摘要,在排除明显不相关的文献后,进一步阅读全文,以确定最终是否纳入。资料提取内容主要包括:①纳入研究文献的基本信息,如论文题目、第一作者、发表时间及期刊名称等;②研究对象的基本特征,如样本量、年龄、性别、国籍、诊断标准和疾病状况等;③干预措施及其具体细节;④偏倚风险评价的关键要素,如随机序列的产生、分配隐藏和双盲等;⑤相关结局指标的有效性和安全性等。
1.4 纳入研究的偏倚风险评价 采用 Cochrane 协作网的偏倚风险评价工具评价纳入研究的偏倚风险。
1.5 统计学处理 采用RevMan 5.3软件进行Meta分析。连续性变量结局指标均采用均数差(MD)为效应量。采用χ2检验并结合I2定量评价各研究结果间的异质性。若异质性低(P≥0.10 且I2≤50%),采用固定效应模型进行 Meta 分析;若异质性高(P<0.10或I2>50%),则进行异质性来源分析,排除明显临床异质性的影响后,采用随机效应模型进行Meta分析。
2 结 果
2.1 文献检索流程及结果 初检共获取相关文献184篇,经剔除重复文献等逐层筛选后,最终共纳入15项RCT,涉及病人1 174例。文献筛选流程及结果见图1。

图1 文献筛选流程图
2.2 纳入研究的基本特征与偏倚风险评价结果(见表1、表2)

表1 纳入研究的基本特征
注:T为治疗组;C为对照组;①为UPDRS评分;②为MoCA评分;③为ADL评分;④为HAMD评分;⑤为MMSE评分;⑥为NT-3;⑦为PARK7;⑧为CRP。

表2 纳入研究的偏倚风险评价
2.3 Meta分析结果
2.3.1 UPDRS评分 共纳入13项[6-11,13-18,20]研究。异质性检验分析结果显示各项研究间异质性较大(P<0.00001,I2=95%),故采用随机效应模型。Meta分析结果显示,治疗组UPDRS评分低于对照组,差异有统计学意义[MD=-10.13,95%CI(-11.62,-8.65),P<0.000 01],提示联合应用丁苯酞软胶囊能够明显改善帕金森病病人症状。详见图2。

图2 两组UPDRS评分比较的Meta分析
2.3.2 MoCA评分 共纳入6项[11-12,15,17-19]研究。异质性检验分析结果显示各项研究间无异质性(P=0.79,I2=0%),故采用固定效应模型。Meta分析结果显示,治疗组MoCA评分明显高于对照组[MD=3.33,95%CI(2.68,3.99),P<0.000 01],提示丁苯酞软胶囊能够明显改善帕金森病病人认知功能。详见图3。

图3 两组MoCA评分比较的Meta分析
2.3.3 ADL评分 共纳入7项[8,11-12,15-16,18-19]研究。异质性检验分析结果显示各项研究间有异质性(P=0.004,I2=69%),故采用随机效应模型。Meta分析结果显示,治疗组ADL评分明显高于对照组[MD=12.87,95%CI(11.06,14.69),P<0.000 01],提示丁苯酞软胶囊能明显改善帕金森病病人日常生活能力。详见图4。

图4 两组ADL评分比较的Meta分析
2.3.4 HAMD评分 共纳入4项[6-7,10,20]研究。异质性检验分析结果显示各项研究间异质性较大(P<
0.000 01,I2=90%),故采用随机效应模型。Meta分析结果显示,治疗组HAMD评分明显低于对照组[MD=-5.13,95%CI(-6.56,-3.71),P<0.000 01],提示丁苯酞软胶囊能明显改善帕金森病病人抑郁状态。详见图5。
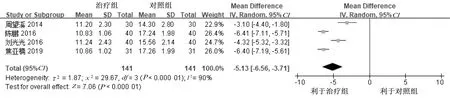
图5 两组HAMD评分比较的Meta分析
2.3.5 MMSE评分 共纳入5项[11-12,15,17-18]研究。异质性检验分析结果显示各项研究间异质性较小(P=0.16,I2=38%),故采用固定效应模型。Meta分析结果显示,治疗组MMSE评分明显高于对照组[MD=3.26,95%CI(2.44,4.08),P<0.000 01],提示丁苯酞软胶囊能够明显改善帕金森病病人的智力状态。详见图6。

图6 两组MMSE评分比较的Meta分析
2.3.6 NT-3 共纳入8项[6-7,11,13,15-16,18-19]研究。异质性检验分析结果显示各项研究间异质性较大(P=0.05,I2=51%),故采用随机效应模型。Meta分析结果显示,治疗组NT-3水平明显高于对照组[MD=8.12,95%CI(7.34,8.91),P<0.000 01],提示丁苯酞软胶囊能明显提高帕金森病病人NT-3水平。详见图7。
2.3.7 PARK7 共纳入5项[11,13,16,18-19]研究。异质性检验分析结果显示各项研究间异质性较大(P<0.000 1,I2=86%),故采用随机效应模型。Meta分析结果显示,治疗组PARK7水平明显低于对照组[MD=-10.63,95%CI(-11.97,-9.29),P<0.000 01],提示丁苯酞软胶囊能够明显降低帕金森病病人PARK7水平。详见图8。

图8 两组PARK7水平比较的Meta分析
2.3.8 CRP 共纳入10项研究[6-7,11,13,15-20]。异质性检验分析结果显示各项研究间异质性较大(P<0.000 01,I2=90%),故采用随机效应模型。Meta分析结果显示,治疗组CRP水平明显低于对照组[MD=-2.40,95%CI(-2.63,-2.16),P<0.000 01],提示丁苯酞软胶囊能明显降低帕金森病病人CRP水平。详见图9。

图9 两组CRP水平比较的Meta分析
3 讨 论
帕金森病已于2018年被收录于国家卫生健康委员会等5部门联合制定的《第一批罕见病目录》中。帕金森病在初期及年轻人中发生不易被察觉,5%~10%的帕金森病病人都在发病初期诊断中被忽略[21]。据估计,每年每10万人中即有10~18人罹患帕金森病。帕金森病的发病率随年龄增长而不断增加,在80岁后达到高峰,其中,大多数病例的平均发病年龄集中在60岁左右[22]。然而,目前还没有减缓神经退化过程的治疗方法,开始治疗的最佳时间范围也尚未明确,一般当帕金森病开始对病人的生活产生负面影响时才建议治疗,往往延误病情[23]。帕金森病除了本身对病人运动功能的影响外,对神经系统的损害更加不容忽视,其并发症如阿尔茨海默病和重度抑郁症(MDD)等能够导致病人生活质量急剧下降,增加病人死亡率。
丁苯酞软胶囊是我国拥有自主知识产权的国家一类新药,其结构与天然芹菜甲素相同,多用于治疗轻度、中度急性缺血性脑卒中。其作用机制为降低细胞内钙浓度、抑制谷氨酸释放、降低花生四烯酸含量、抑制氧自由基和提高抗氧化酶活性等[24]。Jia等[25]的一项RCT结果显示,丁苯酞软胶囊对无痴呆的认知障碍病人认知功能和整体功能均有改善作用,并显示出良好的安全性。Liao等[26]在动物实验中发现丁苯酞软胶囊可通过减轻氧化应激、内质网应激、炎症反应、神经细胞凋亡等缓解氧化应激诱导的焦虑、抑郁样行为。因此,临床医生尝试使用丁苯酞软胶囊治疗帕金森病及神经损伤相关并发症。
本次Meta分析共纳入15项RCT,所有研究对象均为帕金森病病人,其中7项试验为帕金森病合并认知功能障碍的病人,4项试验为帕金森病合并抑郁状态的病人。本研究结果显示,丁苯酞软胶囊可明显改善帕金森病病人UPDRS评分和ADL评分,对帕金森病病人的日常生活能力具有明显的改善作用。丁苯酞软胶囊可明显提高帕金森病病人MoCA评分和MMSE评分,明显改善病人认知功能障碍。治疗组HAMD评分明显低于对照组,表明丁苯酞软胶囊对帕金森病引起的抑郁状态有明显的改善作用。部分纳入研究在进行量表评分的同时,对病人血清指标进行了研究。大量研究报道证实,帕金森病病人血清中NT-3、PARK7及CRP水平可直接反映病人的病情转变,对指导治疗及判断预后起着至关重要的作用[27]。CRP是机体多系统病变的常见炎性因子,对脑神经细胞具有明显损伤作用,其水平升高可引起认知功能障碍;PARK7是在帕金森病变早期出现的常染色体隐性基因,具有强效抗氧化应激和蛋白水解酶作用,当神经系统受损后可大量释放PARK7;NT-3在神经元细胞的分化、发育过程中发挥重要作用,能够营养神经细胞。本次Meta分析结果表明,丁苯酞软胶囊能明显改善帕金森病病人NT-3、PARK7及CRP水平。
本研究的局限性:①虽然经过较为系统的检索,但目前使用丁苯酞软胶囊治疗帕金森病的研究仅出现在中文研究中,缺少英文文献的纳入,是否具有相似的研究结论尚需进一步验证;②本研究纳入的部分中文研究质量较低,可能对结果可靠性产生影响;③本研究纳入多个医疗机构的临床试验,不同医疗机构对病人的基础治疗方法、治疗时间和护理方案存在不同程度的差异,故可能发生偏倚;④丁苯酞软胶囊作为慢性病治疗药物,其长期疗效和安全性在本研究中并未涉及,因此尚需进一步验证。
综上所述,相较于常规基础治疗,联合使用丁苯酞软胶囊能够明显改善帕金森病病人认知功能障碍和抑郁状态,提高病人生活质量。但受样本量和纳入研究质量所限,以上结论尚需更多高质量研究进一步证实。

