乳腺癌保乳术后瘤床同步加量IMRT与序贯加量IMRT的疗效比较
郭守娟
(郑州大学附属郑州中心医院放疗科, 河南省郑州市 450007)
随着现代医疗技术的发展以及疾病普查的实行,乳腺癌的早期确诊数量越来越多。现今,乳腺癌患者的生存质量已得到明显提高,患者对生活质量及美容的需求也越来越高,亟须一种创伤性更小,且可有效保乳的治疗方式[1]。保乳治疗联合术后辅助放疗可很好地满足患者的美容需求,但该治疗方式的生存率和局部复发率、早晚期不良反应发生率等是否与传统治疗方式有区别,目前相关的报道仍较少[2]。因此,本研究对早期乳腺癌保乳术后瘤床同步加量调强适形放射治疗(intensity modulated radiation therapy,IMRT)与序贯加量IMRT的临床效果进行对比观察,为乳腺癌的治疗提供新思路及参考。现将结果报告如下。
1 资料与方法
1.1 一般资料 回顾性分析2013年12月至2015年6月在我院确诊为早期乳腺癌并接受乳腺癌保乳术治疗的60例患者的临床资料。纳入标准:(1)经临床和病理确诊为早期乳腺癌;(2)无放疗禁忌证;(3)行为表现量表(Karnofsky performance status,KPS)评分≥80分;(4)术后切缘阴性、原发肿瘤最大直径≤3 cm;(5)保乳术后钼靶X线检查提示乳房无广泛沙粒样钙化。排除标准:(1)不能耐受或者未完成放疗;(2)既往接受过胸部放疗;(3)临床资料不完整。入组的60例患者年龄为18~65岁。其中接受瘤床序贯加量IMRT的患者纳入常规组,共29例,占48.33%(29/60);接受瘤床同步加量IMRT的患者纳入同步组,共31例,占51.67%(31/60)。两组患者的基线资料比较,差异无统计学意义(均P>0.05),具有可比性。见表1。
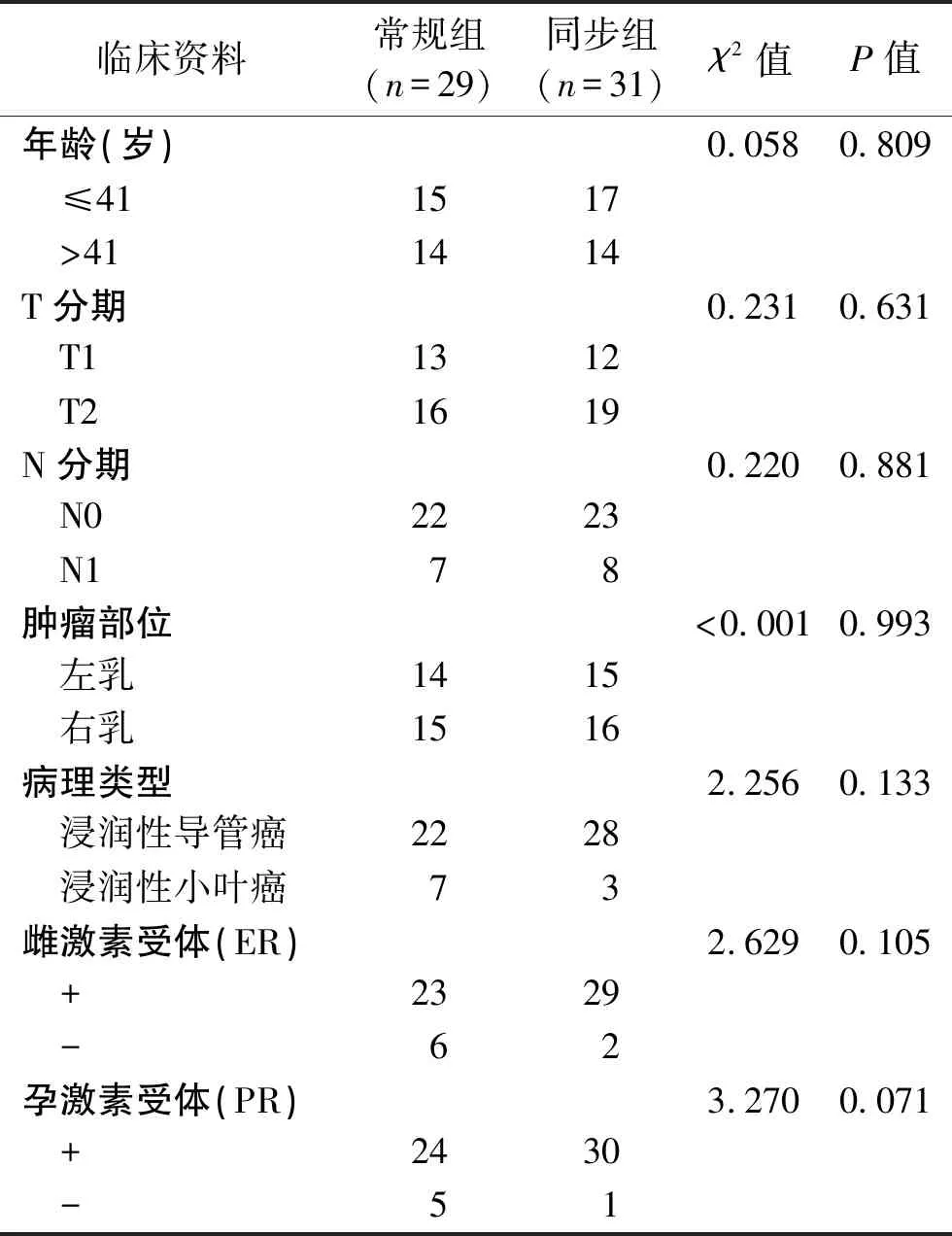
表1 两组患者基线资料比较 (n)
1.2 治疗方法 放疗计划:入组患者均同意接受保留乳房的肿瘤切除手术及术后放疗,并且进行腋窝淋巴结清扫,术腔内留置2~6个银夹标记,镜下切缘均为阴性,无血管及淋巴管的包绕浸润。术后4~6周内进行IMRT。IMRT计划:患者取仰卧位,予真空垫固定,CT平扫定位,扫描范围从下颌至肝脏下缘肾上腺水平,CT重建后层厚为3 mm。勾画靶区: 临床靶区(clinical target volume,CTV)为全乳腺组织+瘤床,CTVtb为瘤床周围的亚临床病灶,一般定义为1~1.5 cm的范围,前界不超过皮肤,后界不超过胸壁肌肉,瘤床包括术后的血肿、血清肿等术后改变及术中标记的金属夹。选用Varian Trilogy直线加速器6 MV-X线,放射治疗计划系统(Eclipse),采用IMRT计划,根据乳腺形态及瘤床位置不同,予4~8野IMRT。剂量处方要求:95%的CTV接受100%的处方剂量,90%以上的计划靶区接受100%的处方剂量,危及器官限量为健侧乳腺Dmax≤5 Gy,Dmean≤1 Gy;心脏 V30<10%,Dmean<26 Gy;患侧肺 V20<25%,V5<60%,双肺V20<20%,V5<50%。常规组患者CTV DT 50 Gy/25 F,2 Gy/F,5 F/W,CTVtb DT 10 Gy/5 F,2 Gy/F,5 F/W;同步组患者CTV DT 50 Gy/25 F,2 Gy/F,5 F/W,CTVtb 60 Gy/25 F,2.4 Gy/F,5 F/W。
1.3 观察指标 进行为期5年的随访,放射治疗期间每周进行门诊随访,观察患者急性放疗不良反应;首次随访在放疗后第3个月,放疗结束后前2年每3个月随访1次;第3~5年,每6个月随访1次。观察比较两组患者的晚期皮肤反应、骨髓抑制、放射性肺炎等不良反应发生率,以及美容优良率、局部复发率和患者生存率。放疗损伤评定按照北美放射肿瘤协作组标准[3]分级,分为0~4级。美容优良率按照放射治疗联合中心标准[4]分为优异、良好、一般及差,优良率=(优异+良好)例数/总例数×100%[5]。
1.4 统计学方法 采用SPSS 22.0统计学软件对数据进行处理,计数资料用例数(n)或百分率(%)表示,组间比较行χ2检验,等级资料比较采用秩和检验,以P<0.05为差异有统计学意义。
2 结 果
2.1 术后放疗的不良反应比较 两组患者急性皮肤反应、骨髓抑制、晚期皮肤反应、放射性肺炎等不良反应发生率比较,差异均无统计学意义(均P>0.05)。见表2。
表2 两组患者乳腺癌保乳术后放疗的
不良反应比较 [n(%)]

不良反应常规组(n=29)同步组(n=31)χ2/u值P值急性皮肤反应0.5580.577 0级8(27.59)5(16.13) Ⅰ级14(48.28)19(61.29) Ⅱ级7(24.13)7(22.58)骨髓抑制0.4590.928 0级5(17.24)5(16.13) Ⅰ级14(48.28)16(51.61) Ⅱ级8(27.59)9(29.03) Ⅲ级2(6.90)1(3.23)晚期皮肤反应0.0040.953 0级27(93.10)30(96.77) Ⅰ级2(6.90)1(3.23)放射性肺炎0.0060.938 0级26(89.66)29(93.55) Ⅰ级3(10.34)2(6.45)
2.2 美容优良率比较 两组患者的美容优良率比较,差异无统计学意义(P>0.05)。见表3。

表3 两组患者的美容优良率比较 [n(%)]
2.3 局部复发率及生存率比较 截至2019年7月,共随访12~60个月,中位随访时间36个月,随访率100%。随访期间,两组患者的局部复发率和生存率比较,差异无统计学意义(均P>0.05)。见表4。
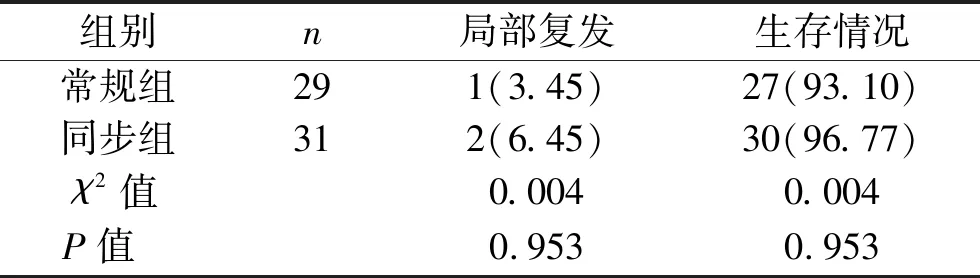
表4 两组患者局部复发率及生存率比较 [n(%)]
3 讨 论
乳腺癌是女性常见的恶性肿瘤之一,中国女性乳腺癌的发病率在全球虽然处于较低水平,但随着现代女性生活习惯的显著改变以及高危因素的普遍存在,国内乳腺癌患者发病率和死亡率明显上升[6]。因此,乳腺癌的防控以及患者生存状况的改善已经刻不容缓[7]。通过人群筛查,乳腺癌可以得到及早发现、诊断以及治疗[8]。Fisher等[9]通过深入研究现代生物学以及免疫学,发现乳腺癌是一种全身性疾病,其癌细胞为无规律转移,虽然区域淋巴结具有重要的生物学免疫作用,但不是癌细胞滤过的有效屏障,血流扩散更具有影响力。而早期乳腺癌表现为肿瘤直径≤3 cm,同侧腋窝淋巴结没有转移或仅有微小转移,无远处转移,上述观点以及临床特征则是早期乳腺癌行保乳术的理论依据以及适应证。研究表明,采用保乳术联合术后放疗同传统根治术比较,疗效与总生存率无明显差异,术后美容优良率更高,患者的依从性大幅度提高,术后患者的生活质量明显提高[10]。因此,保乳术联合术后放疗在国外已成为早期乳腺癌治疗的标准选择,可降低局部复发率,显著提高患者的总生存率[11]。
术后全乳放疗是早期乳腺癌保乳治疗的重要组成部分,包括常规瘤床序贯加量IMRT和瘤床同步加量IMRT[12]。早期乳腺癌保乳术后放疗的常规分割方案通常为5~6周内给予45~50 Gy(5次/周),利用≥1周时间给予瘤床序贯加量、瘤床同步加量IMRT技术,将瘤床需要增加的剂量平均分配至每天的剂量,全乳腺照射和瘤床加量在同一计划内完成,增加瘤床受照的单次剂量[13]。蒙渡等[14]研究显示,乳腺靶区内剂量分布具有更高的均匀性、适形性以及生物学效应,并且瘤床同步加量IMRT疗程易于个体化,适用于低年龄,满足多数患者保留生理曲线、保持良好外形的需求。
目前国内比较序贯加量IMRT和同步加量IMRT之间差异的研究较少。本文通过统计分析我院60例患者的临床资料,比较两种放疗方法的差异。其中根据常规组采用的瘤床序贯加量IMRT的剂量分割计划可以得出,该方法耗时长、放疗次数多、患者依从性差以及治疗费用高,不能满足患者对美容效果和高生活质量水平的要求;而同步组采用的瘤床同步加量IMRT计划可显著缩短治疗周期,且不良反应发生率、美容优良率、局部复发率及生存率与常规组比较,差异无统计学意义(均P>0.05)。可见,同步组的治疗模式使乳腺癌的治疗更加合理以及个体化,患者依从性更高,费用更少。
综上所述,相对于全乳放疗+瘤床序贯加量IMRT,采用瘤床同步加量IMRT可以明显缩短放疗总时间,在保证患者生存状况良好的条件下,同时减少患者往返医院的次数,节省治疗费用,提高患者的依从性。此外,在保证疗效和美容效果的同时,未增加早晚期放疗的不良反应,且患者均能按计划完成放疗,保证了肿瘤的局部控制率,具有很好的应用前景。但由于本研究样本量有限且随访时间有限,对于副反应、美容效果及疗效的评价尚需进一步扩大样本量,其中晚期毒性及远期疗效有待进一步探讨。

