复方-α 酮酸联合高通量血液透析器对血液透析患者残余肾功能和钙磷代谢的影响
丁士新
终末期肾病是各种肾病的终末阶段,患者以酸碱、水、电解质紊乱为主要临床表现,血液透析(HD)是其治疗的主要手段之一[1]。 随着血液净化技术的不断改进,终末期肾病患者能够获得长期生存,但临床应用低通量血液透析器治疗患者常并发钙磷代谢紊乱、甲状旁腺功能亢进,且不利于保护残余肾功能(residual renal function, RRF),对患者预后和生存治疗造成严重影响,可能与常规HD 对血液中大分子物质的清除作用有限有关[2]。 高通量血液透析(HFHD)是应用高分子聚合物膜作为透析器的一种新型透析技术,具有清除大分子物质和良好的生物相容性的优点[3]。 复方-α 酮酸是由多种氨基酸组成的复方制剂,口服后可通过转氨基作用调整机体正氮平衡,发挥辅助纠正机体钙磷代谢和清除毒性代谢产物的作用[4]。 为探讨更具疗效与价值的治疗方案,本研究特将复方-α 酮酸与HFHD 联合应用于血液透析患者的治疗中,观察其对患者RRF 及钙磷代谢的影响,并与常规HD 治疗效果对比,现将结果报道如下。
1 资料与方法
1.1 一般资料
选取2014 年12 月至2019 年12 月海军安庆医院收治的184 例血液透析患者为研究对象,采用随机数表法将其分为A 组、B 组、C 组和D 组,每组46例。 A 组:男25 例,女21 例;年龄(45.10 ±6.22)岁,范围20 ~67 岁;肾衰病程(17.45 ±2.37)个月,范围6 ~38 个月;原发病:慢性肾小球肾炎20 例,糖尿病肾病10 例,高血压肾病8 例,多囊肾5 例,其他3 例。B 组:男23 例,女23 例;年龄(46.20 ±6.15)岁,范围26 ~70 岁;肾衰病程(17.25 ±2.39)个月,范围6 ~42 个月;原发病:慢性肾小球肾炎18 例,糖尿病肾病11 例,高血压肾病9 例,多囊肾5 例,其他3 例。C 组:男27 例,女19 例;年龄(46.38 ±6.75)岁,范围24 ~69 岁;肾衰病程(17.96 ±2.55)个月,范围6 ~40 个月;原发病:慢性肾小球肾炎22 例,糖尿病肾病10 例,高血压肾病8 例,多囊肾4 例,其他2 例。D 组:男26 例,女20 例;年龄(45.08 ±6.20)岁,范围20 ~65 岁;肾衰病程(17.46 ±2.39)个月,范围6 ~40 个月;原发病:慢性肾小球肾炎18 例,糖尿病肾病11 例,高血压肾病8 例,多囊肾5 例,其他4 例。4 组性别构成比、年龄、病程、原发病构成比比较,差异均无统计学意义(P >0.05),具有可比性。本研究获得医院伦理委员会批准。
1.2 纳入及排除标准
1.2.1 纳入标准 (1)接受血液透析的临床指征者;(2)残余肾小球滤过率<15 ml/min 者;(3)签署知情同意书者。
1.2.2 排除标准 (1)严重过敏体质者;(2)合并恶性肿瘤、感染或其他重要脏器功能严重障碍者;(3)合并血液系统、自身免疫系统疾病者;(4)严重贫血、营养不良患者。
1.3 治疗方法
1.3.1 A 组 A 组以低通量血液透析器进行常规HD 治疗。 采用4008B 型血液透析机[德国Fresenius公司)和LOPS15 低通量聚砜膜血液透析器(德国贝朗公司,膜面积1.5 m2,超滤系数(kuf) 9.8 ml/(h·mmHg)](1 mmHg=0.133 kPa),透析方法:建立动静脉内瘘血管通路,透析血流量200 ~300 ml/min,透析液(碳酸 氢 盐: Na+130 mmol/L、 Ca2+1. 50 mmol/L、K+2.5 mmol/L)流量500 ml/min,抗凝剂为普通肝素(首剂量1 250 IU,追加1 250 IU/h,透析结束前30 min 停用),透析时间4 h,透析频率3 次/周,持续治疗6 个月。
1.3.2 B 组 B 组以复方-α 酮酸联合HD 治疗,其中HD 治疗方式完全参照A 组,同时口服复方α-酮酸片(北京费森尤斯卡比医药有限公司,国药准字H20041442,规格0.63 g ×20 s)4 片/次,3 次/d,持续治疗6 个月。
1.3.3 C 组 C 组以单纯高通量血液透析(HFHD)治疗,采用4008B 型血液透析机(德国Fresenius 公司)和HIPS15 高通量聚砜膜透析器[德国贝朗公司,膜面积=1.5 m2,kuf =50.0 ml/(h·mmHg)],透析方法与A 组相同,持续治疗6 个月。
1.3.4 D 组 D 组以复方-α 酮酸联合HFHD 治疗,其中复方-α 酮酸完全参照B 组,HFHD 完全参照C组,持续治疗6 个月。
4 组治疗期间均不调整既往非含钙的磷结合剂治疗方案。
1.4 观察指标
1.4.1 透析相关基线资料对比 记录开始治疗前4 组患者透析龄、透析频率、尿素氮、血肌酐水平;统计既往服用磷结合剂患者构成比。
1.4.2 治疗前后RRF 水平对比 收集治疗前、治疗后患者连续2 次透析间期尿标本、透析前后血标本,采用AU5800 自动生化仪(美国BeckMan Coulter公司)检测血、尿标本中的尿素氮(BUN)水平。 计算公式:RRF = [Vu/Q] × [Cu/Co2 + Ct/2],单位:ml/min;Vu:透析间期总尿量(ml);Q:透析间期时间(min);Cu:透析间期全部尿液平均BUN 浓度(mmol/L);Co2:第二次透析前血BUN 浓度(mmol/L);Ct:第一次透析后血BUN 浓度(mmol/L)。
1.4.3 治疗前后钙磷代谢指标对比 收集治疗前、治疗后静脉血样,采用AU5800 全自动生化分析仪(美国BeckMan Coulter 公司)及其配套试剂检测血钙、血磷水平、钙磷乘积、血清全段甲状旁腺激素(iPTH)水平,严格按照仪器使用操作步骤说明书进行。
1.4.4 治疗期间不良反应发生率对比 记录治疗期间恶心/呕吐、便秘、嗜睡等不良反应发生情况。
1.5 统计学处理
SPSS 26.0 统计软件处理数据,计量资料以均数±标准差(表示,多样本比较以单因素方差分析,每2 样本比较采用SNK-q 检验;计数资料以百分比表示,多样本比较需采用卡方检验,若任一理论频数为1 ~5 需进行校正,若<1 需采用Fisher′s 精确检验。 P <0.05 表示差异有统计学意义。
2 结果
2.1 血液透析患者相关基线资料对比
4 组透析龄、透析频率、尿素氮、血肌酐水平及既往服用非含钙的磷结合剂构成比比较,差异均无统计学意义(P >0.05),见表1。
2.2 治疗前后患者RRF 水平对比
治疗前4 组患者RRF 水平比较,差异无统计学意义(P >0.05);治疗后D 组RRF 水平高于其余3组,且B 组RRF 水平高于A 组和C 组,差异均有统计学意义(P <0.05)。 与治疗前比,4 组RRF 水平均降低,差异均有统计学意义(P <0.05)。 见表2。
表1 血液透析患者相关基线资料对比

表1 血液透析患者相关基线资料对比
注:A 组采用低通量血液透析进行常规血液透析治疗组,B 组采用复方-α 酮酸联合低通量血液透析治疗组,C 组采用高通量血液透析治疗组,D 组采用复方-α 酮酸联合高通量血液透析治疗组
组别 例数 透析龄(月) 透析频率(h/周) 尿素氮(mmol/L) 血肌酐(μmol/L) 既往服用非含钙的磷结合剂[例(%)]A 组 46 15.01 ±2.22 12.15 ±1.34 30.69 ±5.20 800.61 ±102.98 27(58.70)B 组 46 14.89 ±2.03 12.39 ±1.20 31.25 ±5.14 802.48 ±104.73 26(56.52)C 组 46 14.97 ±2.15 12.50 ±1.35 30.89 ±5.09 805.96 ±102.67 27(58.70)D 组 46 15.37 ±2.10 12.08 ±1.08 30.11 ±5.81 806.35 ±114.40 26(56.52)F/χ2 值 0.460 1.157 0.370 0.031 0.032 P 值 0.711 0.328 0.775 0.993 0.875
2.3 治疗前后患者钙磷代谢指标对比
治疗前4 组患者血钙、血磷水平、钙磷乘积、iPTH 水平比较,差异均无统计学意义(P >0.05);治疗后D 组血磷水平、钙磷乘积、iPTH 水平均低于其余3 组,且B 组低于A 组和C 组,差异均有统计学意义(P <0.05),4 组血钙水平差异均无统计学意义(P >0.05)。 与治疗前比,4 组患者血磷水平、钙磷乘积、iPTH 水平均降低,差异均有统计学意义(P <0.05),4 组血钙水平差异均无统计学意义(P >0.05)。 治疗期间4 组恶心/呕吐、便秘等不良反应发生率及总发生率比较,差异均无统计学意义(P >0.05)。 见表3。
表2 治疗前后血液透析患者RRF 水平对比(ml/min
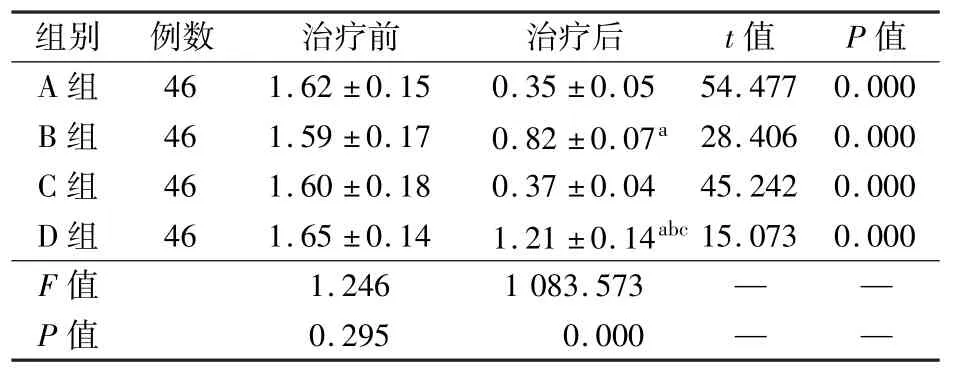
表2 治疗前后血液透析患者RRF 水平对比(ml/min
注:与A 组比较aP <0.05,与B 组比较bP <0.05,与C 组比较cP <0.05。RRF 为残余肾功能;A 组采用低通量血液透析进行常规血液透析治疗组,B 组采用复方-α 酮酸联合低通量血液透析治疗组,C 组采用高通量血液透析治疗组,D 组采用复方-α 酮酸联合高通量血液透析治疗组
组别 例数 治疗前 治疗后 t 值 P 值A 组 46 1.62 ±0.15 0.35 ±0.05 54.477 0.000 B 组 46 1.59 ±0.17 0.82 ±0.07a 28.406 0.000 C 组 46 1.60 ±0.18 0.37 ±0.04 45.242 0.000 D 组 46 1.65 ±0.14 1.21 ±0.14abc 15.073 0.000 F 值 1.246 1 083.573 — —P 值 0.295 0.000 — —
表3 治疗前后血液透析患者钙磷代谢指标对比每组n=46)
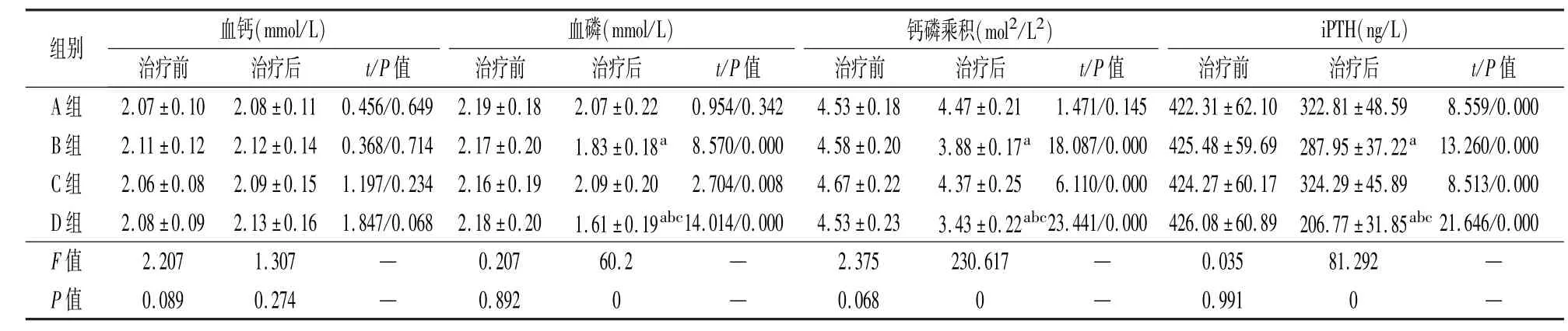
表3 治疗前后血液透析患者钙磷代谢指标对比每组n=46)
注:与A 组比较aP <0.05,与B 组比较bP <0.05,与C 组比较cP <0.05。 iPTH 为甲状旁腺激素;A 组采用低通量血液透析进行常规血液透析治疗组,B 组采用复方-α 酮酸联合低通量血液透析治疗组,C 组采用高通量血液透析治疗组,D 组采用复方-α 酮酸联合高通量血液透析治疗组
组别血钙(mmol/L)血磷(mmol/L)钙磷乘积(mol2/L2)iPTH(ng/L)治疗前 治疗后 t/P 值 治疗前 治疗后 t/P 值 治疗前 治疗后 t/P 值 治疗前 治疗后 t/P 值A 组 2.07±0.10 2.08±0.11 0.456/0.649 2.19±0.18 2.07±0.22 0.954/0.342 4.53±0.18 4.47±0.21 1.471/0.145 422.31±62.10 322.81±48.59 8.559/0.000 B 组 2.11±0.12 2.12±0.14 0.368/0.714 2.17±0.20 1.83±0.18a 8.570/0.000 4.58±0.20 3.88±0.17a 18.087/0.000 425.48±59.69 287.95±37.22a 13.260/0.000 C 组 2.06±0.08 2.09±0.15 1.197/0.234 2.16±0.19 2.09±0.20 2.704/0.008 4.67±0.22 4.37±0.25 6.110/0.000 424.27±60.17 324.29±45.89 8.513/0.000 D 组 2.08±0.09 2.13±0.16 1.847/0.068 2.18±0.20 1.61±0.19abc14.014/0.000 4.53±0.23 3.43±0.22abc23.441/0.000 426.08±60.89 206.77±31.85abc 21.646/0.000 F 值2.2071.307 — 0.207 60.2 — 2.375230.617 — 0.035 81.292 —P 值0.0890.274 — 0.892 0 — 0.068 0 — 0.991 0 —
2.4 治疗期间患者不良反应发生率对比
治疗期间A 组患者恶心/呕吐、食欲不振、嗜睡各1 例,不良反应发生率为6.52%;B 组食欲不振2 例、嗜睡1 例,不良反应发生率为6.52%;C 组食欲不振、嗜睡各1 例,不良反应发生率为4.35%;D组恶心/呕吐、食欲不振各2 例,嗜睡1 例,不良反应发生率为10.87%;A 组恶心/呕吐、食欲不振、嗜睡各1 例,不良反应发生率为6.52%。 4 组不良反应总发生率比较,差异均无统计学意义(校正=0.289,P=0.704)。
3 讨论
终末期肾病患者肾脏损伤后残余部分称为RRF,即使生理功能不全,但RRF 在清除机体内毒素、调节水电解质平衡等方面仍有重要作用[5]。 HD是终末期肾病患者维持生命的重要治疗手段,但在维持性HD 过程中,患者RRF 仍处于持续丢失状态,因此治疗期间有效地保护RRF 对患者预后生存有重要意义[6]。 研究发现[7-8],常规HD 主要以低通量聚砜膜滤过小分子水溶性毒素,对中、大分子量毒素、脂溶性毒素及其他蛋白结合毒素的清除效果不佳,可导致血磷、iPTH 在机体重要组织堆积,易引发高磷血症,增加心血管疾病、透析相关淀粉样变发生率,且不利于保护RRF,增加维持性血液透析患者病死率。
本研究发现,治疗后D 组RRF 水平高于其余3 组,且B 组RRF 水平均高于A 组和C 组,与治疗前比,4 组RRF 水平均降低,提示复方-α 酮酸联合高通量血液透析器可保护血液透析患者残余肾功能。 血液透析通过将患者血液引流至体外,通过对流或弥散等物质交换方式,将血液中的代谢废物和多于水分清除,由于接受HD 治疗的患者存在肾功能不全现象,经过治疗会出现RRF 明显丢失的情况,且呈现不可逆性,因此,在HD 治疗期间需尽量保护RRF。 高通量血液透析器超滤系数较高,除小分子水溶性毒素外,对中、大分子量毒素的清除能力优于低通量血液透析器,有利于保护RRF[9]。 此外,高分子血液透析器生物相容性好,有利于减少粒细胞量,且有利于排出肿瘤坏死因子,起到保护RRF作用[10-11]。 本研究中高通量血液透析器对RRF 的保护作用与张九峰等[12]的研究结果一致。 复方-α酮酸中含有多种非必须氨基酸,进入机体后通过转氨基作用生成必须氨基酸,帮助维持机体正氮平衡[13],在治疗过程中可利用机体少量尿素氮,降低透析间期毒性产物的累积,利于保护RRF。
此外,本研究中,治疗后D 组血磷水平、钙磷乘积、iPTH 水平均低于其余3 组,B 组血磷水平、钙磷乘积、iPTH 水平均低于A 组和C 组,血钙水平无差异;与治疗前比,4 组血磷水平、钙磷乘积和iPTH 水平均降低,4 组血钙水平均无变化,提示复方-α 酮酸联合高通量血液透析器有助于降低血液透析患者血磷水平,调节钙磷代谢;治疗期间4 组恶心/呕吐、便秘等不良反应发生率及总发生率比较均无明显差异,提示复方-α 酮酸联合高通量血液透析器安全可靠。 临床对慢性肾病患者HD 治疗期间钙磷代谢指标建议[14],慢性肾病5 期患者血钙应维持在正常水平的低限,血磷水平应控制在1.13 ~1.77 mmol/L。机体内磷多分布于细胞内,采用HD 或HFHD 仅能清除细胞外少量磷,而无法避免透析间期磷的潴留。本研究采用口服复方-α 酮酸联合HFHD 治疗,一方面复方-α 酮酸在体内通过转氨基作用,有利于维持机体正氮平衡,从而利于抑制细胞内磷释放入血;另一方面,复方-α 酮酸的钙盐作为一种磷结合剂,进入肠道后可与磷结合,减少肠道对磷的吸收[15],增加磷的效果,最终降低血液透析患者血磷水平,从而抑制高磷对血清iPTH 分泌的促进作用,降低血清iPTH 水平,起到调节血液透析期间钙磷代谢的作用。 另外,HFHD 对透析液水质有更高的要求,可避免机体免疫反应,减轻对机体造成的不良刺激,并且不会增加恶心/呕吐等常见血液透析不良反应发生率,安全可靠。
综上所述,复方-α 酮酸联合高通量血液透析器可保护血液透析患者残余肾功能,降低血磷水平,调节钙磷代谢,安全可靠,值得借鉴。

