心脏磁共振成像及二维超声斑点追踪显像评价肺动脉高压病人右室功能的临床价值
邢 宇,周 桦
肺动脉高压(PAH)是一种肺小动脉疾病,其特征为血管增殖以及血管重塑,也是一种恶性进展性病症,可导致右心功能衰竭甚至死亡[1-2]。其病理机制主要为血管收缩、原位血栓形成以及血管重塑,增加了右心室的负荷,以致右心衰竭[3],右室功能不全是导致PAH病人死亡的主要原因,也是预测病人预后不良的独立预测因子[4]。PAH具有发病急促、致残率高、死亡率高等特点,早期诊断、及时合理治疗可有效降低病人的死亡率[5-6]。二维超声斑点追踪显像(2DSTI)基于应变、应变率显像,作为超声定量检测技术,可以追踪超声图像的斑点来得到心肌的应变率、应变以及组织速度,对心肌运动进行分析,从而评价病人的心功能[7-8]。随着医学技术的发展,心脏磁共振成像(CMRI)能够对右心室功能进行无创评价,可以连续获得整个心动周期的图像数据,受右心室形态不规则的影响较小,检测的可重复性强[9-11]。本研究比较CMRI及2DSTI对PAH病人右室功能的评价效果,现总结报道如下。
1 资料与方法
1.1 临床资料 研究组:选取2012年8月—2017年5月在我院诊治的PAH病人40例,符合PAH的诊断标准,排除其他先天性心脏病、异位心律、右室流出道狭窄、肺动脉狭窄等病人。其中男23例,女17例;年龄(56.23±1.20)岁;体质指数(21.89±2.89)kg/m2;急诊入院时间(14.33±2.98)h;收缩压(124.50±15.10)mmHg(1 mmHg=0.133 kPa),舒张压(78.20±14.29)mmHg;心率(76.33±5.10)次/min;原发疾病:系统性红斑狼疮10例,慢性阻塞性肺疾病10例,尿毒症8例,肺源性心脏病12例。对照组:为同期40名无任何心血管病的健康人,其中男22名,女18名;年龄(56.11±2.19)岁;体质指数(22.39±1.04)kg/m2;收缩压(123.01±15.02)mmHg,舒张压(78.11±14.92)mmHg。两组年龄、性别、舒张压、体质指数等比较差异无统计学意义(P>0.05),所有研究对象均签署知情同意书,本研究获得我院医学伦理委员的批准。
1.2 CMRI检查方法 选用西门子公司的1.5T双梯度超导型全身磁共振成像(MRI)扫描仪,设置200 T/(m·s)的梯度切换率,以45 mT/m作为梯度场强。选择多通道采集、相控阵线圈,采用FIESTA获得右室CMRI图像。成像参数:重复时间(TR)/回波时间(TE) min full/min full,带宽125 kHz,视野(FOV) 35 cm×35 cm,翻转角45°,扫描层厚/间隔8/0 mm,矩阵224×224,NEX=1。将整个右室覆盖,依照入选者心率的不同指导其呼气未屏气8~15 s,上述全部检查时间为30 min左右。在血流动力学参数测定中,在轴位幅度图中,勾画出感兴趣区(region of interest,ROI),采集的数据主要为三尖瓣反流速度、主动脉峰值流速、右肺动脉峰值流速等。
1.3 2DSTI检查方法 选用GE公司的Vivid 7型彩超诊断仪,设置3.5~7.0 MHz探头频率。入选者取左侧卧位,采用心尖四腔观、右室流出道观及大动脉短轴观分别测量右室舒张末横径(RVED)、肺动脉主干内径(PA)、右室面积变化率、右心室射血分数(RVEF)等指标。然后启动斑点追踪模式,选取清晰图像,保证回声斑点位于心肌内,调节心内膜边缘的曲线及ROI的宽度使之与室壁厚度一致,测量并记录右室舒张晚期峰值应变率(SRa)、收缩峰值应变率(SRs)以及舒张早期峰值应变率(SRc)。CMRI、2DSTI两种检查方法要求在3 d内完成,检查次序不限。

2 结 果
2.1 两组肺动脉收缩压(PAPs)比较 研究组与对照组的PAPs分别为(85.30±12.49)mmHg和(12.49±2.57)mmHg,研究组明显高于对照组(P<0.05)。
2.2 两组CMRI指标比较 研究组三尖瓣反流速度、主动脉峰值流速与右肺动脉峰值流速均高于对照组(P<0.05)。详见表1。

表1 两组CMRI指标比较(±s) 单位:cm/s
2.3 两组常规超声指标比较 研究组RVEF、右室面积变化率均低于对照组,PA与RVED均高于对照组,差异均有统计学意义(P<0.05)。详见表2。

表2 两组常规超声指标比较(±s)
2.4 两组2DSTI指标比较 研究组SRs高于对照组,SRc与SRa均低于对照组,差异均有统计学意义(P<0.05)。详见表3。

表3 两组2DSTI指标比较(±s) 单位:/s
2.5 相关性分析 在研究组中,直线相关分析显示,PAPs与三尖瓣反流速度、右肺动脉峰值流速、RVEF、SRs呈正相关性(P<0.05),与SRc、SRa、右室面积变化率呈负相关性(P<0.05)。详见表4。
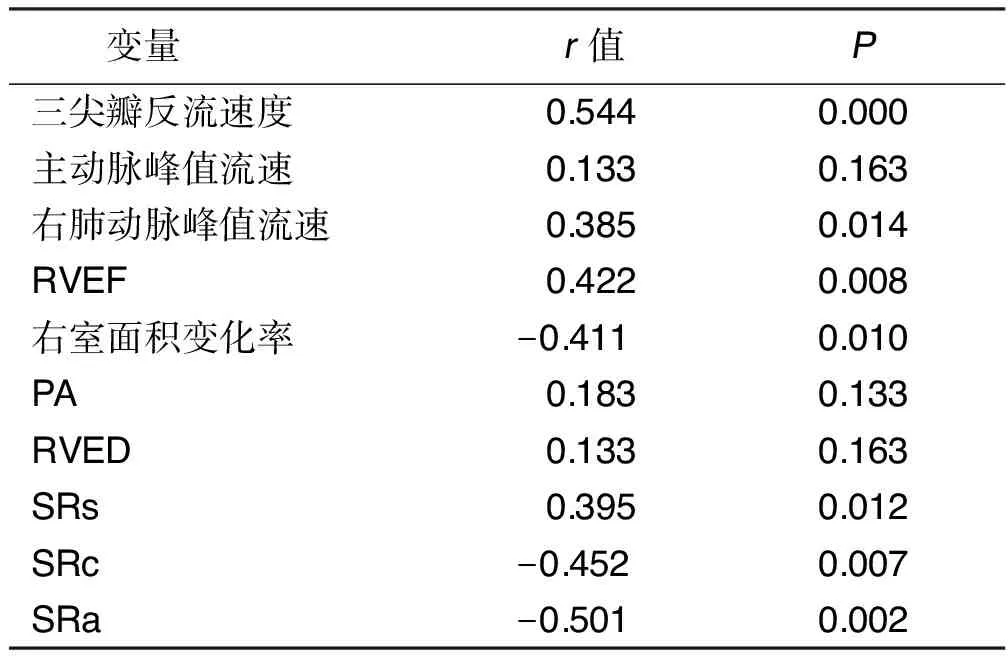
表4 PAH病人PAPs与CMRI、超声指标的相关性
3 讨 论
PAH作为肺循环疾病,其特征是肺动脉压力与肺血管阻力不断提升,导致右心衰竭,既是一种疾病,又可以是其他疾病的一种表现[12]。其发病机制为机体心肺功能异常可导致左室舒张末压和肺静脉压力升高,引起肺动脉反应性收缩,可直接刺激管壁平滑肌细胞、内膜弹力纤维及胶原纤维增生,形成PAH[13]。右室功能检查是测量肺动脉压的金标准,传统的导管法是把压力探测器放置在左肺动脉、右肺动脉或主动脉来得到血流动力学数据,虽然诊断效果好,但是为有创性检查方法,技术条件要求高,在临床上很难推广使用[14]。
MRI作为一种影像学检测技术,综合运用了形态学、功能学,有着较强客观性、清晰成像、准确性高等优点[15-16]。本研究结果显示,研究组三尖瓣反流速度、主动脉峰值流速、右肺动脉峰值流速均明显高于对照组(P<0.05)。但是有研究提出,MRI对三尖瓣反流压差进行测量得到肺动脉的收缩压,该方法无法准确得出病人肺动脉压力,同时其在测定中需要选择操作平面,造成不同操作者之间存在着差异[17]。
PAH是由不同病因导致的,其病理机制主要为血管收缩、原位血栓形成以及血管重塑,增加了右心室的负荷,右心室室壁承受压力的能力较弱,长期承受压力可能会致室壁增厚以及扩张右心室,心肌收缩、舒张功能受损,右心室心肌纤维收缩阻力增加,最终导致右心功能衰竭[18-19]。右室心肌主要为纵行方向、浅层、螺旋状的肌肉,超声评价右室整体功能时,主要是评价纵向整体功能。超声检查具有无创性、敏感度高等特征,为早期评估PAH最常用的检测手段[20]。本研究结果显示,研究组RVEF、右室面积变化率低于对照组,PA与RVED高于对照组,差异均有统计学意义(P<0.05)。常规超声方法具有一定的局限性,其固有的角度依赖性不能准确反映心肌形变,也很难反映心室的整体功能[21]。
2DSTI为一种无创评价心肌整体功能和局部功能的方法,追踪超声图像中各个小像素斑点在运动时留下的轨迹,可以获得轨迹曲线,并作为测量应变率、应变曲线的参数值,从而反映疾病状况[22]。研究发现,右心室壁的纵向应变率与右心室的射血分数存在正相关关系,而且纵向应变及应变率与右心室的等容加速度呈正相关[23]。并且2DSTI可以较准确地评估不同负荷状态下的右心室功能,对评估先天性心脏病病人的右心室功能具有一定优势。特别是2DSTI无角度依赖性,不仅可以客观、准确、定量评估局部的心肌功能,同时还可以定量、客观分析整体功能[24]。本研究结果显示,研究组SRs高于对照组,SRc与SRa均低于对照组,差异均有统计学意义(P<0.05)。特别是PAH程度越重,右室心肌应变能力受损越严重,心功能损害也越严重。
本研究直线相关分析显示,研究组PAPs与三尖瓣反流速度、右肺动脉峰值流速、RVEF、SRs呈正相关(P<0.05),与SRc、SRa、右室面积变化率呈负相关(P<0.05)。从机制上分析,因为PAH可以增加右心室的负荷,增加心肌细胞的长度,重新整合肌小节序列,右室发生代偿性重构,可导致室壁收缩能力降低,心肌功能受损。主动脉峰值流速可用于PAH病人其血流动力学情况,然而准确度较低,主要在于MRI采用三尖瓣反流压差法测量PAH病人的PAPs不够准确,不能准确判断病人的肺动脉压力[25-26]。本研究也存在一定的不足,比如导致PAH的病因种类繁多,本研究没有对不同疾病造成的PAH进行右室功能分析。
总之,CMRI及2DSTI评价PAH病人右室功能具有快速、无创的特点,其中2DSTI可更好地评价右室整体功能。

