抗体检测(免疫层析法)用于新型冠状病毒肺炎的辅助诊断及影响因素
郜振国,李 方,黄 佳,陈 媛,马合木提
自2020年1月以来,我们对新型冠状病毒肺炎(COVID-19)疾病临床表现等各个方面的认识逐渐加深[1-2],同时随着新型冠状病毒肺炎防控、诊断、治疗经验的积累,越来越多的检测方法进入我们的视野,也给我们提供了越来越多的技术手段和方法来追踪和监测新型冠状病毒肺炎(COVID-19)病例。随着疾病的发展,不管是确诊病例还是无症状感染者都会在体内产生抗体,《新型冠状病毒肺炎防控方案(第五版)》和《新型冠状病毒肺炎诊疗方案(试行第七版)》中都提到了抗体的检测,且逐步将抗体检测纳入了我们疾病诊断的范畴[3-4]。
新型冠状病毒抗体检测试剂(免疫层析法)的出现让我们对于新型冠状病毒肺炎(COVID-19)病例的发现和诊断又提供了一种实验室技术手段和方法。尽管免疫层析法检测试剂不能单独作为新型冠状病毒肺炎(COVID-19)病例确诊和排除的依据,但是由于其检测方法简便、快速,其在用于临床新型冠状病毒肺炎(COVID-19)感染者初筛方面还是具有一定的意义,可以作为临床、流行病学及核酸检测方法的补充。为了了解在实际应用过程中该方法的灵敏度、特异度及实际工作过程中哪些因素会影响检测结果阳性率。我们选择该试剂进行了应用方面的测试和研究。
1 材料与方法
1.1对象 共收集来自于不同人群的84例血清学标本进行抗体检测情况的研究。其中病例组为21例新型冠状病毒(COVID-19)确诊病例的血清标本,同时收集病例组患者咽拭子进行实时荧光定量PCR检测进行比对。确诊依据新型冠状病毒防控方案及诊疗方案。其余63例为对照组,其中包含2020年非病例血清标本13例,2016-2019年禽流感职业暴露人群血清标本50例。
1.2实验试剂 广州万孚生物技术股份有限公司生产的《新型冠状病毒抗体检测试剂(免疫层析法)》试剂盒,病例组和对照组血清标本,百世诺核酸提取试剂,上海伯杰2019新型冠状病毒核酸检测试剂盒(双重荧光PCR法)。
1.3血清学检测方法 试验所使用试剂适用于检测人血清、血浆、静脉全血中的新型冠状病毒(2019-nCoV)抗体(总抗体,包括IgG和IgM)。待测样本、检测试剂及其他材料平衡至室温,使用移液枪吸取10 μL血清样本加入测试卡小孔中,向测试卡大孔加入样本稀释液80 μL。静置15 min后观察实验结果。判断标准:被检测区(T)二抗(抗μ链抗体/抗人IgG抗体)形成红色反应线,此时结果判为阳性;反之不显带结果判为阴性。
1.4核酸提取及检测方法 核酸提取过程使用自动核酸提取仪西安天隆公司生产的NP968进行,使用百世诺预封装核酸提取试剂盒,提取过程参见试剂盒说明书。使用上海伯杰公司生产的2019新型冠状病毒核酸检测试剂盒进行核酸检测,反应体系配制方法为:每个体系加入qRT-PCR反应液12 μL,酶混合液4 μL,引物探针4 μL,加入模板5 μL,总体系25 μL。扩增反应温度为:50 ℃,10 min,1循环;95 ℃,5 min,1循环;95 ℃ 10 s,55 ℃,40 s,40循环。结果判定:扩增曲线呈S型,且Ct值≤35,为阳性;Ct值>38或未检出,为阴性;扩增曲线呈S型,且35
1.5数据分析 数据的分析使用Excel 2003及SPSS 22.0软件进行整理及统计学处理。其中非正态分布资料使用非参数检验方法中的MannyWhitney方法分析;满足正态性及方差齐性的资料使用t检验进行统计学分析,检验水准α=0.05。
2 结 果
2.1灵敏度、特异度、阳性预测值及阴性预测值 我们共纳入了84例来自不同人群的血清标本进行检测,具体情况详见表1。共选择的21例核酸检测阳性的确诊病例血清样本中,阳性检出15例,其灵敏度为71.43%;选择的非病例共63例,其中准确检测为阴性者为62例,特异度为98.41%。综合判定来看,其临床诊断准确率为91.67%;使用该种试剂进行检测的阳性预测值为93.75%,阴性预测值为91.18%。
表1 新型冠状病毒抗体检测试剂(免疫层析法)检测结果
Tab.1 Results of 2019-nCov antibody detection reagent
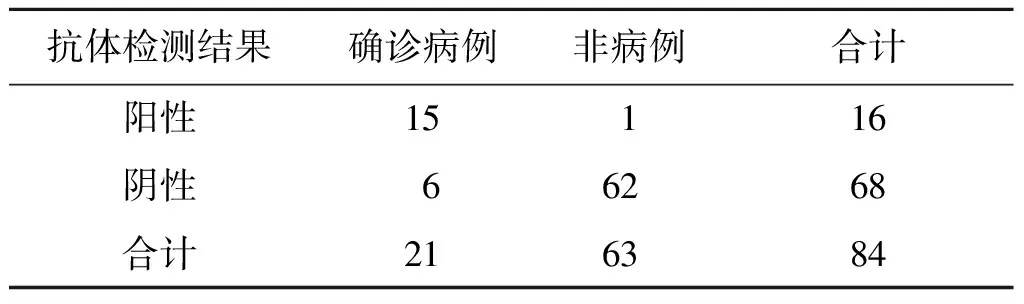
抗体检测结果确诊病例非病例合计阳性15116阴性66268合计216384
2.2病例血清学样本的采集时间对检测结果的影响 为了解采样时间对阳性检出是否有差异和影响,我们详细记录了每一例确诊病例有明确症状时间开始到样本采集时间进行检测结果的分析(见表2)。21例确诊病例的血清采集介于病例发病后的第1 d至第18 d。其中能够检出阳性的采集时间介于3~18 d,平均采集时间7.7 d。无法检出阳性的血清采集时间介于1~6 d,平均采集时间2.5 d,Wilcoxon W=33.5,P=0.011<0.05,差异具有统计学意义,所以采样时间的先后对于该试剂的阳性检出具有影响,样本采集时间过早阳性检出率降低。

图1 确诊病例中抗体检测阳性组与检测阴性组的采集时间比较Fig.1 Comparison of the collection time of the positive antibody test group and the negative test group in the confirmed cases
2.3发病后第1 d咽拭子病毒载量对于检测结果的影响 对于所纳入该研究的所有确诊病例发病后的第1 d我们都及时采集了咽拭子标本并使用统一的核酸提取试剂和核酸检测试剂进行了实时荧光定量PCR方法的检测。同时检测了ORF1a/b基因和N基因并记录了检测Ct(Cycle threshold)值(见表3)。由于我们所使用的核酸提取试剂和核酸检测试剂相同,并使用实时荧光定量PCR的检测方法,所以其Ct值的高低可以反映病例发病后早期的咽部病毒载量。ORF1a/b以及N基因的两组Ct值数据均满足正态分布及方差齐性,ORF1a/b基因检验结果t=1.390,P=0.181>0.05;N基因检验后得到t=-0.066,P=0.948>0.05。这两个基因的检测结果都显示出早期咽部病毒载量并不是影响抗体检出差异的因素。
3 讨 论
在早期的新型冠状病毒肺炎(COVID-19)防控方案中,并未提到抗体检测的方法,更多的是采用病毒核酸检测和病毒基因组测序的方法进行新型冠状病毒肺炎病例(COVID-19)的实验室检测。在实际应用中,由于核酸检测会受到咽拭子标本采集准确性及病毒清除的影响,存在一定的假阴性[5-6]。但是抗体在机体内所存在的时间较长且在相当一段时间内具有稳定性,所以测定血清中抗体的方法就会为核酸检测的方法提供很好的补充。同时,由于核酸检测的方法所需要的仪器耗材等条件比较高,耗费时间相较抗体检测试剂(免疫层析法)更长,所以其在一定时间内所检测的样本量有限。
表2 确诊病例中抗体检测阳性组与阴性组中咽拭子核酸检测Ct值比较
Tab.2 Comparison of Ct values in the throat swab nucleic acid test between positive groups and negative groups
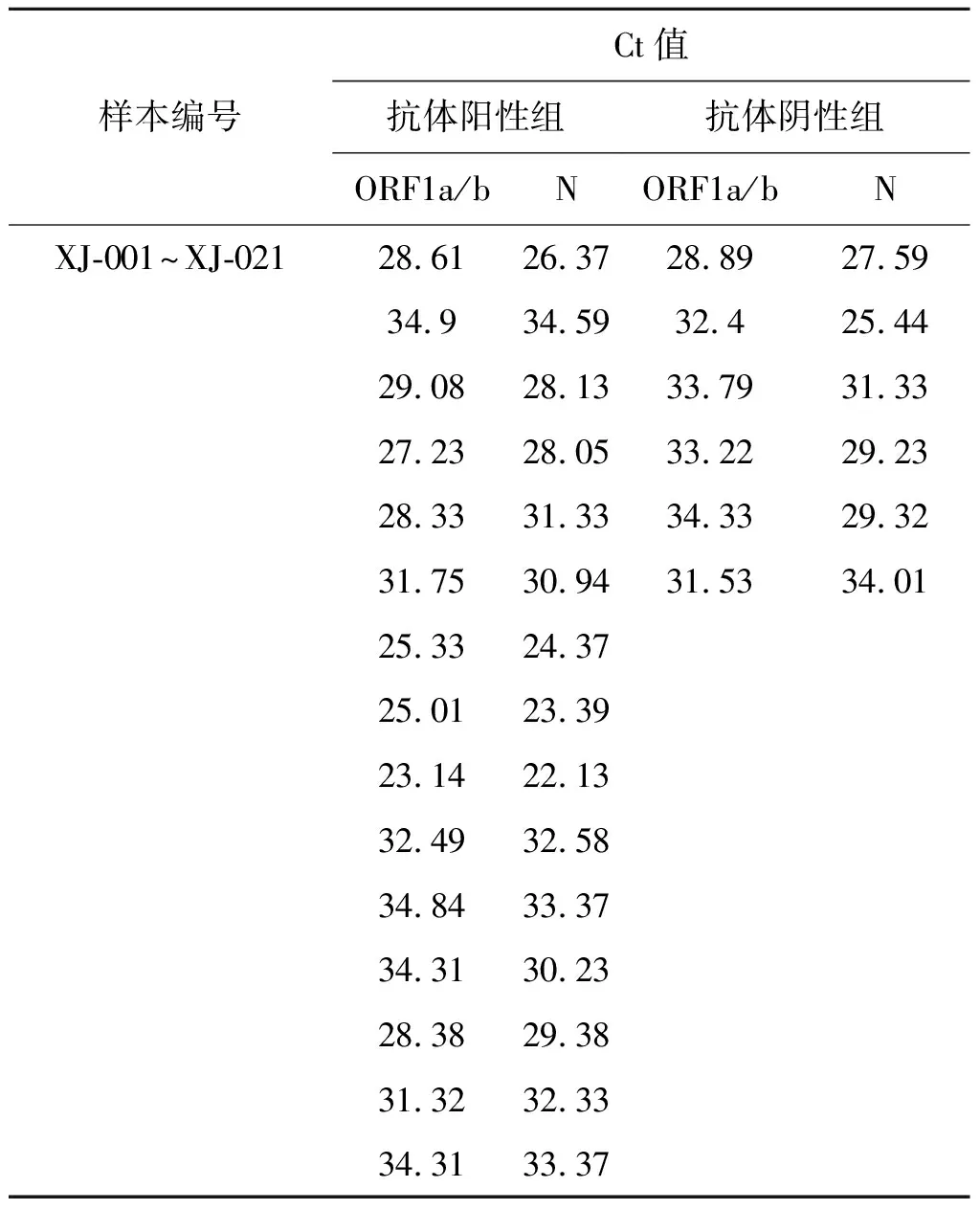
样本编号Ct值抗体阳性组抗体阴性组ORF1a/bNORF1a/bNXJ-001~XJ-02128.6126.3728.8927.5934.934.5932.425.4429.0828.1333.7931.3327.2328.0533.2229.2328.3331.3334.3329.3231.7530.9431.5334.0125.3324.3725.0123.3923.1422.1332.4932.5834.8433.3734.3130.2328.3829.3831.3232.3334.3133.37
新型冠状病毒肺炎(COVID-19)病例的抗体检测并不是只有免疫层析法这一种方法,化学发光法也是很好的选择,但其同样存在着需要大型检测仪器,检测方法较繁琐、耗费的检测时间较长等缺点。而新型冠状病毒抗体检测试剂(免疫层析法)操作简便快捷,时间短,可以在相同时间内筛检更多的病例,但是由于免疫层析法抗体检测试剂灵敏度和特异度无法达到100%,所以这对其应用带来了很大的限制,评估其灵敏度和特异度对于提出其作为诊断的补充检测方法具有很大的作用和意义。
胶体金抗体检测方法的灵敏度和特异度是诊断的主要影响因素之一。为了更好的了解该种试剂在实际应用中的情况,我们选择了84例标本进行检测。经检测,该试剂的灵敏度为71.43%,特异度为98.41%,通过本次结果可以发现,该试剂的特异度较高,灵敏度欠佳。也就表明使用该试剂进行检测存在一定的漏检可能性,同时也存在着一定的假阳性情况,并且漏检可能性相较于假阳性的比率高。同化学发光法相比较,其灵敏度和特异度均较化学发光法低(灵敏度96%,特异度100%)[7]。
通过本次研究可以发现,病例从发病到血清学样本采集的时间对抗体的阳性检出率有影响。病毒感染早期产生IgM抗体,晚期大量产生IgG抗体,由于我们所研究的试剂包被了两种抗原,所以IgM和IgG均能检出,其中任意一项阳性或者两者都阳性均记录为阳性检出,所测定的抗体为患者机体产生的总抗体,采样时间对抗体阳性检出率有影响的结论适用于总抗体检测的情况。本次研究的血清学标本采集时间介于确诊病例出现明确症状后的第1 d至第18 d。经统计学检验发现,抗体阳性组的血清学标本采集时间和抗体阴性组的血清学标本采集时间有统计学差异,抗体阴性组的血清学标本采集时间均在病例发病后的7 d以内;而阳性组的血清采集时间都相对较晚,表明病例发病后的抗体产生需要经过一定的时间,过早采集病例的血清标本会降低抗体的检出率。所以病例发病后的早期采用核酸检测的方法对于确诊新型冠状病毒肺炎(COVID-19)病例来说比较可行,该阶段病例可能处于窗口期,血清中抗体还未产生或者产生的量很低,难以检出。除了采集时间外,血清标本是否灭活对于阳性检出也存在影响,灭活标本的阳性检出率略低于未灭活标本[8]。
由于新型冠状病毒抗体检测试剂(免疫层析法)的简便、快捷,尽管其检测灵敏度没有达到90%以上,但是在注意其检测灵敏度的同时,也可以很好的用作临床诊断的辅助诊断方法,同时可以用于核酸检测方法的补充。在遇到疑似新型冠状病毒肺炎暴发疫情时,也可以用该试剂进行筛检以初步提示疫情性质。

