四种医院制剂微生物限度检查方法的适用性研究
余静,刘亮镜,徐斌
(芜湖市中医医院,安徽 芜湖 241000)
微生物限度检查是药品安全中的一项重要内容,也是药品质量控制中的必检项目之一。院内制剂多为中药复方制剂,成分复杂,且部分中药已被明确证实具有抑菌作用[1-2],因此建立合适的检验方法以消除制剂本身对微生物生长的影响非常必要,可确保检验结果的科学性和合理性,为药品安全提供保障。本次实验中所研究的四个制剂为参术健胃胶囊、十七味大活血胶囊、玉夏胶囊及腰痹康颗粒,均是本院的明星制剂,是由我院制剂室和临床专科共同研制而成的中药复方制剂,临床疗效独特,毒副作用少。其中腰痹康颗粒来源于我院名老中医戴勤瑶三十多年的经方,由丹参、当归、川断、枸杞、杜仲、木瓜等多味名贵中药组成,具有舒筋活血、补益肝肾、软坚散寒等功效,可用于治疗腰椎退行性病变。因临床疗效确切且不良反应少,可以长期服用而备受患者的青睐。玉夏胶囊是我院国家级重点专科高血压中心在中医药理论指导下,优选出的针对痰湿壅盛型的高血压制剂,主要由玉米须、夏枯草、防己等组成。因其降压平稳、疗效确切而深受广大高血压患者的欢迎,使用患者已遍及全国各地。参术健胃胶囊是我院脾胃科的重要用药,方由党参、炒白术、茯苓、黄连等组成,具有健脾和胃、化湿消导的作用,常用于急慢性胃炎、食道炎及功能性消化不良等引起的上腹饱胀、隐痛、嗳气、嘈杂等症状。十七味大活血胶囊为我院省级重点专科骨科的重要用药,方中主要含有延胡索、牡丹皮、当归、丹参、桃仁、三七等17味中药,具有活血化瘀、消肿止痛之功效,主要用于骨伤初期及手术后、肢体肿胀、疼痛等。本研究旨在建立四种医院制剂的微生物限度检查方法。报告如下。
1 试验材料
1.1 样品
玉夏胶囊三批(批号170321,170707,171108),参术健胃胶囊三批(批号170202,170603,171017),十七味大活血胶囊三批(批号170507,170823,171008),腰痹康颗粒三批(170801,171103,171203),以上样品均由芜湖市中医医院制剂室生产。
1.2 菌种
金黄色葡萄球菌[CMCC(B)26003]、铜绿假单胞菌[CMCC(B)10104]、枯草芽孢杆菌[CMCC(B)63501]、白色念珠菌[CMCC(B)98001]、乙型副伤寒沙门菌[CMCC(B)50094]由中国医学菌种保藏中心提供。黑曲霉[CMCC(B)98003]由中国药品生物制品检定所提供。
1.3 培养基
胰酪大豆胨液体培养基、胰酪大豆胨琼脂培养基、沙氏葡萄糖琼脂培养基、沙氏葡萄糖液体培养基、麦康凯琼脂培养基、麦康凯液体培养基等脱水培养基均购自北京三科科技开发公司,并严格按照说明书要求配制灭菌后使用。
2 方法与结果
2.1 菌液的制备
取按规定培养的各菌株培养物1 mL,用稀释液倍比稀释至适宜的浓度,菌数均不大于10 000 cfu/mL,备用。
2.2 供试液的制备
取样品各10 g,加至胰酪大豆胨液体培养基100 mL中,混匀,作为1∶10的供试液。取1∶10的供试液加胰酪大豆胨液体培养基稀释制成1∶20的供试液。
2.3 需氧菌和真菌及酵母菌总数计数方法的验证
按照《中国药典》2015版四部非无菌产品微生物限度检查法(通则1105)[3],试验组菌落数减去供试品对照组菌落数的值与菌液对照组菌落数的比值应在0.5~2.0之内。本次试验中,需氧菌、真菌及酵母菌总数计数方法的验证采用平皿法(各浓度的供试液均取1 mL),检验结果见表1。试验组:取制备好的菌液0.1 mL,分别加至各供试液中,混匀,使每1 mL供试液中含菌量均不大于100 cfu/mL。分别取1 mL加入无菌平皿后,倾注不超过45 ℃的相应培养基,按规定培养。菌液对照组:取2.1项下制备好的各菌悬液0.1 mL,加至10 mL的胰酪大豆胨液体培养基中,混匀。分别取1 mL加至无菌平皿,其中白色念珠菌和黑曲霉用沙氏葡萄糖琼脂注皿,35 ℃培养3~5 d;其他各试验菌株用胰酪大豆胨琼脂培养基注皿,25 ℃培养5 d。以上各菌株均平行测定2皿,菌数均不大于100 cfu/mL。供试品对照组:除不加菌外,其余操作同试验组。
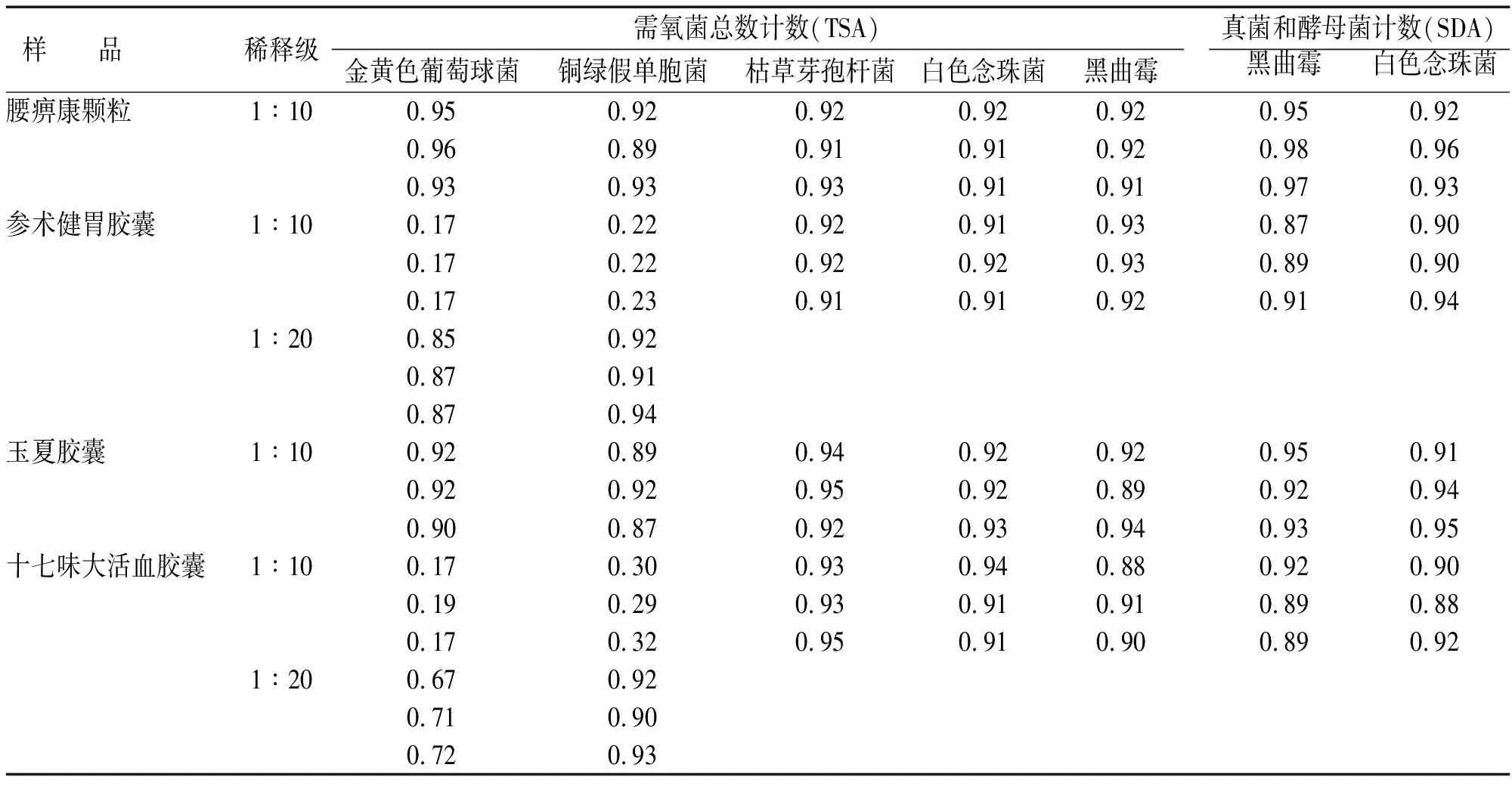
表1 需氧菌和真菌及酵母菌总数计数方法的适用性试验回收比值
2.4 控制菌检查方法的验证
2.4.1 大肠埃希菌检查方法的验证
按常规法试验。取1∶10供试液10 mL加至100 mL胰酪大豆胨液体培养基中,加入1 mL菌数不大于100 cfu/mL的大肠埃希菌悬液,混匀,置35 ℃培养24 h,按通则1106检查法检查,结果见表2。
2.4.2 耐胆盐革兰阴性菌检查方法的验证
取1∶10的供试液置25 ℃培养2 h,使供试品中的细菌充分恢复但不增殖,作为供试液。另制成1∶100,1∶1 000的溶液,按常规法试验。取供试液1∶10,1∶100,1∶1 000各1 mL分别加至10 mL肠道菌增菌液体培养基中,各制成两份,分别加入不大于100 cfu/mL的大肠埃希菌、铜绿假单胞菌菌悬液1 mL,混匀,置35 ℃培养24 h,按通则1106检查法检查,结果见表2。
2.4.3 沙门菌检查方法的验证
取供试品10 g加至200 mL胰酪大豆胨液体培养基中,加入不大于100 cfu/mL的沙门菌1 mL,混匀,置35 ℃培养24 h,按通则1106检查法检查。以上各控制菌的检查方法验证同时制备阴性对照组(除不加菌液及不加供试品外其他同试验组)、阳性对照组(除不加供试液外同试验组)、供试品对照组(除不加菌外同试验组)。检查结果见表2。

表2 四种医院制剂控制菌检查验证结果
3 讨 论
上述结果表明,以上四种院内制剂的需氧菌及真菌、酵母菌计数均可采用平皿法计数,其中腰痹康颗粒及玉夏胶囊需氧菌总数的计数采用1∶10的供试液,各试验菌株的回收比值均在0.5~2.0内,符合要求。试验中我们发现,参术健胃胶囊及十七味大活血胶囊1∶10稀释液在进行需氧菌总数计数时,金黄色葡萄球菌和铜绿假单胞菌的回收比值均<0.5,应再次对样品进行稀释后试验。因此,在采用1∶20的供试液后各试验菌株的回收比值均达到了要求。关于验证时加菌回收率的试验结果,有实验研究表明[4],主要受到两个方面因素的影响。首先是样品本身的因素。样品在检验过程中,从前处理到供试液的制备、稀释、注皿等,其抑菌能力也在不断地变化,总体上对微生物生长的抑制作用逐渐弱化。其次是操作因素。在试验操作过程中在加菌样品分散、稀释、转移等过程中造成微生物的损伤而影响回收比值。对于控制菌的验证,本次试验中,各试验组及阳性对照组均呈阳性,供试品对照组、阴性对照组均呈阴性,因此四种医院制剂均可采用常规法检验。
另外,试验中菌液的检验也是一个难点,按照《中国药典》2015版通则1105的要求,各菌株的接种量均不大于100 cfu。本文中各菌液的最终稀释级为:金黄色葡萄球菌至10-5,铜绿假单胞菌至10-7,枯草芽孢杆菌至10-3,大肠埃希菌至10-5,沙门菌至10-6,此时按规定培养后的各菌数在50~100 cfu/mL,符合试验要求。
本研究为上述四种医院制剂建立了科学可行的微生物限度检查方法,为后期制剂的检验提供了可靠依据。

