气相色谱-质谱法测定食品中17种邻苯二甲酸酯类塑化剂的含量
张国民,温素素
(1.嘉兴市食品药品检验检测院,嘉兴314050; 2.嘉兴学院 医学院,嘉兴314033)
邻苯二甲酸酯类(PAEs)塑化剂是邻苯二甲酸酐与醇类的反应产物,其化学结构由1个刚性平面芳烃和2个可塑非线性脂肪侧链组成[1]。PAEs与塑料制品中的基质是以氢键或范德华力等物理方式相结合,而非通过化学键结合到产品的碳链上,因此在强光、雨淋等环境影响下,PAEs易从塑料中不断释放,进入土壤、水体和大气等环境介质中[2-3]。长期摄入含PAEs的食品可能引起生殖系统异常,甚至存在畸型胎、癌症的风险[4]。目前针对食品中PAEs的检测主要集中在食用油、饮用水、酒类等少数几类食品中,对不同类别食品基质中PAEs的测定却相对不多[5-16]。
本工作采用气相色谱-质谱法(GC-MS)对12种具有代表性的不同类别食品中的PAEs进行测定,外标法定量,并针对不同的食品基质,优化了国家标准GB 5009.271-2016前处理流程,并进一步探讨了影响PAEs测定结果的各方面因素。本方法前处理过程简单,加标回收率较高,对食品中PAEs的测定具有一定的参考价值。
1 试验部分
1.1 仪器与试剂
Thermo TRACE GC ULTRA/DSQⅡ型气相色谱-质谱联用仪;ME204E 型电子天平;NEVAPTM111型氮吹仪;RV10型旋转蒸发仪;SZ-1型涡旋混合器;SK5210HP型超声波清洗器。
17种PAEs混合标准储备溶液:1 000 mg·L-1,分别称取各邻苯二甲酸酯标准品25 mg,用正己烷溶解并转移至25 m L 容量瓶中,用正己烷定容,混合摇匀,备用。
17种PAEs混合标准溶液系列:用正己烷将17种PAEs混合标准储备溶液逐级稀释,配制成0.05,0.1,0.2,0.5,1.0,2.0 mg·L-1的17种PAEs混合标准溶液系列。
邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二烯丙酯(DAP)、邻苯二甲酸二异丁酯(DIBP)、邻苯二甲酸二正丁酯(DBP)、邻苯二甲酸二(2-甲氧基)乙酯(DMEP)、邻苯二甲酸二(4-甲氧-2-戊基)酯(BMPP)、邻苯二甲酸二戊酯(DPP)、邻苯二甲酸二己酯(DHXP)、邻苯二甲酸丁基苄基酯(BBP)、邻苯二甲酸二环己酯(DCHP)、邻苯二甲酸二(2-乙基)己酯(DEHP)、邻苯二甲酸二苯酯(DPh P)、邻苯二甲酸二正辛酯(DNOP)和邻苯二甲酸二壬酯(DNP)等15种PAEs标准品(纯度均大于97%);邻苯二甲酸二(2-乙氧基)乙酯(DEEP)和邻苯二甲酸二(2-丁氧基)乙酯(DBEP)标准品(纯度均大于99%);试验所用试剂均为色谱纯;试验用水为全玻璃重蒸馏水。
试验所用玻璃器皿洗净后,用水淋洗3次,于丙酮中浸泡1 h,在200 ℃下烘干2 h,冷却至室温备用。
梨、菠菜、奶粉、酸奶、芹菜、黄酒、白酒、食醋、酱油、鸡精、芒果汁和面包等12种样品均购自某超市。
1.2 仪器工作条件
1)色谱条件 Thermo DB-5MS 色谱柱(30 m×0.25 mm,0.25μm);进样口温度为250℃;进样量为1.0μL;不分流进样;载气为氦气,纯度为99.999%;流量为1.0 m L·min-1。柱升温程序:初始温度为60 ℃,保持1 min;以20 ℃·min-1的速率升温至220 ℃,保持1 min;再以5 ℃·min-1的速率升温至250 ℃,保持1 min;最后以20 ℃·min-1的速率升温至290 ℃,保持7.5 min。
2)质谱条件 电子轰击离子源(EI);电离能量为70 e V;离子源温度为280 ℃;传输线温度为280 ℃;溶剂延迟10 min;选择离子监测(SIM)模式;选择离子检测组分的基他质谱参数见表1。
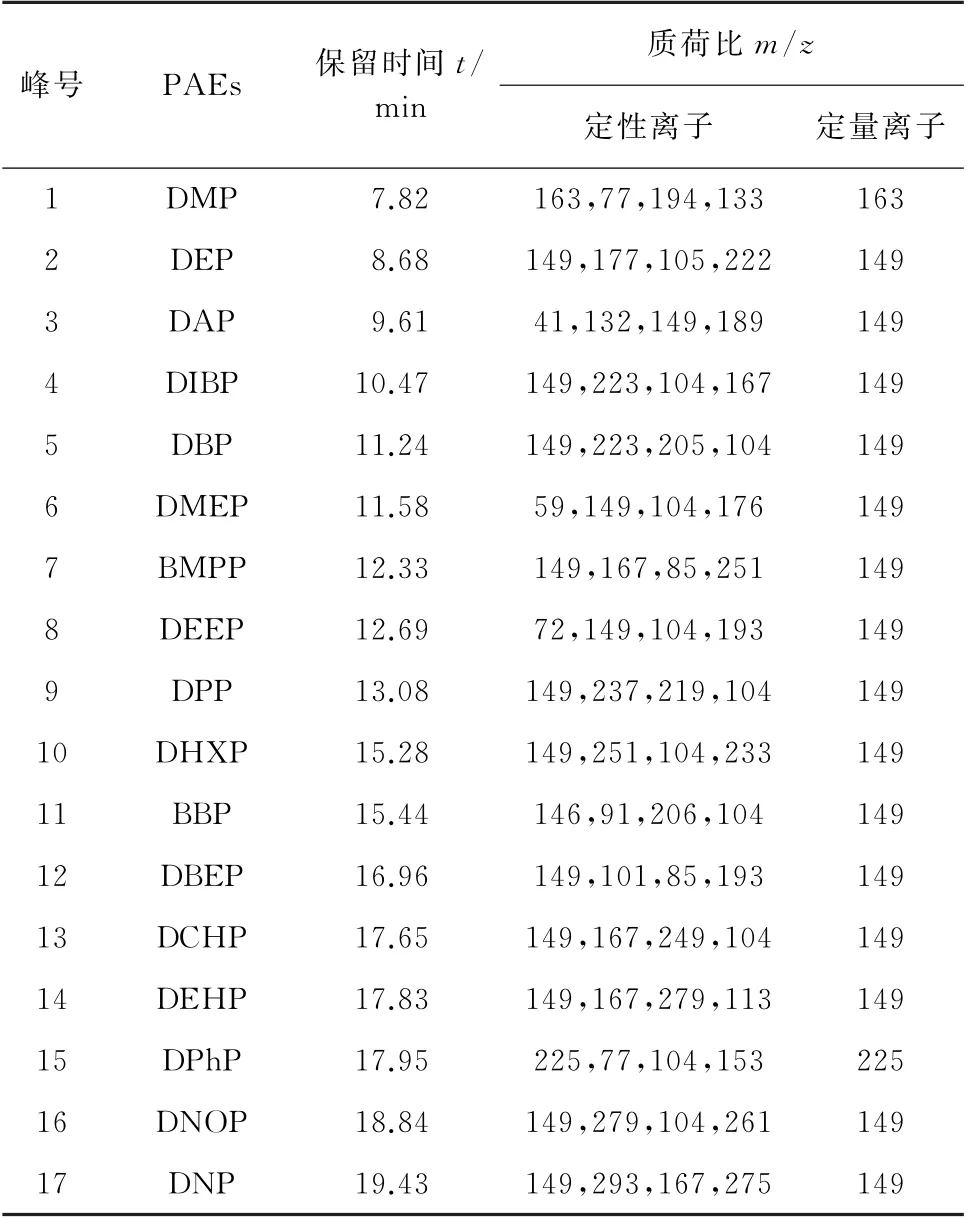
表1 质谱参数Tab.1 MS parameters
1.3 试验方法
按照国家标准GB 5009.271-2016对液态、半固态、固态等3大类12种试验样品进行前处理,按照仪器工作条件对其进行测定。同时设置空白对照试验,测定结果扣除空白后计算样品中PAEs的残留量。
2 结果与讨论
2.1 色谱行为
按照仪器工作条件对17种PAEs的混合标准溶液进行测定,色谱图见图1。
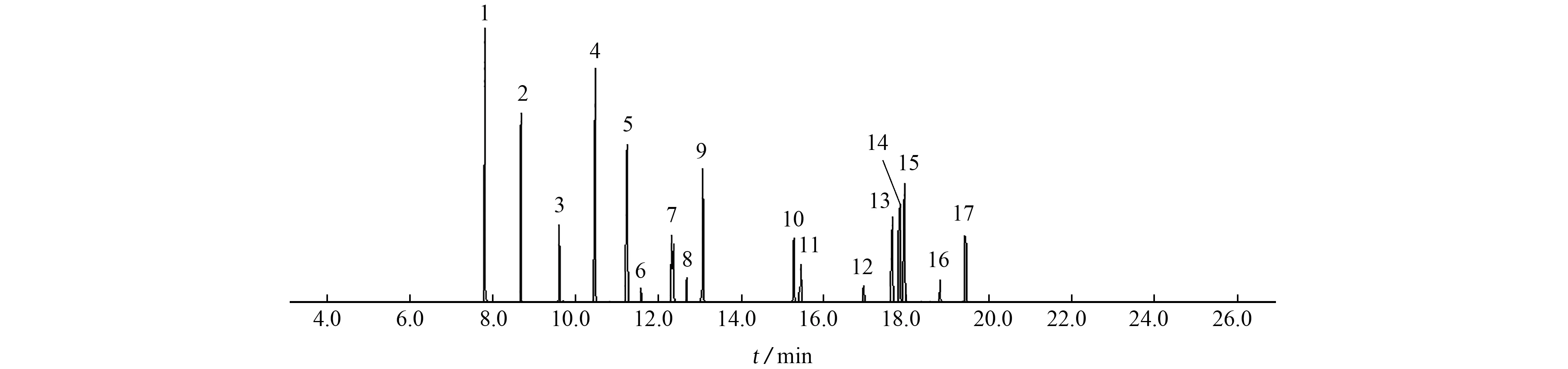
图1 17种PAEs的混合标准溶液的色谱图Fig.1 Chromatogram of mixed standard solution of the 17 PAEs
2.2 仪器工作条件的选择
17种PAEs中部分PAEs的保留时间十分接近,且PAEs属于弱极性物质,试验选择非极性DB-5MS色谱柱,并适当降低色谱柱初始温度和程序升温速率,保证PAEs得到有效分离,确保定量结果的准确性。试验发现进样口吸附和离子源脏污是影响PAEs定量结果准确性的重要因素,进样时应选用经硅烷化处理的带玻璃毛超惰性衬管,并适当提高气相进样口温度为300~310℃,正式进样前可用较高浓度的标准样品来饱和带玻璃毛超惰性衬管的活性位点,从而降低进样口吸附的影响。同时进样前应检查仪器状态,及时清洗离子源,建议多次进空白样品,减少仪器系统中残留的PAEs对试验测定结果的影响。
2.3 试验条件的选择
2.3.1 净化条件
奶粉、蔬菜和果汁等基质复杂的样品,在通过提取溶剂萃取后,存在明显的基质增强效应,对PAEs的测定造成很大的干扰。按照国家标准GB 5009.271-2016对上述基质复杂的样品进行前处理,在未经固相萃取柱净化后直接测定,发现PAEs的回收率偏高很多。试验选择菠菜、芹菜、芒果汁和奶粉等4种基质效应明显的样品进行N-丙基乙二胺与硅吸附剂复合填料(PSA/Silica)玻璃固相萃取柱净化,参照国家标准GB 5009.271-2016进行洗脱,同时对上述4种样品未经净化处理,直接上机进行测定,2种不同净化方式下17种PAEs的回收率见图2。
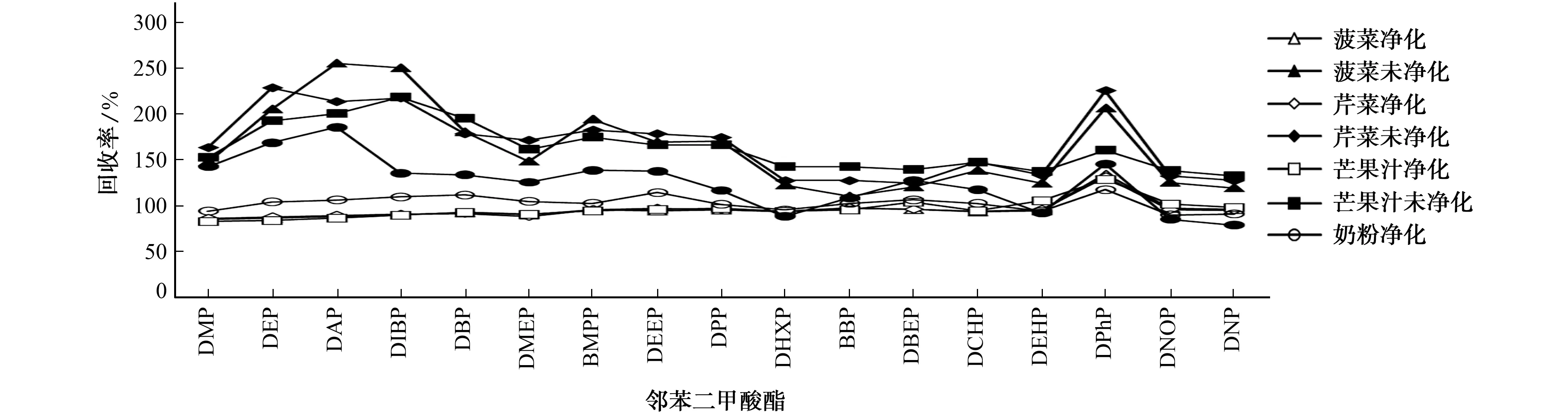
图2 17种PAEs在2种不同净化方式下的回收率Fig.2 Recovery of the 17 PAEs obtained by 2 different purification methods
由图2可知:4种样品经过PSA/Silica玻璃固相萃取柱净化后,可以有效去除色素和有机酸等基质干扰物质,17种PAEs的回收率为83.2%~135%。
2.3.2 提取溶剂
PAEs作为非极性或弱极性化合物,在水中溶解度极低,但易溶于大部分有机溶剂,试验比较了二氯甲烷、乙酸乙酯、正己烷和乙腈分别作为提取溶剂时,对白酒、鸡精、梨、食醋和面包等5 种样品中DHXP、BBP、DBEP、DCHP和DEHP等5种PAEs回收率的影响,结果见图3。
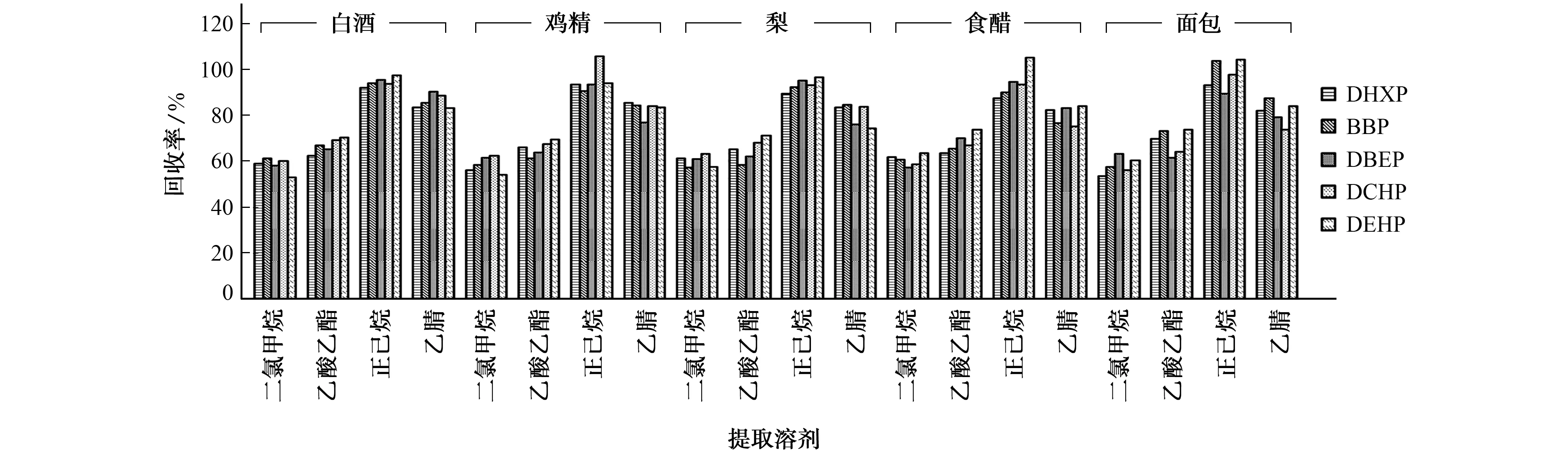
图3 提取溶剂对5种PAEs回收率的影响Fig.3 Effect of extraction solvents on recovery of 5 PAEs
结果表明:正己烷对样品中5种PAEs的回收率为80%~120%;其他提取溶剂对样品中5 种PAEs的回收率均低于正己烷。试验选择的提取溶剂为正己烷。
2.3.3 超声时间
超声可以加快两种不能互溶分散相之间的质量传递,使萃取效果在短时间内获得迅速提升,但长时间超声可能导致萃取剂严重挥发,影响测定结果的准确性。试验选择超声时间分别为10,20,30,40 min时,比较了不同的超声时间对DHXP、BBP、DBEP、DCHP和DEHP 等5种PAEs回收率的影响,结果见图4。
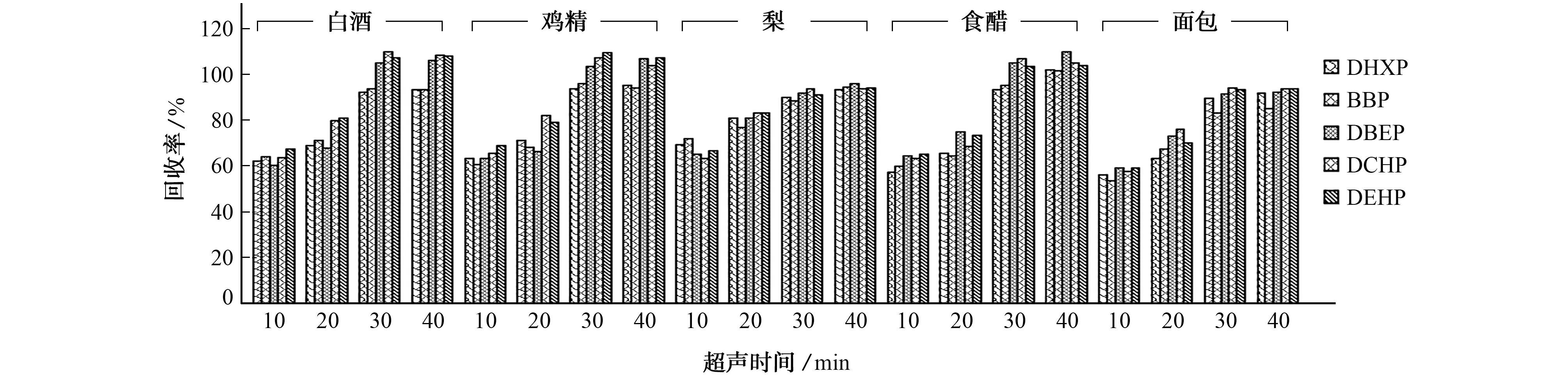
图4 超声时间对5种PAEs回收率的影响Fig.4 Effect of time of ultrasonic extraction on recovery of 5 PAEs
由图4可知:随着超声时间的延长,5种PAEs的回收率逐渐增大;当超声时间为30 min时,5种PAEs的回收率均达到较大值;继续延长超声时间,5种PAEs的回收率趋于稳定。试验选择的超声时间为30 min。
2.3.4 超声温度
研究表明,在较高温度下有机物和基质活性位点之间的作用力更容易被破坏,溶剂的溶解能力明显提升,同时溶剂的表面张力和黏度会随着温度的升高而降低,使得溶剂和基质之间的接触保持的更加良好[3]。试验选择的超声温度分别为20,30,40 ℃时,比较了不同的超声温度对DHXP、BBP、DBEP、DCHP和DEHP 等5种PAEs回收率的影响,结果见图5。
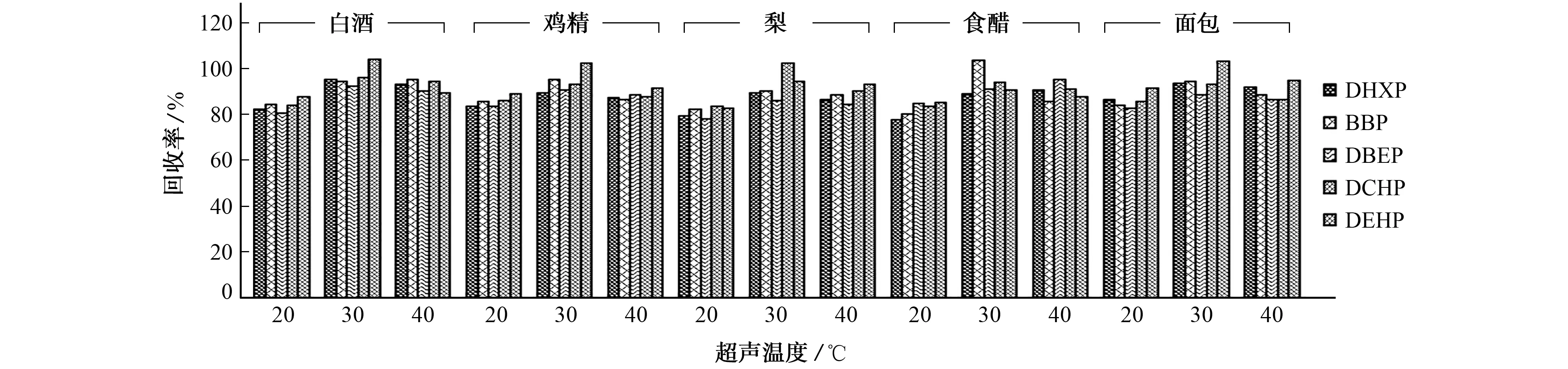
图5 超声温度对5种PAEs回收率的影响Fig.5 Effect of temperature of ultrasonic extraction on recovery of 5 PAEs
由图5可知:5种PAEs的回收率随着超声温度的升高而增大;当超声温度为30℃时,5种PAEs的回收率均达到较大值;继续增大超声温度为40℃时,5种PAEs的回收率反而下降。试验选择的超声温度为30 ℃。
2.4 空白试验影响
试验中发现相隔数天的空白试验数据有较明显差异,因此在每一批试验时都必须做空白试验,且保证同一批试验中试剂、玻璃仪器、固相萃取柱等条件相同,应选用色谱纯试剂以降低试剂空白,试验用水应为重蒸水,所有涉及玻璃器皿必须洗涤浸泡后经200 ℃烘干2 h。不应使用带有塑料管路的可调定量加液器吸取试剂,操作中不应带塑料薄膜手套,整个试验过程中,应确保避免接触塑料制品。
2.5 标准曲线与检出限
按照仪器工作条件对17种PAEs的混合标准溶液系列进行测定,以17种PAEs的质量浓度为横坐标,与其对应的峰面积为纵坐标绘制标准曲线。17种PAEs的线性范围、线性回归方程和相关系数见表2。以3倍信噪比计算方法的检出限(3S/N),结果 见表2。
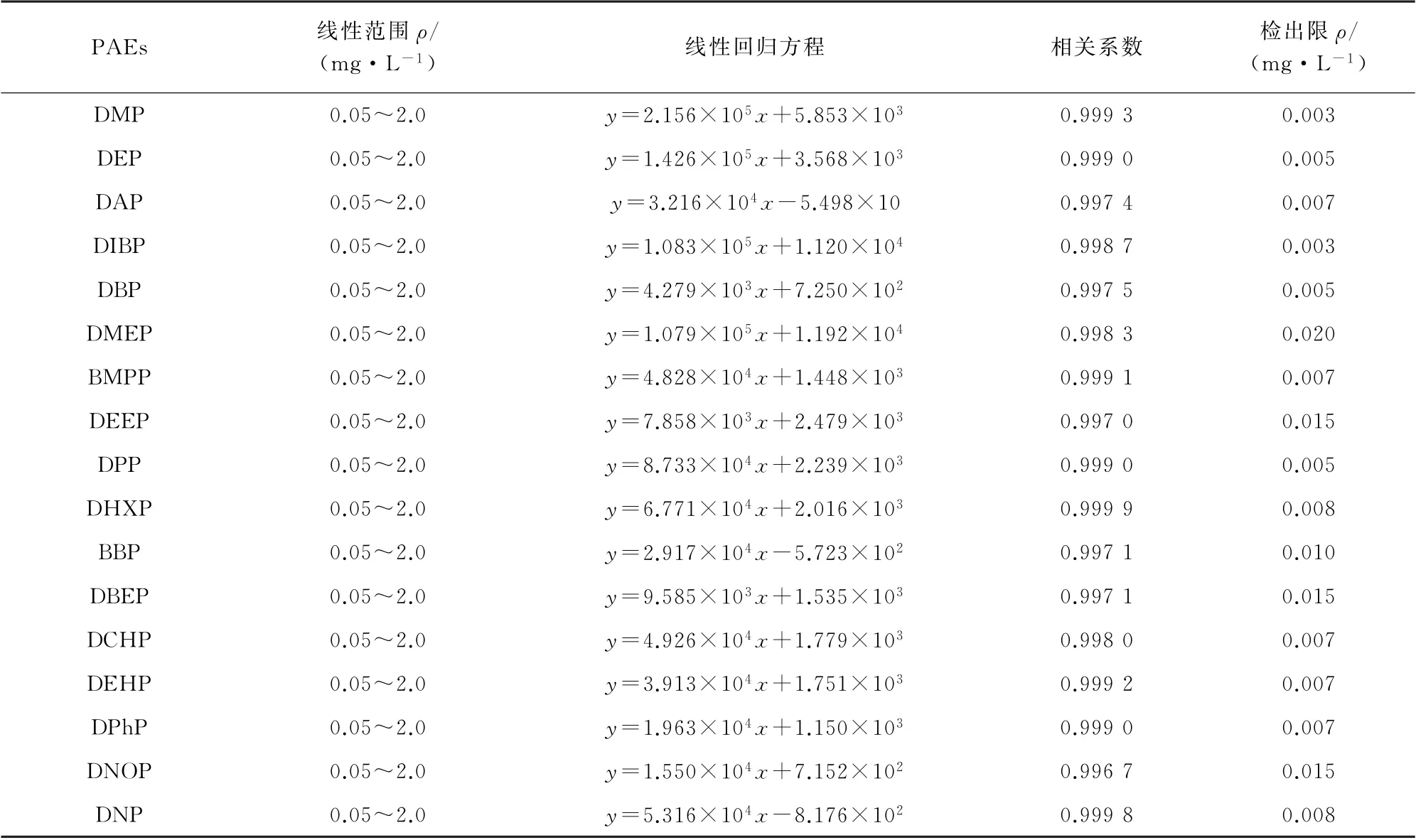
表2 17种PAEs的线性参数和检出限Tab.2 Linearity parameters and detection limits of the 17 PAEs
2.6 精密度和回收试验
按照试验方法对梨、菠菜和奶粉等12种样品分别进行不同浓度水平的加标回收试验,每个加标样品平行测定6次,扣除样品的本底值和空白后,计算回收率和测定值的相对标准偏差(RSD),结果见表3。
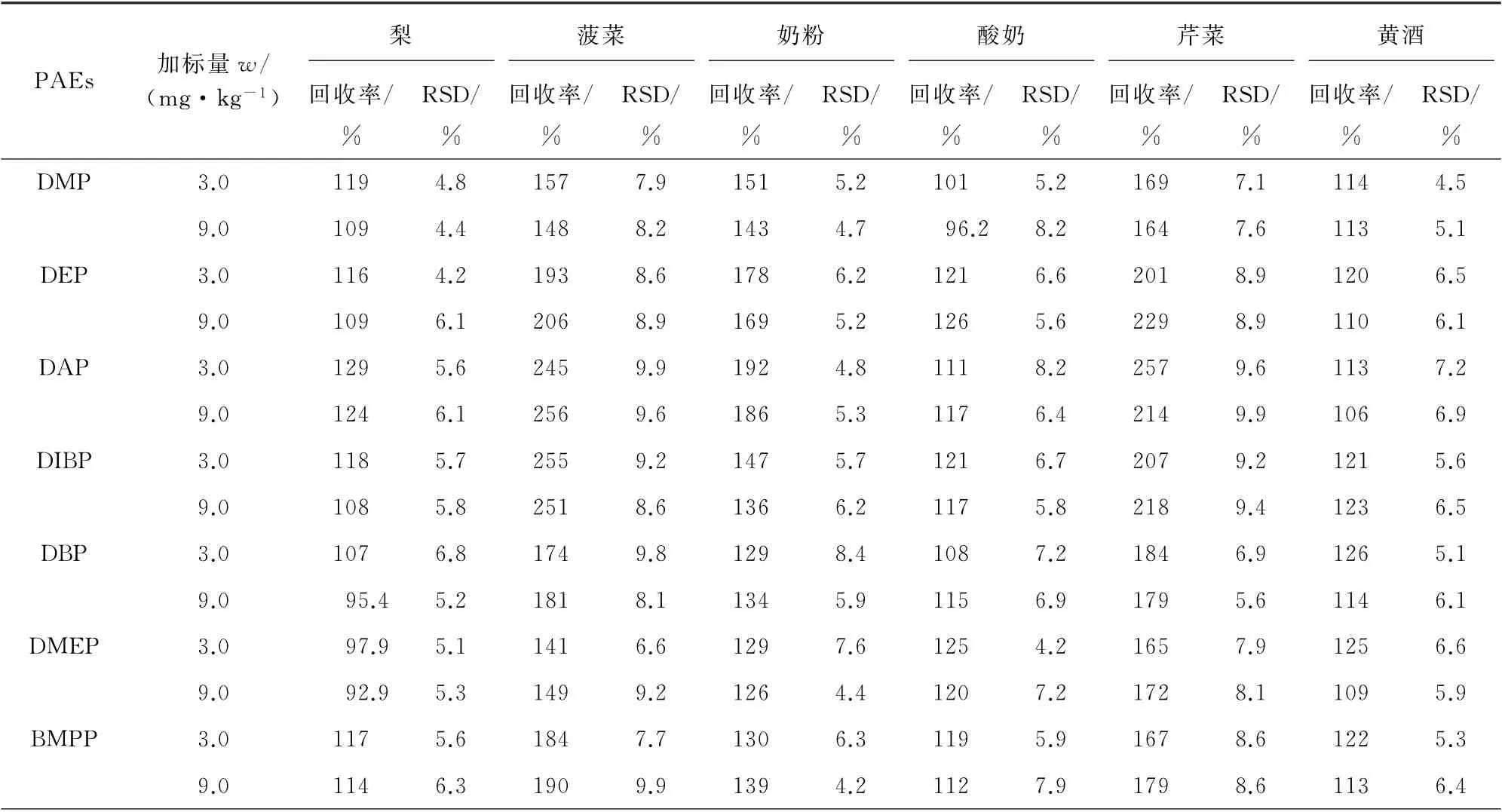
表3 梨、菠菜和奶粉等样品的精密度和回收试验结果(n=6)Tab.3 Results of tests for precision and recovery of pear,spinach and milk powder samples(n=6)
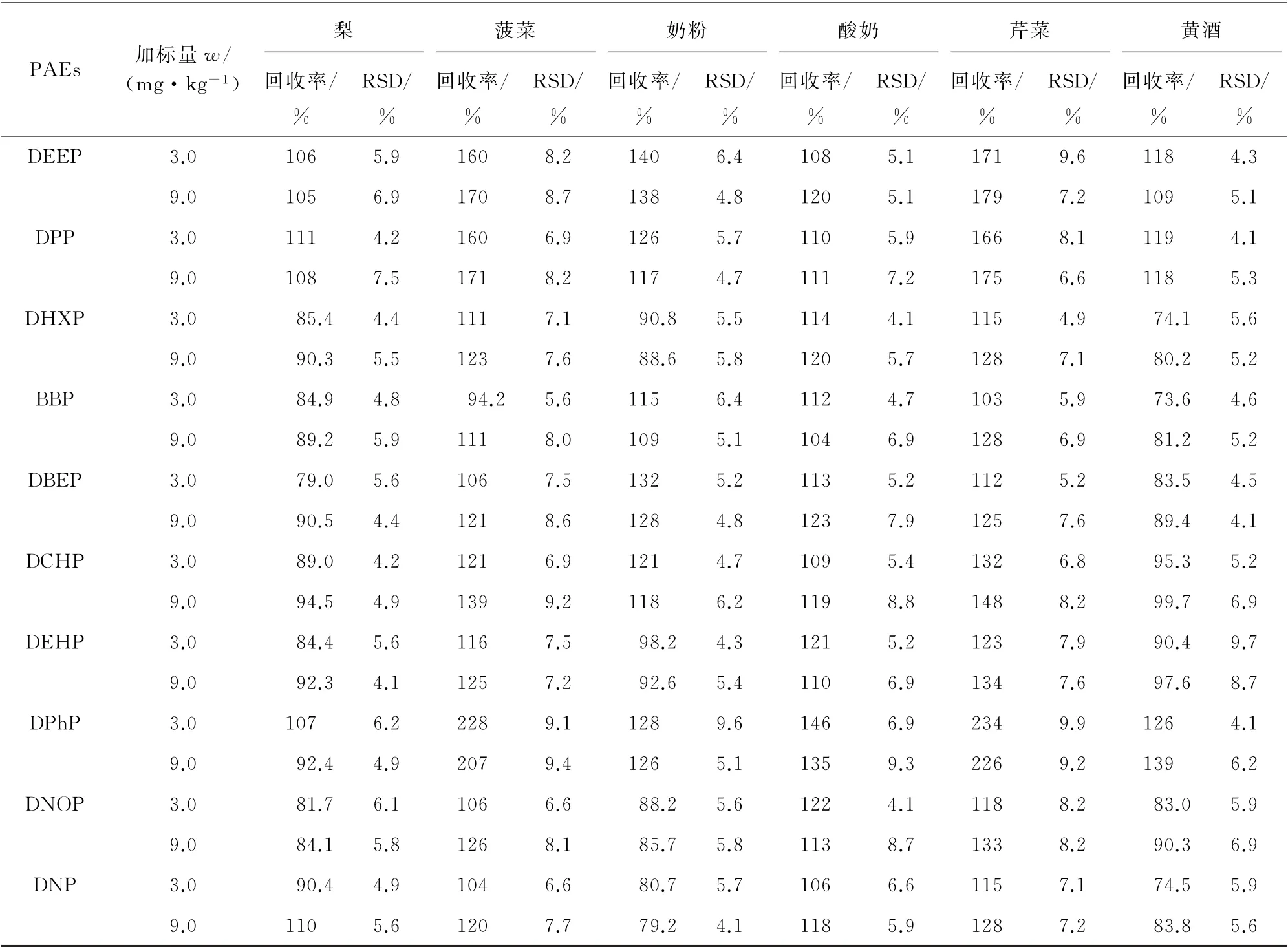
表3(续)
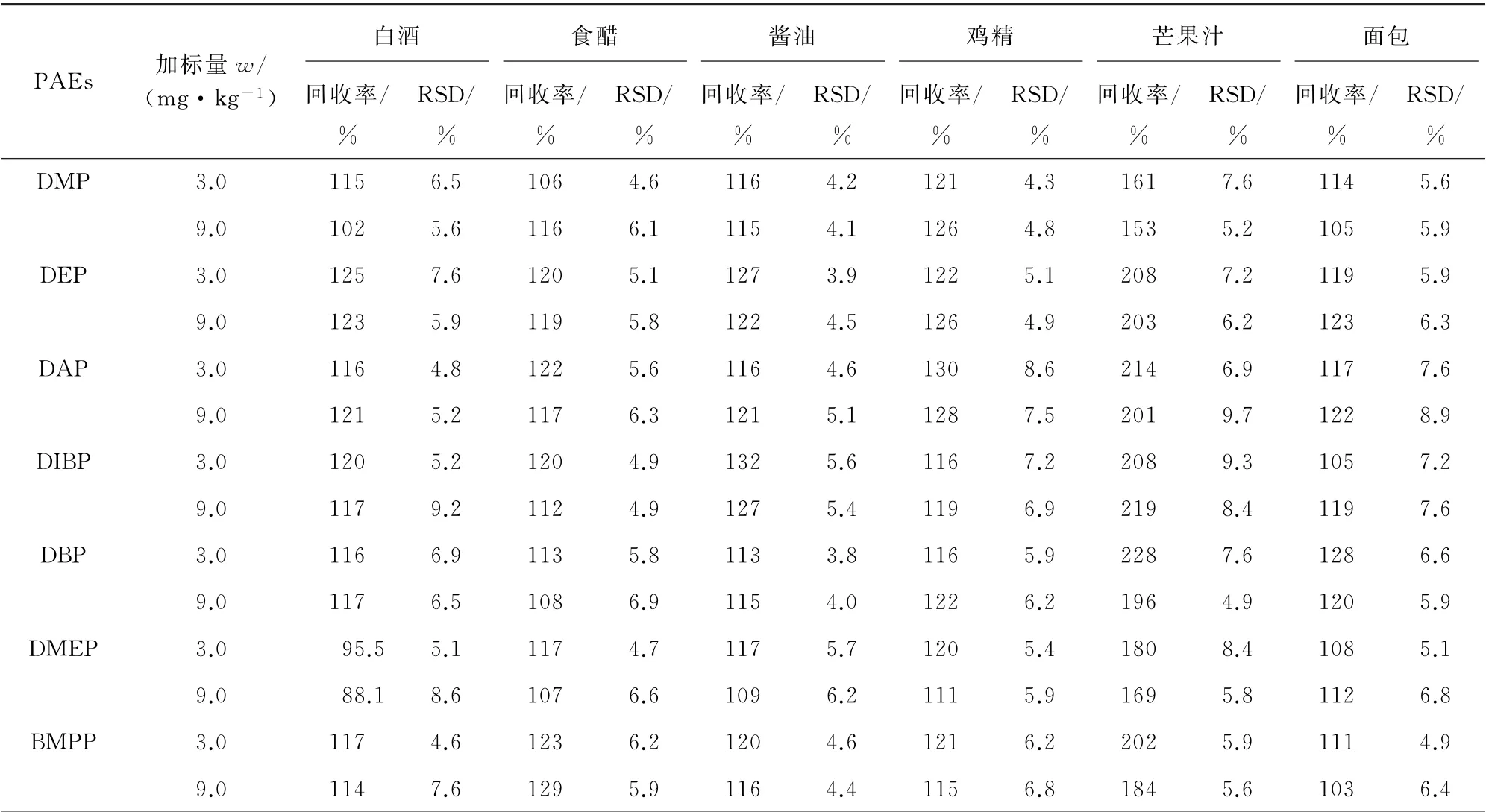
表4 白酒、食醋和酱油等样品的精密度和回收试验结果(n=6)Tab.4 Results of tests for precision and recovery of white wine,vinegar and soy sauce samples(n=6)
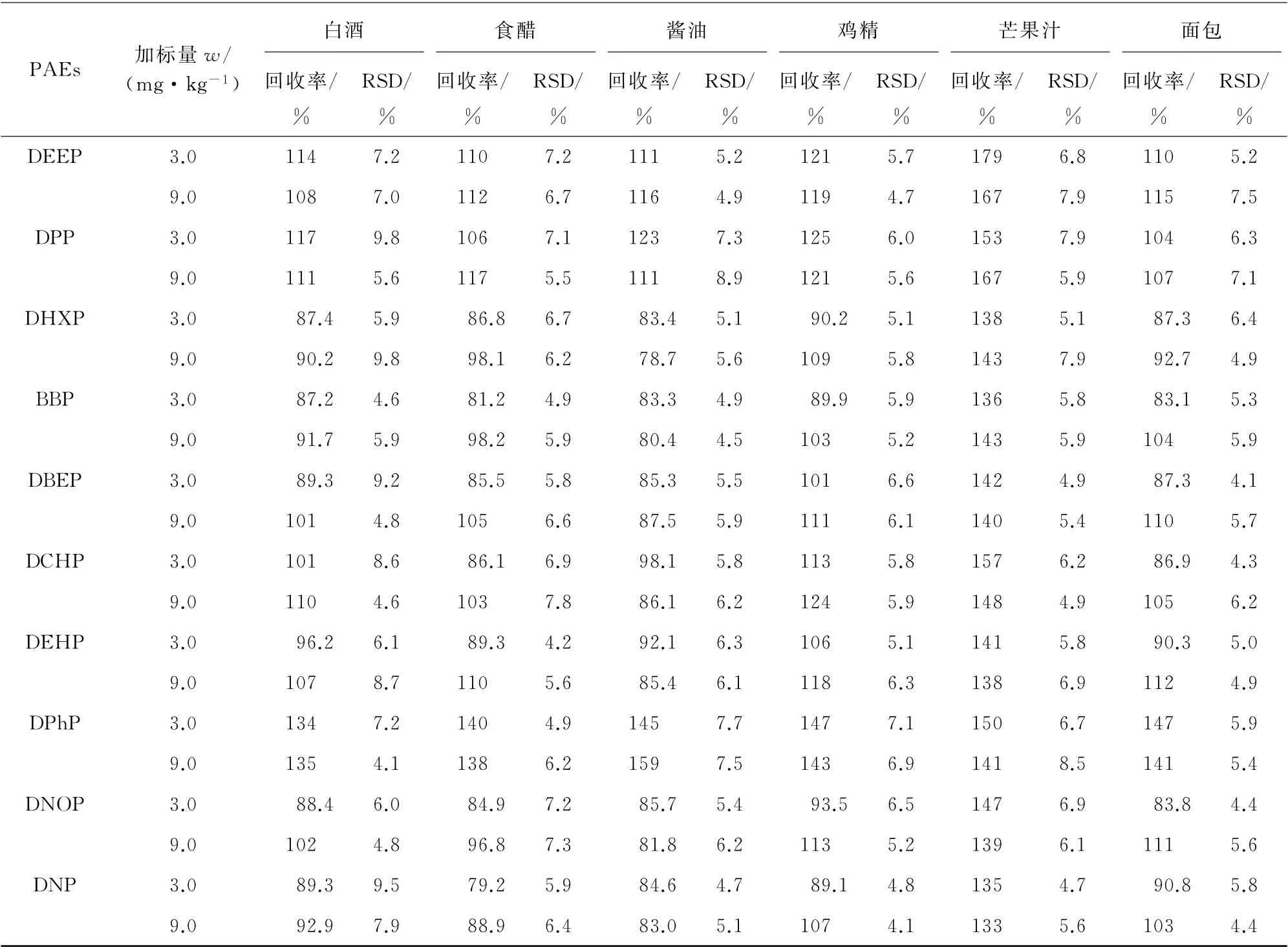
表4(续)
由表3和表4可知:基质较为复杂的样品,例如奶粉、蔬菜、芒果汁等回收率偏高,而基质相对较为简单的样品,例如白酒、黄酒、食醋等回收率较好;大部分食品中DEP、DAP、DIBP和DPh P的回收率均较高于其他PAEs的回收率。
2.7 样品分析
试验选择了水果、蔬菜、乳制品、酒类、调味品等12种有PAEs残留风险的样品,按照试验方法对其进行测定。结果表明:梨和芒果汁样品中均未检出PAEs残留;其余样品中均检出不同浓度水平的PAEs,检 出 种 类 有DMP、DIBP、DBP、DMEP、DEEP、BBP、DEHP,其中DBP 和DEEP 的检出率最高,有8种样品检出DBP 和DEEP,具体结果见表5。
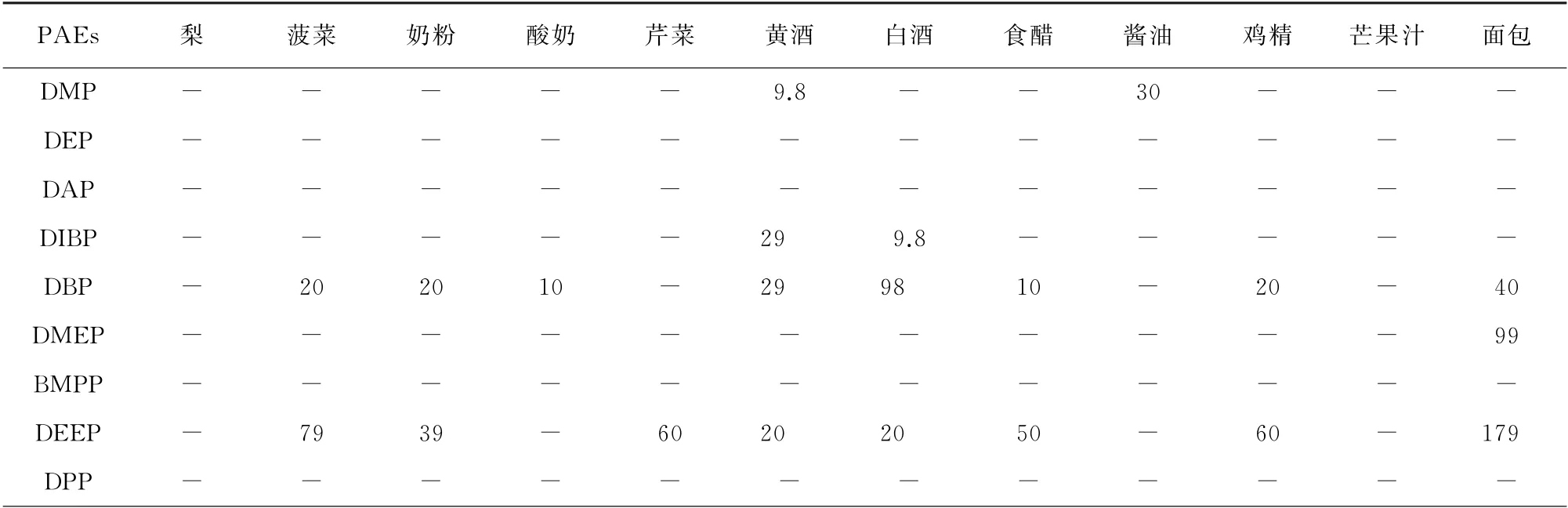
表5 样品分析结果Tab.5 Analytical results of samples μg·kg-1
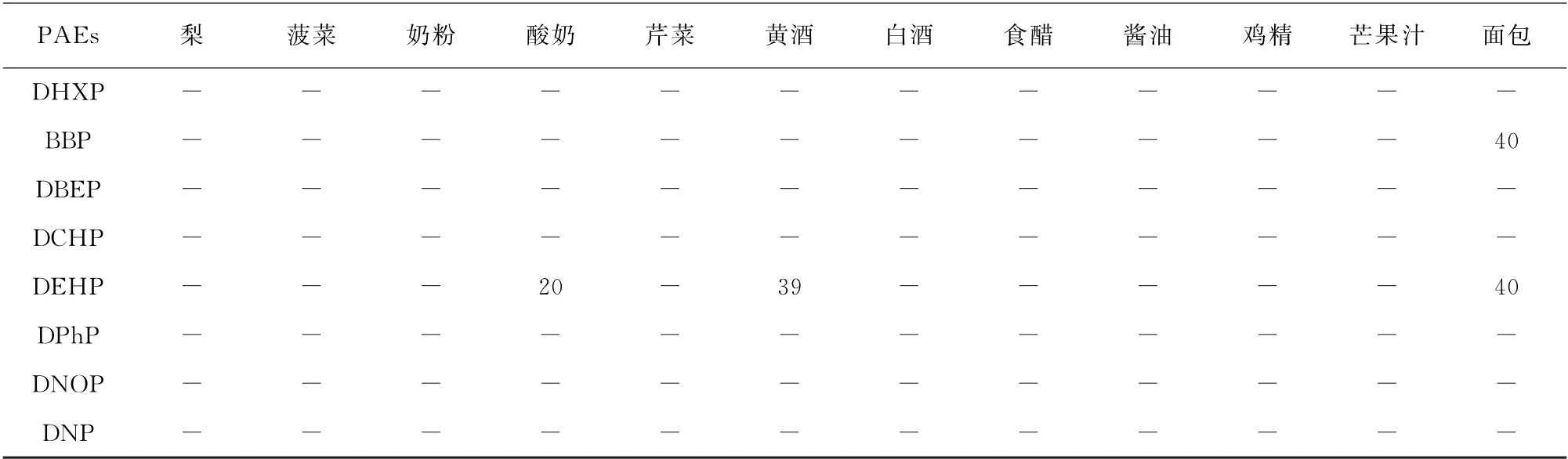
表5(续) μg·kg-1
蔬菜中检出PAEs大致可归因于土壤中存在PAEs,以及运输过程中使用塑料袋进行包装等。酒类、调味品等样品中检出PAEs可推测为产品生产过程中接触到塑料制品,亦或原料中带入等。面包、乳制品中检出PAEs可能归因于产品的塑料包装以及生产过程中接触等。

