冷冻切片包埋仪在组织冷冻制片中的应用效果观察
翁丹枫,骆慧颖,蔡伟栋,黎三艳,李国平
冷冻切片是在低温条件下使组织迅速冻结到一定硬度后进行切片的一种方法,目前广泛应用于术中病理诊断[1]。高质量且快速的冷冻制片病理学检查能够缩短术中等待时间,帮助临床医师在手术过程中尽快决定手术方案。本实验通过比较3种不同冷冻方法下的冷冻制片速度和质量,探究一种新的速冻包埋法的冷冻制片质量效果,现介绍如下。
1 材料与方法
1.1 标本收集福建医科大学实验动物中心存档的小白鼠肺、肝、肾、脑组织各25例,合计100例,以及福建医科大学附属第一医院存档的子宫肌瘤及甲状腺标本各20例,合计40例。
1.2 仪器与试剂Chaser冷冻包埋仪(江苏无锡启盛实验设备公司),冷冻锤,Thermo Fisher Linistat直线型自动染色机,Thermo切片机,OCT包埋剂,AAF混合固定液,HE染液,乙醇,二甲苯等。
1.3 方法小鼠采用颈椎脱臼法处死后,取小鼠肺、肝、肾、脑组织。小鼠及人标本组织平均分为3份,分别采用不同方法包埋:(1)速冻台冷冻法:组织放入预冷的组织托上加适量的OCT胶后放入冷冻箱速冻台上进行速冻;(2)冷冻锤速冻法:将组织放在预冷的组织托上后放至速冻点,加入适量OCT胶,待底部变白且表面未凝固时立即加盖冷冻锤速冻,注意保持冷冻锤水平;(3)包埋仪速冻法:冷冻包埋仪凹槽里先加少许OCT胶后将组织放入槽内,然后继续把胶填满包埋槽,最后将组织托朝下进行包埋,速冻时间设置为30 s,之后取出放入冷冻机进行切片。
1.4 HE染色与结果判定组织经三种不同冷冻方式包埋切片后,经AAF固定液固定1 min,然后放入自动染色机进行HE染色、封固。冷冻切片质量评分等级标准:甲级片(优)90分以上、乙级片(良)80~89分、丙级片(合格)60~79分,丁级片(不合格)低于60分。甲级、乙级片定义为质量佳者,丙级、丁级片定义为质量不佳者。
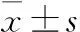
2 结果
2.1 不同冷冻方式制片时间的比较单因素方差分析结果表明,在小鼠肺、肝、肾、脑组织及人子宫肌瘤、甲状腺组织中,包埋仪速冻法组织制片时间明显短于冷冻锤速冻法(P<0.001)和速冻台冷冻法,差异有显著性(P<0.001);冷冻锤速冻法与速冻台冷冻法之间的制片时间差异无显著性(P=0.861,表1)。

表1 不同冷冻方法组织制片时间
#A组与B组比较;*B组与C组比较;△A组与C组比较
2.2 不同冷冻方式制片HE染色质量的比较在小鼠及人标本中,包埋仪速冻法制片质量明显优于冷冻锤速冻法(P<0.001)和速冻台冷冻法(P<0.001)(表2)。镜下观察三种方式包埋制片的HE冰晶情况(图1、2),可见速冻台冷冻法包埋的组织内形成大量冰晶,细胞间出现不规则空隙,细胞被挤压收缩,结构变形;冷冻锤速冻法及包埋仪速冻法包埋的组织中冰晶较少,且结构完整、染色均匀。包埋仪速冻法小鼠及人的各组织冰晶形成量与冷冻锤速冻法相比差异无显著性(P>0.05,表3、4),与冷冻台速冻法相比差异有显著性(P<0.001)。此外,切片质量方面,包埋仪速冻法在小鼠脑(P=0.044)、肝(P=0.037)、肾(P=0.031)及人子宫肌瘤(P=0.005)、甲状腺(P=0.017)组织制片质量优于冷冻锤速冻法,差异有显著性。在固定与染色、外观方面,3种冷冻方法各组织HE染色质量差异无显著性(P>0.05)。

表2 不同冷冻方法组织制片质量
质量佳:≥80分;质量不佳:<80分
3 讨论
冷冻制片技术因其制片时间短、组织结构保存完好而成为术中病理诊断的首选检查方法,但冷冻制片易出现冰晶,导致组织裂隙、细胞形态变化,严重影响冷冻制片快速诊断准确性[2]。因此减少冰晶形成是术中冷冻制片的重要质量保证。本实验通过比较发现,与速动台冷冻法相比,冷冻包埋仪及冷冻锤速冻法可有效减少冰晶的产生,并且包埋仪速冻法明显缩短制片时间且制片质量明显好于冷冻锤速冻法及速冻台冷冻法,大大提高了制片质量及工作效率。
冰晶是缓慢冷冻过程中细胞内的水分子向细胞间疏松区域游离、聚集,然后凝结成冰。组织细胞内冰晶形成的区域无细胞结构,呈结晶样或不规则空隙,周围组织或细胞间隙扩大,组织结构呈不同程度破坏[3]。在冷冻切片冷冻的过程中形成冰晶主要有两个原因:(1)冷冻速率慢导致细胞内的水分子向细胞间疏松区域游离、聚集,然后凝结成冰;(2)样本周围水溶液的组成成分。使用高度专业化快速冷冻系统或者高渗溶液能够减少冰晶大小和密度[4]。蔗糖是一种化学惰性和亲水性溶质,可以干扰冰结晶过程中的氢键形成,控制冷冻样品的脆性[5]。将组织样本经20%~30%的梯度蔗糖溶液脱水至组织沉底可减少冰晶形成。但是,其应用于脑组织脱水时仍可形成较多、较大的冰晶,制片效果并不十分理想[6]。不同的组织可能需要不同的蔗糖浓度来获得相似的冷冻切片质量。另一方面,20%~30%蔗糖脱水法消耗时间通常需要12~24 h,而蔗糖浓度越高,溶液黏度越高,这可能会减慢样品的渗透率,无法满足术中快速病理诊断的需要。速冻可以阻止水分子游离,保持基质的匀质。组织冷冻速度决定了组织内冰晶形成的方式与数量[3]。

①A①B①C②A②B②C
图1小鼠肾标本不同冷冻方式制片HE质量比较:A.速冻台冷冻法;B.冷冻锤速冻法;C.包埋仪速冻法图2人子宫肌瘤不同冷冻方式制片HE质量比较:A.速冻台冷冻法;B.冷冻锤速冻法;C.包埋仪速冻法

表3 不同冷冻方法下小鼠组织的制片评分(min±s)
P1:A组与C组比较;P2:B组与C组比较
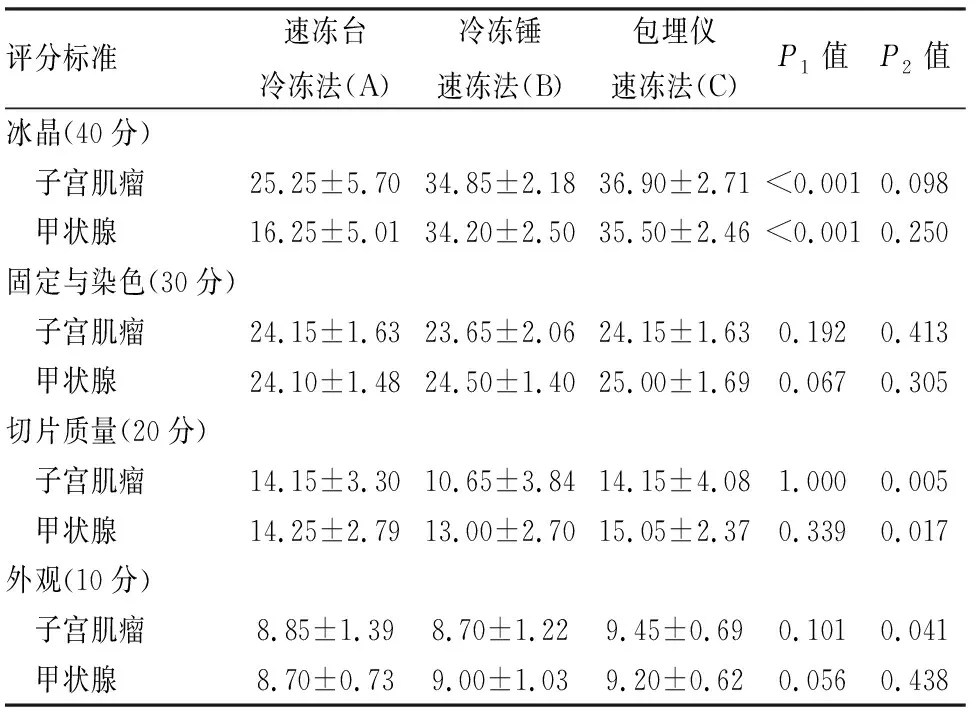
表4 不同冷冻方法下人组织的制片评分(min±s)
P1:A组与C组比较;P2:B组与C组比较
本科室使用的冷冻切片机箱内的温度一般控制在-20 ℃~-25 ℃,组织在速冻台冷冻的时间在5~8 min,冷冻速度缓慢,形成的冰晶较多;加上冷冻锤可使组织冷冻时间缩短至3~5 min,而Chaser冷冻包埋仪能在短时间内将箱室内的温度降至-80 ℃,工作温度一般设定为-40 ℃,可使组织在30 s内完成冷冻过程,快速越过冰晶形成期,极大地减少了冰晶的形成,其总制片时间比速冻台冷冻法及冷冻锤速冻法缩短了近5 min。相对于使用超低温的液氮冷冻法,冷冻包埋仪使用更安全,对操作人员没有伤害。虽然冷冻锤速冻法与包埋仪速冻法在冰晶形成方面差异无显著性,但是本实验结果表明,包埋仪速冻法甲级片或者乙级片的数量明显多于冷冻锤速冻法,主要表现在脑、肝、肾、子宫肌瘤及甲状腺组织的切片质量优于冷冻锤速冻法,主要原因是冷冻锤的冷冻时间主要靠肉眼判别,存在一定主观性差异,有可能在组织速冻的过程中过度冷冻,导致组织发脆,产生裂隙、皱褶及刀痕现象,影响了切片质量。而冷冻包埋仪具备定时功能,能够统一控制速冻时间及胶量,当冷冻时间结束后会发出提示音提醒开始制片,避免导致冷冻过度产生脆裂现象。而肺组织结构疏松,切片难度较大,两种速冻方法下的切片质量均较差,因此无明显差异。
综上所述,术中冷冻制片过程中,冷冻缓慢造成冰晶形成及组织裂隙产生对冷冻切片的质量及术中快速诊断的准确性有重要影响,而冷冻切片包埋仪能够达到速冻要求,可以有效减少冰晶的含量,提高冷冻制片的质量及工作效率,能够满足术中快速诊断的需要,值得在冷冻制片过程中推广使用。

