聚乳酸/海藻多糖电纺支架的制备工艺研究
张茜
(上海药明康德新药开发有限公司,上海 200131)
组织工程学经过33年的发展,已经成为一门研究开发生物活性替代物的专业学科。血管组织工程技术是利用血管细胞与可降解材料来构建血管替代物的一门技术,血管支架是血管组织工程的重中之重,静电纺丝法以其独特的技术为血管的修复和移植提供了一种新的选择。以玉米为主要原料的聚乳酸,具有良好的生物性能,且无毒性、可降解,可以广泛用于药理学研究及临床研究等方面。海藻多糖是一种水溶性多糖,易于人体吸收,生物活性强,且原料丰富易于提取。
1 材料与方法
1.1 试剂与仪器
海藻多糖,西安西海生物科技有限公司;聚乳酸,上海塑享贸易有限公司;明胶,上海山浦化工有限公司;草酸铵和EDTA-Na2为分析纯,兰州科器化玻有限公司;氯仿和无水乙醇为分析纯,天津市富宁精细化工有限公司;蒸馏水,兰州锋源纯净水有限公司;小鼠血清,兰州大学动物实验中心。
TJ-1000高压静电发生,天津大学现代科技有限公司;移液枪(10~1 000 μL),兰州博辉化玻仪器有限公司;IX71-A21PH光学显微镜,奥林巴斯;ES-2002H电子天平,长沙湘平科技发展有限公司;游标卡尺,兰州科器化玻有限公司;HH-4数显恒温水浴锅,国华电器有限公司。
1.2 实验方法
1.2.1 聚乳酸溶液的配制
取干燥洁净的烧杯,准确称取 0.6 g、0.8 g、1.0 g和1.2 g聚乳酸后,加入10 mL氯仿,密封、静置,溶解后搅拌至澄清,制得6%,8%,10%,12%不同浓度的聚乳酸溶液。
1.2.2 多糖明胶溶液的配制
多糖明胶溶液:准确称取 0.2 g、0.4 g、0.6 g、0.8 g和1.0 g多糖至洁净干燥的烧杯中,加入10 mL蒸馏水,配置成浓度为2%、4%、6%、8%和10%的多糖溶液,加热溶解,后准确称取7.0 g明胶,加入已溶解的多糖溶液中,加热振荡使溶解完全。
1.2.3 复合电纺支架的构建
静电纺装置见图1。由于多糖溶液和聚乳酸溶液互不相容,因此采用夹层静电纺丝方法,并以旋转的轴心来收集带电的聚合物射流形成的细丝,先在旋转轴上收集10%的聚乳酸形成纤维层,随后覆盖一层多糖纤维,然后继续收集聚乳酸纤维层,重复几次。
收集聚乳酸时采用自动装置,用1 mL的玻璃针管吸取不同浓度聚乳酸1 mL,用铁架台固定,使针管和地面竖直,调整接收距离为12 cm,高压静电发生器的电源电压设置为12 kV,收集装置接地,注射泵流速设为0.8 mL/h,开通电源。收集多糖时采用手推装置,用1 mL塑料针管吸取不同浓度多糖溶液,用铁架台固定,使针管和地面平行,接收距为10 cm,针头接15 kV的电压,收集装置接地,开通电源。改变接收距、电源电压和注射泵流速,构建不同参数下的复合电纺支架。

图1 聚乳酸静电纺装置(a)和多糖静电纺装置(b)
1.2.4 力学性能测定
(1)抗拉强度:从不同浓度的复合电纺支架上切取3段3.00 cm的支架,每段任意选择5点测其厚度,计算其平均值,即为厚度,计算横截面积;任取一段支架,一端固定,另一端用夹子固定在空的矿泉水瓶中,使整个装置垂直于地面,然后慢慢向矿泉水瓶中加水,直到细长条断裂,称量矿泉水的重量,计算出最大荷重,按照公式1计算抗拉强度。

(2)断裂伸长率:从不同浓度的复合支架上切取2.00 cm的支架,固定在游标卡尺上,适量拉伸,直到即将断裂,用游标卡尺计算出拉伸后的长度,按照公式2计算断裂伸长率。

(3)爆破强度:取最优工艺的电纺管状支架1 cm,铺成矩形,取紧邻6个点测最大爆破强度,然后用其堵住真空泵,打开真空泵,在压力表上读出数据,即为爆破强度。
1.2.5 血小板黏附性实验
(1)血液的稀释抗凝
无抗凝剂的新鲜血液,一段时间后会自动结块,无法用来测量血小板的黏附性实验。为了让血液保持完好且不影响血小板的形状,必须在新鲜的血液里添加抗凝剂。实验中选用草酸铵稀释液阻止血液凝固,稀释之后血小板形态清晰,便于观察。
草酸铵稀释液的配制方法为:准确秤取5.0 g草酸铵、0.06 g EDTA-Na2,加适量蒸馏水使其完全溶解;为除去溶液里面的杂质,用多层滤纸过滤2次,以防杂质干扰血小板的观察;然后把滤液定容至500 mL即可;密封好,保存在4 ℃的冰箱里备用。
取1.0 mL新鲜血液,加入配好的草酸铵稀释至10 mL,装入离心管中,总共取5管,存4 ℃冰箱备用。
(2)血小板黏附性实验
把原来稀释10倍的血液用移液枪取出5 mL置于10 mL离心管中,加2.5 mL草酸铵稀释液制得血液的15倍稀释液;然后用移液枪取200 μL置于计数板中,静置5 min后在光学显微镜的高倍镜下,观察血小板数并记录,得出黏附前血小板数目。
准备含有0%、2%、4%、6%、8%和10%多糖的聚乳酸复合电纺,用剪刀小心地剪取6段长度均为0.8 mm的电纺支架,并沿着管孔把血管支架剪开,形成一矩形即可。准备1个大培养皿和6个洁净干燥的小培养皿,分别编号1~6。把事先准备好的6段电放支架依次放入6个小培养皿,分别添加1 mL草酸铵稀释液,盖上盖子后放入大培养皿中,然后在恒温38 ℃水浴锅中孵育20 min。20 min后尽量倒干6个小培养皿中的稀释液,再向小培养皿各加500 μL的血液15倍稀释液。盖上盖子,在38 ℃水浴锅中保温40 min后取出,用镊子夹着电纺膜,小心缓慢地用500 μL草酸铵稀释液清洗掉电纺膜上的血液,清洗液合并到原来的小培养皿中,即血液由15倍变为30倍。然后用移液枪取200 μL小培养皿中的血液置计数板中,静置5 min后在光学显微镜的高倍镜下,观察血小板数,并记录数据,得出黏附后的血小板数目。按照公式3计算血小板的黏附率。

2 结果与分析
2.1 电纺工艺
2.1.1 聚乳酸和多糖的浓度
(1)聚乳酸浓度
实验发现,当聚乳酸含量过低时,溶液太稀,即使高压条件也无法形成纤维;含量过高时,溶液太黏,喷射液会堵塞针头,并且纤维过粗过硬。见表1,因此,最终将聚乳酸浓度设为10%。
(2)多糖浓度
在实验过程中,以不同浓度梯度(2%、4%、6%、8%和10%)的多糖溶液进行纺丝,发现不同浓度的多糖都能形成电纺纤维。因此,多糖浓度并不是影响电纺纤维的主要因素。
2.1.2 接收距
接收距能够影响纳米纤维形态的参数。实验中,在电场不被干扰的情况下,当接收距取值较小时,出丝效果不明显,呈液滴状态,很难形成纤维;当接收距过大,电纺产生的纤维难以集中于滚轴收集器上,在收集器的周围及电场外都有分布。通过实验,最终确定最优的聚乳酸接收距为12 cm,多糖接受距为13 cm。
2.1.3 电压
在其他因素一定的条件下,实验设定了电压分别为10 kV、15 kV和20 kV的电场。当电压为10 kV时,喷射流开始释放,却并不流畅,导致滚轴收集器形成的电纺纤维不够连续;电压升高至15 kV,滚轴收集器形成的电纺管状支架很理想;当电压继续升高至20 kV,电场强度的增大使得多次纺丝形成的纤维出现更多的缺陷。因此,电压取15 kV为宜。
2.1.4 纺丝液流速
相关研究表明,纺丝液流速是影响纤维形态的次级因素之一[17]。纺丝液流速和电压是两个互相作用的参数,其一值的变化会引起另一值的改变。考虑到电压的设定,流速也将随之调整。综合考虑所有参数,将聚乳酸纺丝液流速设定为3个值:0.2 mL/h、0.8 mL/h和1.0 mL/h。当流速太慢时,电纺过程中会产生小液珠滴落的现象,影响成丝效果;流速过快时,电纺产生的纤维会出现过多孔眼。因此,将聚乳酸纺丝液流速的优化值设定为0.8 mL/h。另外多糖明胶溶液纺丝时流速控制是关键,流速过快时,因转速一定,出丝量大,使得滚轴收集到的纤维丝缠绕得松散不紧密,最终导致纺出的管子强度不够;流速过慢时,针头易被堵塞,很难出丝。因此,多糖明胶纺丝液的流速优化值设定为4.8 mL/h,此条件下形成的电纺纤维形状较为完好。

表1 不同浓度聚乳酸纤维现象
2.2 力学性能
2.2.1 抗拉强度
由于静电纺丝的原理和方法相同,测得平均厚度均为0.042 cm,则原横截面积为s=0.5×0.042=0.021 cm2(g=9.8 N/kg,1 N/cm2=1 Pa=10-3kPa)。不同多糖浓度的电纺支架抗拉强度结果见表2。当厚度一定,即横截面积不变时,随着多糖浓度的增加,抗拉强度呈上升趋势。
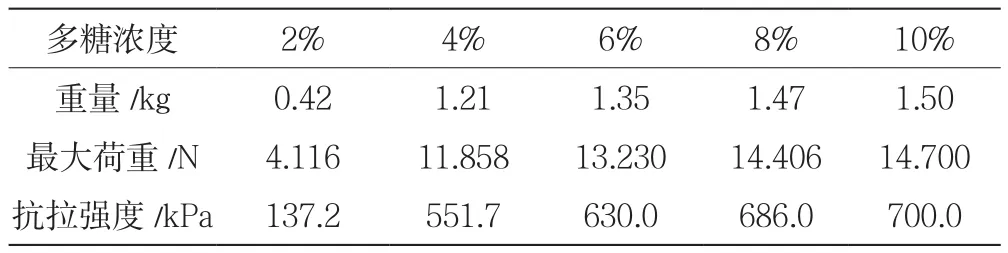
表2 不同多糖浓度的电纺支架的抗拉强度
2.2.2 断裂伸长率
在实验过程中,所截取的细长条长度均为2.00 cm,即拉伸前长度为2.00 cm。不同多糖浓度的电纺支架的断裂强度见表3。当厚度一定,即横截面积不变时,随着多糖浓度的增加,断裂伸长率基本在30%附近波动。
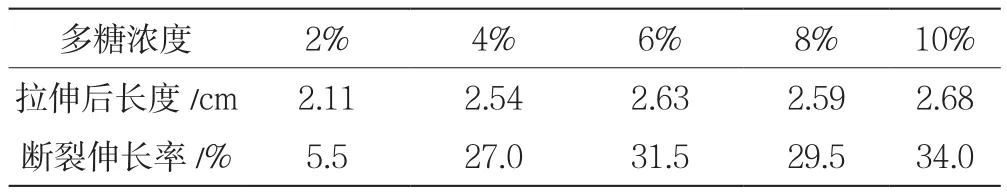
表3 不同多糖浓度的电纺支架的断裂强度
2.2.3 爆破强度
取聚乳酸浓度为10%、接收距离为12 cm、电压为12 kV、纺丝液流速为0.8 mL/h;海藻多糖明胶溶液静电纺丝接受距离为10 cm、电压为15 kV、流速为4.8 mL/h时的电纺管状支架1.0 cm,铺成矩形,取紧邻6个点测最大爆破强度,真空泵压力表上的读数分别为0.050 MPa、0.046 MPa、0.052 MPa、0.050 MPa、0.048 MPa和 0.046 MPa,取平均值为0.048 MPa。这一数值远远超过了人体血管所能承受的压力。
2.2.4 血小板粘附实验
15倍血液黏附前的血小板总数取3次平行测定结果的平均值,结果为127.66。不同多糖浓度的电纺支架血小板黏附率如表4所示。随多糖浓度升高,电纺支架的粘附率逐渐减小,而表中6%多糖浓度的血管支架的粘附率出现偏差,可能是纺丝过程中出现误差,或者是测血小板粘附性时,育孵、显微镜计数板读数时产生读数误差,使得该浓度下的粘附率出现偏高。但8%、10%浓度支架的粘附率均低于2%、4%的支架的粘附率,总体上血管支架的粘附率随多糖浓度的升高而降低,10%聚乳酸的电纺支架在相同条件下未添加多糖时对血小板的黏附率最高。
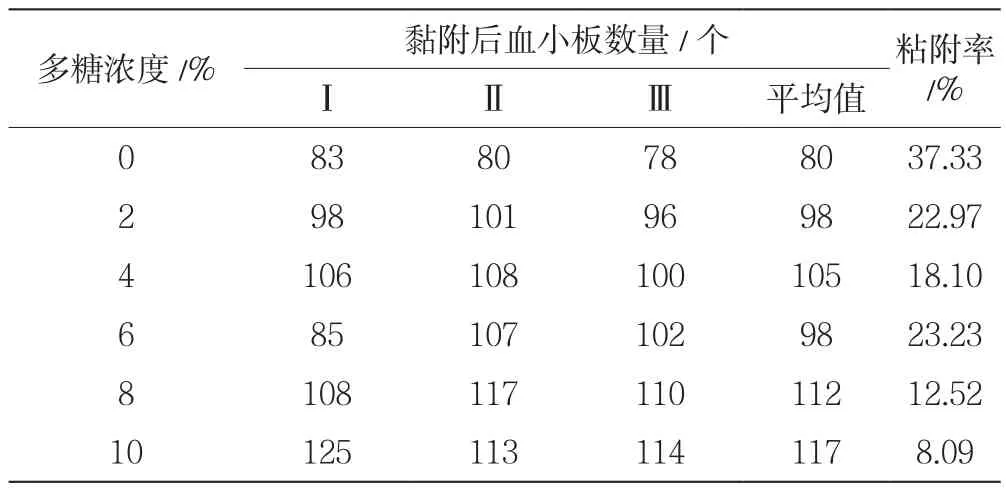
表4 不同多糖浓度的电纺支架血小板粘附率
3 讨论
实验中构建电纺支架时,如果聚乳酸的溶解时间过长,造成氯仿挥发过多,会使得聚乳酸的浓度过大,流速减慢,容易使针头堵塞,纺出的电纺管状支架过硬过脆,无法达到预期要求;纺聚乳酸时,利用重力场作用,若转轴的接收距离控制不好,会造成纺出的丝很难接收,通过改进,在重力场和电场力的同时作用下,聚乳酸溶液可以顺利出丝,成丝效果很理想;纺多糖时采用手推法,流速控制不好会使得喷出的丝粗细不均匀,且时间掌握不好针头容易堵塞,通过对装置改进并熟练操作过程,可以使得纺出的电纺支架韧性、柔软性都很好。
正常情况下,人体股动脉理论抗拉强度为0.7~1.0 MPa,理论断裂伸长率36%~46%。现阶段使用的人造血管,是由膨体聚四氟乙烯材料制成,其抗拉强度为0.6~1.5 MPa,断裂伸长率为20%~30%。实验制备的复合电纺支架在多糖浓度为10%时,更接近人体股动脉的抗拉强度。多糖浓度为4%、6%、8%时,复合电纺管状支架的断裂伸长率接近正常人体股动脉的断裂伸长率。因此,当聚乳酸浓度为10%,多糖浓度为10%时,复合电纺人造血管的抗拉强度和断裂伸长率均高于或接近人体血管,抗拉强度和断裂生长率符合移植的基本要求。另外,复合电纺的爆破强度也是主要影响因素,人体在正常静息状态下的血压值收缩压不超过140 mmHg,舒张压不超过90 mmHg,隐静脉承受的最大压力为(1 680±307)mmHg,约合(223.0±40.8)kPa。实验过程中所得到的爆破强度值为483 kPa,符合要求。因此复合管装支架的力学性能接近人造血管。
本实验中,通过加入海藻多糖明显改善了纯PLA的血液相容性,能够更好地抑制血小板的黏附,即在纯PLA中加入海藻多糖后,复合电纺材料的抗黏附率更好。另外,海藻多糖的加入改变了复合电纺材料的表面电荷和和化学结构,同时由于硫酸根基团与硫酸纤维素钠的抗凝血活性的影响,使得加了海藻多糖后的复合材料具有良好的血液相容性。
4 结论
采用复合管状支架的静电纺丝法,以高速旋转的轴心收集带电的聚合物射流形成的细丝,成功构建了PLA/海藻多糖复合电纺管状支架。随着多糖的加入,复合电纺管状支架的韧性增加,断裂伸长率基本维持在一定的范围内,血小板粘附性整体呈下降趋势。说明材料的血液相容性得到了明显的改善。浓度为10%聚乳酸、10%多糖的复合电纺管状支架的爆破强度超过人体血管所承受的最大压力,且血小板粘附率最低,可作为血管移植工程的人造血管。

