3.0T多参数MRI在直肠癌术前评估中的价值
饶慧敏,梁玉玉,何维恒,哈若水
在2018年全球新增的1 810万癌症患者中结直肠癌占到10.2%,位于第三位,在我国结直肠癌新发病例及死亡病例均位于第四位。结直肠癌中直肠癌约占60%[1],严重威胁着我国人民健康和生活质量。随着临床诊疗方式的改进,新辅助放化疗及全直肠系膜切除术(TME) 广泛应用于临床,患者的预后明显改善。2017版欧洲肿瘤学会(EMSO)基于肿瘤位置(距肛缘距离)、T分期、N分期、肠壁外血管侵犯(EMVI)和直肠癌术后环周切缘(CRM)等因素对直肠癌的局部复发风险进行分级,依此选择不同的治疗模式[2],使患者得到个体化的精准治疗。磁共振成像是直肠癌TNM分期的主要影像学检查之一,尤其是高分辨率小视野扫描可以清楚地显示直肠壁各层,HR-MRI是采用小视野、薄层、垂直或平行于肠管长轴扫描的T2WI成像,是国外临床患者术前常规检查方式[3-4]。常规核磁影像与功能影像相联合对直肠癌术前评估有着重要价值。本研究就3.0T多参数磁共振在直肠癌术前T、N分期、肠壁外血管侵犯及环周切缘术前评估的价值进行讨论。
1 资料与方法
1.1 一般资料:选取2016年8月-2018年11月在我院行肠镜检查并取得病理结果的直肠癌患者80例,所有患者均为腺癌,其中男性43例,女性37例,中位年龄66.5岁。患者均在术前1周内行直肠MRI检查。排除标准:①有前列腺增生及心脏病、青光眼等山莨菪碱(654-2)禁忌证;②术前做过放化疗;③MRI图像质量不好或数据不完整,无法进行诊断;④患者肿瘤未切除,仅行姑息治疗;⑤术后病理T分期、N分期、CRM及EMVI结果完整。
1.2 MRI检查技术:患者于检查前2 d 进流质饮食,检查前夜晚餐后1 h 口服缓泻剂复方聚乙二醇电解质散剂,将1大包内3小袋中规格Ⅰ(68.56 g/袋)溶于1 L 水,规格Ⅱ(137.15 g/袋)溶于2 L 水中,分3 h 服完(检查当日晨起空腹)。检查前约12 min肌肉注射东莨菪碱20 mg,抑制肠管蠕动。采用飞利浦全数字核磁共振 3.0T Ingenia进行扫描,用飞利浦Extended Brilliance Workspace(EBW)图像后处理工作站来分析图像。扫描序列:①矢状位T2WI,视野(FOV)26 cm×22 cm,矩阵324×249,TR/TE 3 400 ms/100 ms,NAS 1次,层厚3 mm,层间距0.3 mm。②轴位T2WI通过矢状位图像定位,垂直病变肠管,视野(FOV)16 cm×16 cm,矩阵200×143,TR/TE 3940 ms/100 ms,NAS 2次,层厚3 mm,层间距0.3 mm。③轴位T1WI,视野(FOV)30 cm×30 cm,矩阵200×176,TR/TE 535 ms/8 ms,NAS 1次,层厚3 mm,层间距0.3 mm。④DWI成像,视野(FOV)30 cm×30 cm,矩阵104×121,TR/TE 4 000 ms/8 ms,NAS 1次,层厚3 mm,层间距0.3 mm,B值为0,800。动态增强扫描应用的对比剂为钆双胺,剂量0.1 mmol/kg,5 s内快速静脉注射完,扫描所用序列为T1高分辨力各向同性容积激发(e-THRIVE)。
1.3 图像评价:直肠癌T分期、N分期依据第7版美国癌症联合委员会(AJCC)指南,由2位多年从事腹部MRI诊断的影像医师分别评价,意见不一致时由主任医师参与,共同讨论、协商达成一致意见。观察直肠病变位置,与覆膜返折关系,病灶距肛门的距离,病变横径、纵径、累及肠管长度,侵及直肠系膜、直肠系膜筋膜、骶前筋膜、肛门括约肌、肛提肌是否累计,脉管是否侵及,直肠系膜内及周围是否有癌结节,淋巴结大小、形态、内部信号、DWI及动态增强扫描特点,腹股沟区淋巴结以及骨盆骨质信号。评价标准:①T分期,T1指肿瘤仅局限在黏膜及黏膜下层;T2指肿瘤侵犯至肌层;T3指肿瘤超过肌层到达浆膜层(覆膜返折以上)或进入直肠系膜(覆膜反折以下);T4又分为T4a及T4b期,肿瘤直穿破直肠系膜筋膜(腹膜返折以下)或侵透浆膜层(腹膜返折以上)为T4a,侵犯周围器官或结构为T4b期。②N分期,N0是指区域内淋巴结未见转移;N1指有1~3个区域内巴结转移;N2指4个及以上肠周淋巴结转移,其中对于髂血管旁淋巴结需要重点指出,因为它在TME手术范围之外;另外,腹股沟区肿大的淋巴结分期属于M期,也需要单独列出,手术范围亦需要扩大。③环周切缘,是指肿瘤外缘距离直肠系膜筋膜之间的最短长度。在PACS工作站测量肿瘤最外缘或者瘤结节以及转移淋巴结距离直肠系膜筋膜的最短距离。MRI横断面连续扫描中肿瘤组织或转移淋巴结距离盆筋膜脏层的距离≤1 mm[5]称之为环周切缘阳性。④肿瘤周边血管(EMVI)是指壁外血管侵犯,即胃肠道肿瘤所在肠管固有肌层外的血管腔内被原发肿瘤直接侵入。在高分辨率T2WI上当流空现象消失,血管管腔扩大且轮廓不规则时可诊断为EMVI 阳性[6]。
1.4 统计学方法:采用SPSS 17.0统计软件,对直肠癌MRI T分期结果与术后病理T分期结果进行Kappa诊断一致性检验(Kappa检验中K系数越大,吻合度越高,K≥0.7表示吻合度较强,0.4~0.7表示吻合度一般,K<0.4表示吻合度弱)。
2 结果
2.1 直肠癌MRI的一般情况:形态不规则肿块在T1WI呈等、稍低信号,T2WI呈高信号及混杂稍高信号,DWI呈高信号,注入对比剂后呈不均匀强化,强化曲线多为廓清型。上段直肠癌34例,中段直肠癌38例,下段直肠癌8例。肿块矢状位最大长径5.3 cm,肿块轴位最大长径1.63 cm。肿瘤最长径为1.2~7.3 cm。
2.2 直肠癌MRI分期与病理:MRI正确T分期71例,错误分期9例,包括过低分期5例,过高分期4例。MRI对80例直肠癌T分期判断与病理对照结果见表1。MRI对直肠癌术前T分期的总准确性为88.8%(71/80),其中各分期的诊断准确率、敏感性、特异性、阳性预测值结果见表2。N分期总的准确性为81.25%(65/80),7例过高分期,8例过低分期,阳性预测值为70.83%,敏感度为68%,特异度为87.27%,准确度为81.25%。病理组织学结果显示CRM(+)10例,CRM(-)70例;MRI能正确判定其中的77例,2例CRM(-)术前误认为CRM(+),1例CRM(+)术前误认为CRM(-)。多参数MRI对CRM判定的敏感度为83.33%,特异度为98.59%,阳性预测值为90.90%,准确度为96.25%。病理组织学结果显示EMVI(+)10例,EMVR(-)70例,MRI能正确判定其中70例,有6例EMVI(-)术前误认为EMVI(+),有4例EMVI(+)术前误认为(-)。

表1 直肠癌MRI T分期和术后病理结果比较(n=80)
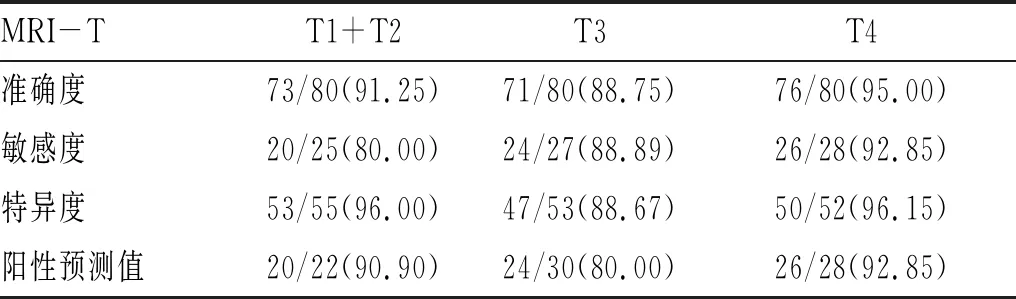
表2 MRI诊断直肠癌T分期结果[n(%)]
3 讨论
3.1 直肠MRI检查技术
3.1.1 检查前准备:在直肠MRI检查技术成熟前的探索阶段,笔者对患者肠道还进行过清洁肠道后灌注生理盐水,这种方式会使得肠壁变薄,同时生理盐水极易与残存气体间形成气液平面,进而产生磁化率伪影,同时还造成肠蠕动的增加,对观察肠壁各层结构及肿瘤的浸润深度造成困扰。因此本组病例均在检查前2 d 进低渣饮食,前一晚服用清肠药,检查前10~15 min注射20 mL东莨菪碱,以减少肠道蠕动。在少量生理性渗液的衬托下可以清楚地显示病变及肠壁的黏膜、黏膜下层及肌层,有助于观察病变位置、范围及肿瘤侵犯深度。
3.1.2 扫描方位、序列的选择:MRI有良好的软组织分辨率,同时可以采用多参数、多方位成像。笔者单位选择序列有高分辨率T2WI,垂直于病变段直肠长轴的斜横断位、斜冠状位扫描,以真正显示肿瘤的切面,避免由于直肠(尤其是上段)走行迂曲所致的误判,同时还采用了DWI及动态增强等功能成像。文献报道[7-10],高分辨率T2WI结合DWI及动态增强扫描序列对直肠癌的局部T、N分期及CRM、EMVI是否受侵具有重要价值。
3.2 MRI评估T分期:高分辨率T2WI上,黏膜为低信号、黏膜下层为高信号、肌层为低信号,直肠系膜表现为高信号,直肠系膜筋膜及腹膜返折表现为低信号。在T1期表现为低信号的黏膜及(或)高信号黏膜下层受累;T2期病变侵及低信号肌层,且肌层低信号连续,肌层外缘光整,DWI上未见结节状、粗条状突起,肠管周围脂肪间隙清晰; T3期腹膜返折以下病变为累及并穿透肌层,肌层低信号中断,肌层外缘毛糙,见结节状突起向周围延伸,腹膜返折以上病变肠管外缘光整,未见突出结节及粗条影;T4a期病变累及浆膜或直肠系膜筋膜,CRM为阳性,T4b为病变侵及邻近器官。在临床工作中,T1和T2期病变的治疗原则和手术方案基本相同,所以本研究将T1期和T2期合并为T1~T2期,代表未突破直肠肌层组。T2、T3期的鉴别在临床上尤为重要,本研究有2例T2期高估为T3期,有3例T3期被低估为T2期。笔者认为区分关键在于观察固有肌层连续性是否存在,直肠周围的脂肪间隙是否清晰,同时要注意确认病变周边条索影是肿瘤侵润还是炎症、纤维条索还是血管,DWI及动态增强扫描序列结合高分辨T2WI对肿瘤肌层是否为断续显示更有价值。同时,DWI及动态增强可以观察病变外缘是否光整对鉴别有价值。对于T4期病变MRI有较高的诊断率,本研究诊断的准确度为95%,收集的 28例患者中有2例均被低估分期,均为腹膜返折以上病变,突破浆膜面,鉴别较为困难。
3.3 MRI评估N分期:单纯以淋巴结大小作为有无转移的主要依据外,其准确性和特异性均较低。正常淋巴结轮廓光滑,类似肾形,其内见淋巴门,周边在T2WI上常可见化学位移伪影(淋巴结周边见一圈明暗带)。文献报道[11]以淋巴结短径≥5 mm,形态不规则,内部信号不均匀,其内可见囊变、坏死等特点综合评估淋巴结有无转移。MRI在鉴别转移性淋巴结及直肠周围癌肿结节困难,使得分期准确度降低。本研究应用淋巴结短径>5 mm,且淋巴结的轮廓不规则、边界不清或内部有坏死,同时结合DWI的信号及动态增强特征作为判断标准。N分期总的准确性为81.25%(65/80),阳性预测值为70.83%,敏感度为68%,特异度为87.27%,准确度为81.25%,与文献报道接近[7]。所以,笔者认为既往单采用高分辨率T2WI来诊断是否为淋巴结转移存在局限性。
3.4 MRI评估肠壁外血管侵犯:肠壁外血管侵犯(EMVI)指肿瘤细胞侵犯固有肌层以外的脉管系统,是在直肠壁肌层外的静脉或动脉内存在癌细胞或组织,肿瘤浸润到腔外血管可能会为肿瘤细胞提供一个血行转移途径,是局部复发、远处转移和总生存期的不良预后指标。病理对EMVI评价时,是将脉管侵犯作为EMVI阳性,但脉管包括血管和淋巴管,在常规HE染色中,受限于切片大小、固定后血管萎缩等因素影响,区别淋巴管和血管是非常困难的,所以病理诊断EMVI 有其局限性[12]。
MRI对EMVI有5 级评分标准(0~4级),0分:肿瘤侵犯肌层的形态不呈结节形,而且肿瘤侵犯区域无血管相邻;1分:最小的壁外侵犯呈串状或结节状,但是附近没有血管结构;2分:壁外血管附近有串状肿瘤,但是血管管径正常,血管内没有明确肿瘤信号;3分:管腔内可见中等信号强度,血管廓轮和管径轻度扩张;4分:管腔轮廓不规整或者肿瘤呈结节状侵犯血管。当评分为3级和4级时可诊断为EMVI阳性[13]。本研究8例患者有脉管受侵,但病理上仅有4例确诊,这种差异有待进一步研究。
3.5 MRI评估环周切缘:直肠癌术后环周切缘(CRM)是指将整个直肠肿瘤和直肠系膜沿冠状面连续切片,观察其整个周边切缘是否有肿瘤侵犯,是评价TME手术效果的重要指标。病理学镜下病变距离直肠系膜筋膜<1 mm为CRM阳性。MRI图像中肿瘤距离直肠系膜筋膜>1 mm可以保证CRM阴性,肿瘤距离直肠系膜筋膜最近的距离,包括淋巴结,即如果直肠系膜内高度可疑为转移的淋巴结,其与直肠系膜筋膜距离小于肿瘤距离直肠系膜筋膜距离,则测量淋巴结到直肠系膜筋膜的距离[13]。本研究证实多参数MRI对CRM判定的准确度为96.25%,有较高的使用价值。
总之,3.0T多参数MRI使用高分辨率T2WI、常规T1WI以及功能成像DWI、动态增强扫描,能够清晰显示直肠壁各层、肛提肌、直肠系膜、直肠系膜筋膜、腹膜返折、瘤周脉管等结构,对直肠癌术前分期准确性较高,能够为直肠癌的个体化精准治疗提供准确的影像学依据。

