锂离子电池正极材料磷酸铁锂的研究进展
王甲泰,赵 段,马莲花,张彩虹
(青海师范大学物理与电子信息工程学院,青海西宁810000)
具有橄榄石结构的磷酸盐正极材料LiFePO4自从被发现以来,由于具有热稳定、环境友好、价廉、较高理论容量(170 mA·h/g)、工作电压较高(3.4 V)及循环性能较好等多种优势而成为最有发展潜力的锂离子二次电池(特别是能够用于动力型电源的)正极材料[1]。 但橄榄石型LiFePO4正极材料的自身电导率差及较低的锂离子扩散系数, 限制了LiFePO4材料的更广泛的应用[2-5]。为了解决其电导率及离子扩散系数较低的问题, 目前有大量的文献对LiFePO4进行了研究,其改进方法总结起来主 要有3 类[2-5]:1)对LiFePO4进行表面改性,例如包覆碳材料来改进其导电性;2)对LiFePO4进行掺杂,例如掺杂Ti4+、Co2+、Zn2+、Mn2+等离子来改进其电化学性能;3)制备亚微米或纳米级的LiFePO4, 或制备特殊形貌的LiFePO4来改进其电化学性能。 本文主要对近年来上述3 种LiFePO4改进方法的研究状况进行综述,说明各自改进方法的优缺点。
1 LiFePO4 的基本性质
1.1 LiFePO4 的基本结构
LiFePO4为有序的橄榄石结构,属于正交晶系,在晶体结构中氧原子以稍微扭曲的六方紧密堆积的方式排列。 Fe 与Li 分别位于氧原子八面体中心4c和4a 位置,形成了FeO6和LiO6八面体。P 占据了氧原子四面体4c 位置,形成了PO4四面体。 其晶胞参数a=0.600 8 nm,b=1.032 4 nm,c=0.469 4 nm。 LiFePO4的结构示意图如图1 所示[6]。
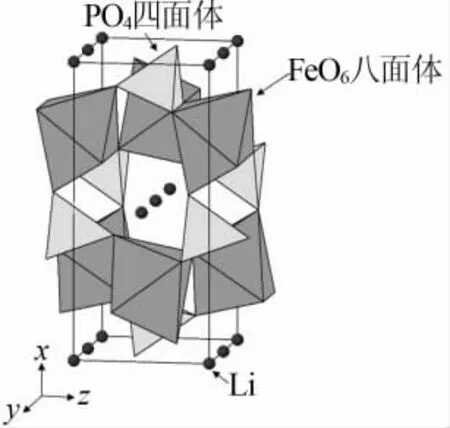
图1 LiFePO4 的结构示意图[6]
1.2 LiFePO4 的电化学反应原理
LiFePO4正极材料的理论电化学比容量为170 mA·h/g,相对金属锂的电极电位约为3.45 V,理论能量密度为550 W·h/kg[1]。LiFePO4电池充放电是在LiFePO4与FePO4两相之间进行,由于LiFePO4与FePO4的结构相似,所以LiFePO4具有较好的循环稳定性,在充放电过程中,体积变化约为6.81%[1]。
锂电池充电时,Li+从正极脱出,经过电解液、隔膜,迁移到负极,此时负极处于富锂状态。 锂离子从正极脱出后,正极的LiFePO4转化为磷酸铁。放电过程正好相反[1],其充放电化学反应式可表示成式(1)和式(2):

2 改性LiFePO4 的电化学性能研究
对LiFePO4的改性,主要是利用碳材料(活性炭、碳纳米管、碳纤维、石墨烯等)进行表面修饰或掺杂,利用Ti4+、Co2+、Zn2+、Mn2+、N3+、F-等离子进行锂位掺杂、铁位掺杂或氧位掺杂来改进其电化学性能。
2.1 碳材料改进LiFePO4 的电化学性能研究
因为碳材料有优良的电导率, 通过将正极材料LiFePO4与活性炭、介孔碳、纳米碳纤维(CNF)、多壁碳纳米管(MWCNTs)、石墨烯等进行复合,制备LiFePO4复合正极材料,可以有效地改善其循环、倍率等电化学性能[7-10]。
Y.Q.Qiao 等[7]利用商业碳纳米管,并利用聚乙烯吡咯烷酮(PVP)进行巧妙地包覆,最终经过一系列工艺与LiFePO4复合, 形成了碳纳米管包覆的LiFePO4纳米复合材料。 其中, 碳纳米管形成了3D网络结构, 有力地改进了LiFePO4的电导率和锂离子的扩散系数, 使得复合正极材料展现出了杰出的倍率性能和超长的循环寿命。 以10C 电流密度循环1 000 次之后,比容量约为123 mA·h/g,只损失了约1.6%的比容量,当循环到3 400 次时,比容量大约为100 mA·h/g,仍保持有80%的比容量,电化学性能非常优异。X.Tu 等[8]利用氮掺杂碳纳米管,也成功地改进了LiFePO4的电化学性能。
R.A.Susantyoko 等[9]利 用MWCNT 取代了常用的集流体铝箔,重新设计了正极结构,形成了MWCNT-LiFePO4正极材料,成功地改进了LiFePO4的比容量。 当添加10%MWCNT 的LiFePO4材料以较低的电流密度(17 mA/g)放电时,其比容量达到了144.9 mA·h/g,当以较大的电流密度(170 mA/g)循环100 次之后,其比容量仍然约为126.7 mA·h/g,有效地提高了LiFePO4的电化学性能。
Y.Zhang 等[10]以蔗糖作为碳源,通过溶胶 凝胶法合成了活性炭包覆的颗粒尺寸为1~2 μm 的不规则球形的LiFePO4正极材料, 电化学性能测试表明,当放电电流密度为0.1C 时,其比容量达到了163.5 mA·h/g,经过110 次循环,其比容量保持率为91.1%(149.0 mA·h/g),并且具有良好的倍率性能,相比商业用LiFePO4,其电化学性能得到了很大提升。 G.Wu 等[11]合成的LiFePO4/C 复合材料,表现出良好的低温性能,在-20 ℃,其比容量提高了20%。文献[12-16]报道了活性炭包覆或者氮掺杂的活性炭碳包覆, 都能够一定程度上提高LiFePO4的电化学性能。
石墨烯具有优异的性能, 经常用来改进锂电池正负极材料的电化学性能。Y.Guan 等[17]利用商业石墨烯, 制备了LiFePO4与活性炭及石墨烯的复合正极材料,表现出优异的倍率性能。 以100C 电流密度放电时,其比容量达到了66 mA·h/g,经过3 000 次的循环,其比容量仍然保持在82%,结构相当稳定。同课题组制备的3D 结构LiFePO4石墨烯复合材料,也表现出优异的倍率性能,分别以30C 和50C 电流密度放电时,其比容量达到了112.4 mA·h/g 和96.7 mA·h/g,并且在30C 电流密度下,经过300 次的循环,其比容量保持率为96.3%[18]。 文献[19-21]报道了直接用石墨烯或者氮掺杂石墨烯等改进LiFePO4的电化学性能,都有效地提高了LiFePO4的循环性能或倍率性能。
以上分析可见,利用碳材料尤其利用石墨烯改进LiFePO4的电化学性能,是行之有效的途径,但是碳材料的应用,也会一定程度上降低材料振实密度,并且存在制备过程较为复杂的问题,期待进一步的研究。
2.2 掺杂改进LiFePO4 的电化学性能研究
掺杂是改善材料电导率的常用方法, 指在LiFePO4晶格中掺杂一些导电性好的金属离子或非金属元素,改变LiFePO4晶粒尺寸,形成空穴等晶格缺陷,提高其电导率及锂离子的扩散速率,最终提高LiFePO4材料的电化学性能, 掺杂主要有锂位掺杂和铁位掺杂[22]。
LiFePO4晶体结构中添加碳能阻止Fe2+在反应过程中被氧化, 抑制了在结晶过程中微晶的快速生长,从而能提高材料的电导率。掺杂主要是指在包覆碳层的LiFePO4/C 晶格中掺杂某些导电性好的离子,造成材料的晶格产生缺陷,从而促进Li+扩散,改善晶体内部的导电性能。 LiFePO4/C 的缺陷主要包括:锂离子的缺位、铁位缺陷、氧位替代等。根据S.Y.Chung 等[3]提出的第一性原理,在LiFePO4/C 中,如果O 被F 取代,将会有最低的禁带宽度,其次是Mn取代Fe 或者Na 取代Li,故合适的离子取代可以提高LiFePO4/C 的电化学性能。 原因是,LiFePO4/C 是一种半导体,导带与价带之间的能级宽度约为0.13 eV,在电池的充放电过程中,Fe3+/Fe2+共存的混合价态结构的比例会发生改变, 使得LiFePO4/C 晶体也在P型与N 型之间发生变化。在充电过程中,P 型的成分增加,而在放电时,恰好相反。 单独的Fe2+和Fe3+的导电性都比较差, 金属离子掺杂通过在LiFePO4/C的禁带中间引入掺杂能级可以降低导带和价带间的禁带宽度,并通过掺杂金属离子可以造成LiFePO4/C晶格缺陷,使得空穴迁移率大于电子迁移率,从而提高其导电性和锂离子的扩散速率[3,22]。
早在2002 年,S.Y.Chung 等[3]对LiFePO4进行了Mg2+、Al3+、Ti4+、Zr4+、Nb5+及W6+等金属离子掺杂,大大提高了LiFePO4的电导率, 其电导率甚至超过了常用的锂电池正极材料LiCoO2和LiMn2O4, 引起了广泛关注。在此之后,很多科学家致力于通过掺杂来提高LiFePO4的电化学性能[5,23-26]。
Z.H.Wang 等[5]发现LiFePO4掺杂Na+时,可以抑制Li4P2O7相的出现,但是Li3PO4相会增加,说明一定的非化学计量比的Na+掺杂, 有利于控制杂相的产生, 进而可以优化LiFePO4正极材料的电化学性能。 优化实验程序,发现当掺杂1%的Na+时,经过200 次循环充放电,其比容量仍然为142 mA·h/g,只衰减了1.3%。A.R.Madram 等[27]研究了Na+和K+共同掺杂的LiFePO4,发现比容量有所提高。
谷和云等[23]通过简单水热反应制备LiFePO4前驱体,并结合后期热处理过程制备了镁离子掺杂碳包覆的LiFePO4正极材料。性能测试结果表明,镁离子掺杂后的LiFePO4材料具有较高的放电比容量(0.1C 放电比容量为160.1 mA·h/g)和优越的倍率性能(20C 放电比容量为77.2 mA·h/g),同时减小了极化和电荷迁移电阻。
J.M.Zhu 等[28]利用Cu+掺杂LiFePO4,发现Cu+能够占据铁位,有利于减小颗粒尺寸及稳定LiFePO4的结构。在以0.2C 放电时,其首次比容量为148.8mA·h/g,经过50 次的循环,其比容量为149.8 mA·h/g,循环性能可谓相当的稳定。
虽然通过掺杂来提高LiFePO4的电化学性能有了一定进展, 可以在不同程度上提高LiFePO4的电化学性能, 但是单纯的掺杂金属离子实验结果并不理想。另外,很多研究者在掺杂金属离子的同时也对LiFePO4进行了表面碳包覆[24-26],这就导致究竟是何种因素引起LiFePO4电化学性能的改变并不清楚。因此有必要采用新的制备工艺, 在LiFePO4不包覆碳的情况下,掺杂金属离子,最好能控制LiFePO4的晶粒尺寸及颗粒分散性,研究清楚金属离子掺杂对其电化学性能的影响。
2.3 制备特殊形貌、亚微米或纳米级别的LiFePO4
纳米材料是随人类对材料的原子或分子排列结构的认识加深, 出现的不同于常规材料结构的新型材料。由于结构单元的尺寸特殊性,使得纳米材料与传统常规材料的性能有很大差异, 主要具有表面与界面效应、小尺寸效应、量子尺寸效应及宏观量子隧道效应4 个方面特殊性。相较在导电性方面的限制,锂离子在LiFePO4材料中的扩散是电池放电最主要也是决定性的控制步骤, 如果制备LiFePO4纳米材料,其优点主要有[29-32]:1)LiFePO4纳米材料具有较高的比表面积,这就可以增大LiFePO4的反应界面,并可以为锂离子的扩散提供更多的通道;2)LiFePO4纳米材料的缺陷和微孔较多,理论储锂容量较高,同时, 较小的颗粒尺寸可以减少锂离子嵌入脱出深度和行程,加快锂离子的迁移;3)LiFePO4纳米粒子之间有较大的间隙, 可以有效地缓解脱嵌锂离子的应力,最终可以提高电池循环寿命;4)纳米材料的蠕变性,使LiFePO4具有较强的体积变化承受能力,可以有效缓解充放电过程中材料体积变化导致的材料结构破坏,提高电池循环稳定性。 另外,由于一些特殊结构,例如壳层、片层、花状等微观结构,也有利于提高材料比表面积,可以提高锂离子的传输速率,也被研究者广泛关注。
Ren Yu 等[29]以LiOH·H2O、H3PO4和Fe(NO3)2·9H2O 为原料, 利用旋转蒸散法制备了介孔LiFePO4纳米材料,并进行了详细研究。 发现在1C 倍率下,放电比容量为137 mA·h/g; 在30C 高倍率充放电后,材料的容量仍能恢复到160 mA·h/g,证明介孔纳米化的LiFePO4电化学性能得到了显著提升。
人们通常认为LiFePO4材料, 锂离子主要是沿着[010]方向扩散,在[100]方向锂离子扩散能力有限。 Z.Li 等[30]利用溶剂热法,成功地制备了[100]取向的LiFePO4纳米薄片,厚度为12 nm。 用碳包覆后,以20C 电流密度放电时,其放电容量达到了122 mA·h/g;更重要的是在10C 电流密度下进行1 000 次循环之后仍然保持了90%的容量, 说明纳米化后的LiFePO4材料电化学性能发生了很大改变。
C.Sun 等[31]以乙酸锂水合物(CH3COOLi·2H2O)、铁(Ⅲ)硝酸盐水合物[Fe(NO3)3·9H2O]和磷酸二氢铵(NH4H2PO4)为原料,利用溶剂热法结合高温煅烧,成功地制备了LiFePO4花状微米球结构材料,其电化学性能得到了极大改善。在0.1C 电流密度充放电时比容量约为140 mA·h/g,以5C 电流密度循环1 000 次之后比容量为110 mA·h/g, 在10C 电流密度循环1 000 次之后比容量仍然有86 mA·h/g。近年来,Z.Ma 等[32]以LiOH·H2O、H3PO4、FeSO4·7H2O 和柠檬酸为原料,以乙二醇(EG)为反应介质,采用溶剂热法制备了C 包覆的厚度为25 nm 的LiFePO4纳米片材料。 在1C 电流密度充放电时其比容量可达到160 mA·h/g 以上, 并且展现出超高倍率性能,以100C 电流密度充放电时比容量可达64.5 mA·h/g。
大量实验结果表明, 特殊形貌的LiFePO4或者纳米LiFePO4材料,有利于提高其电化学性能,但是纳米材料团聚、制备成本高仍是目前亟待解决的问题。
3 结论
总结了近年来对LiFePO4的研究, 介绍了对LiFePO4进行表面改性、体相掺杂及制备纳米LiFePO4、花状等特殊形貌LiFePO4正极材料。 将碳材料与LiFePO4进行复合,可以有效地改善其循环、倍率等电化学性能; 对LiFePO4进行体相掺杂可以改进其电化学性能;纳米LiFePO4、介孔花状等特殊形貌LiFePO4材料,可以有效增大材料比表面积,可以提高锂离子的传输速率。
以现有的实验结果来分析, 通过对LiFePO4表面包覆碳材料进行改性更具有现实意义, 建议研究者主要通过利用碳材料来改进LiFePO4电化学性能, 但是需要对碳包覆导致LiFePO4材料的电化学性能改变规律、碳形态、包覆成本等进一步深入地研究。 另外如果能够实现简易制备LiFePO4纳米材料或者特殊形貌结构LiFePO4,很有可能解决LiFePO4的自身缺陷,使LiFePO4的大范围应用成为可能。虽然在LiFePO4表面改性、 体相掺杂及制备纳米LiFePO4等方面已有大量研究, 但相关改进方法也存在工艺复杂、性能不稳定等问题,仍然需要进一步的研究改进。

