右室不同部位起搏对术后新发房颤和心功能不全影响的研究
刘怡
徐州市中心医院心脏诊疗中心,江苏徐州 221009
近几年生理性起搏(physiological pacing)的概念越来越受到关注, 不仅要求电激动的房-室顺序下传,还应尽可能维持双心室肌电-机械活动的生理性同步,从而使起搏器介导下的血流动力学更接近生理状态。 过去观点认为双腔DDD 模式是生理性起搏,但研究证实长期的右心室心尖部(rightventricularapex,RVA)起搏可导致心功能不全和心房颤动的发生。 选择最佳部位起搏被逐渐应用于临床, 以期避免起搏所带来的电机械活动的不同步, 以期获得最大的心排血量满足机体的需要。 右室选择性起搏的常用部位在右心室流出道间隔 部(right ventricular outflow tractseptal,RVOT),该 部位起搏引起的心脏电激动的顺序接近正常生理状态,使心室内和室间的激动更加协调,减少了心室电-机械活动的失同步,心肌组织的血流灌注改善,从而降低了对心功能及血流动力学等一系列不良影响[1-2]。 该研究对该中心2017 年1 月—2018 年12 月期间因房室传导阻滞行DDD 起搏的患者60 例进行了随访观察, 探讨右室不同部位起搏与术后新发房颤和心功能不全发生的关系,以期对临床上选择起搏部位、评价起搏术后疗效提供依据。 现报道如下。
1 资料与方法
1.1 一般资料
随机选取该院因房室传导阻滞行双腔起搏器植入的患者60 例,其中男33 例,女27 例。 随机分为两组:右室流出道起搏组(ROVT 组)30 例, 男17 例, 女13例;平均年龄(60.15±11.81)岁。 右室心尖部起搏组(RVA组)30 例,男16 例,女14 例;平均年龄(60.22±10.47)岁,入组后分别行右室流出道起搏和右室心尖部起搏,术后随访12 个月。纳入标准:①经十二导联心电图或动态心电图明确诊断高度房室传导阻滞或III 房室传导阻滞,符合双腔起搏器植入指南;②年龄>18 周岁;③超声心动图检查提示心脏结构正常,左室收缩功能正常;④心功能分级( NYHA) I 级。 排除标准:①术前存在房性心动过速、房扑、房颤等房性心律失常的患者;②心功能分级(NYHA)II 级以上;③瓣膜性心脏病、甲状腺疾病、先天性心脏病、慢性阻塞性肺部疾病病史;④恶性肿瘤、严重器官损害的疾病患者;⑤无法配合研究的患者。 该研究经过伦理会批准入组患者及家属均签署知情同意书。
1.2 方法
双腔起搏器的植入:①常规消毒后行局部麻醉,选取左侧锁骨或左腋静脉穿刺点, 穿刺成功先后分别递送右心室螺旋电极和右心房电极。 ②右室电极植入:RVOT 起搏组:将右室螺旋电极导线送至右心室,调整电极头端与右心室流出道间隔部关系, 使得左前斜位时右室电极头端指向脊柱, 找到起搏QRS 时限最小处再固定电极。RVA 起搏组:按常规方法将螺旋电极固定在右室心尖部。③心房电极固定于右心耳。④固定电极导线后测量感知、阈值、阻抗等各项起搏参数、监测起搏心电图。 ⑤连接导线和脉冲发生器,并将皮下组织进行缝合, 同时用纱布包扎伤口。 ⑥所有患者均程控为DDD 起搏模式。
1.3 观察指标
所有患者术后随访12 个月,随访时间为术后1 个月、6 个月、12 个月。 在术前及术后的随访时间点完善相关检查:常规十二导联心电图、动态心电图、心功能分级(NYHA)评估、超声心动图以及起搏器程控检查。记录新发房颤发生率及术后第一次发生时间、 心功能分级、左心室舒张末期容积(LVEDV)、左室射血分数(LVEF)。 心功能评价指标:①按NYHA 标准评定心功能;②根据美国超声学会标准,测定左心室舒张末期容积(LVEDV)、左室射血分数(LVEF)。 房颤(AF)的发生定义为程控记录到350 次/min 以上的心房高频事件或心电图及24 h 动态心电图记录到AF。
1.4 统计方法
采用SPSS 22.0 统计学软件分析数据,计量资料用(±s)表示,组间差异比较用t 检验;计数资料采用[n(%)]表示,组间差异比较用χ2检验,P<0.05 为差异有统计学意义。
2 结果
2.1 一般资料
右室流出道起搏组(ROVT 组)30 例,男17 例,女13 例;平均年龄(60.15±11.81)岁。 右室心尖部起搏组(RVA 组)30 例,男16 例,女14 例;平均年龄(60.22±10.47)。年龄、性别等临床资料差异无统计学意义(P>0.05),具有可比性。 见表1。

表1 两组患者一般资料比较
2.2 新发房颤指标
两组术后房颤发生率比较:RVOT 组术后新发房颤4 例, 发生率为13.33%;RVA 组术后新发房颤5 例,发生率为16.67%;两组比较差异无统计学意义(χ2=0.000,P>0.05)。ROVT 组术后新发房颤首次出现时间为(9.12±2.55)月,RVA 组首次出现时间为(6.34±2.78)月,ROVT组术后新发房颤首次出现时间晚于RVA 组,差异有统计学意义(t=4.036,P<0.05)。
2.3 心功能相关指标
两组术前左心室舒张末期容积 (LVEDV)[(46.2±7.1)mm vs (47.3±10.1)mm] 及左室射血分数(LVEF)[(54.1±0.8)% vs (51.2±13.5)%],差异无统计学意义(t=0.488、1.175,P>0.05)。 而在术后12 个月,LVEDV 低于右室心尖起搏组[(47.5±6.9)mm vs (51.2±13.5)mm],右室流出道起搏组LVEF 高于RVA 组[(52.5±0.7)% vs(47.5±0.9)%],均差异有统计学意义(t=4.050、24.020,P<0.05)。 见表2。
表2 两组患者LVEDV 和LVEF 的比较(±s)
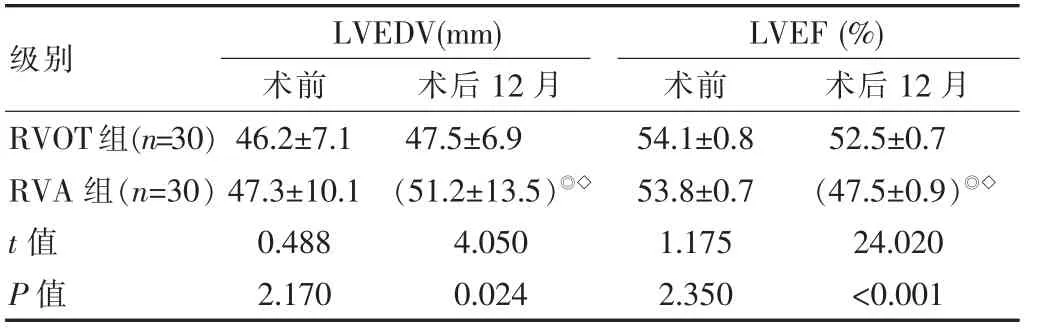
表2 两组患者LVEDV 和LVEF 的比较(±s)
注:与术前比较,◎P<0.05;与RVOT 组相比,◇P<0.05
级别LVEDV(mm)术前 术后12 月LVEF (%)术前 术后12 月RVOT 组(n=30)RVA 组(n=30)t 值P 值46.2±7.1 47.3±10.1 0.488 2.170 47.5±6.9(51.2±13.5)◎◇4.050 0.024 54.1±0.8 53.8±0.7 1.175 2.350 52.5±0.7(47.5±0.9)◎◇24.020<0.001
3 讨论
临床工作中许多患者因房室传导阻滞和病窦综合征植入心脏起搏器后,发生了心功能不全及房颤。 目前已有的研究证实[3]房室顺序起搏较单心室起搏能够降低术后房颤的发生,改善患者生活质量,生理性右心房起搏有助于预防房颤的发生。 而在减少心衰发生方面DDDR 并没有积极作用,仅通过增加心率来增加心输出量,改善患者的生活质量。 右心室心尖部起搏因手术植入操作相对简单、容易固定、不易脱位等特点至今仍被许多医生选择。 但长时间的RVA 起搏会改变双心室电同步性, 使心室内电激动顺序异常类似左束支传导阻滞,造成非同步的室间及室内的室壁收缩运动,使心脏扩大和心肌重构,心脏泵功能受损,发生心功能不全和房颤的风险增加[4]。 多中心的随机对照研究结果表明[5],与单纯的RVA 起搏比较,房室同步起搏在减少心衰和房颤等方面并没有显著的优势。 因此对房室传导功能正常的病窦综合征的患者, 通过优化起搏参数和程控起搏模式尽可能地减少右室起搏, 以减少起搏所致室间不同步带来的一系列不良影响; 而对于房室传导阻滞行双腔起搏治疗的患者,希氏束(His)起搏以及随之而来的左束支起搏所引发的电刺激, 通过希氏—浦肯野系统这一正常的传导通路下传, 是最符合生理性起搏要求的心室起搏方式[6]。但由于His 定位难、导线置入困难以及起搏阈值较高等问题,临床应用受限[7]。 而右室流出道在解剖上接近His 束及室间隔上部,理论上可以使激动尽早进入传导系统, 提高起搏后心肌电活动的同步性。 该部位起搏可避免右室心尖部起搏引起的心室间及室内的收缩失同步, 更大程度地提高起搏后心脏电-机械运动的同步性。 龙曼云等[8]观察了行永久起搏器治疗的老年患者人群, 结果显示短期右室流出道起搏较右室心尖部起搏具有更好的血流动力学效应,对心功能的影响小。
该研究结果显示, 两组术后房颤发生率比较差异无统计学意义, 而ROVT 组术后新发房颤第一次发生时间晚于RVA 组。 Mittal S 等[9]随访了起搏器植入术后房性快速性心律失常(AHRE)的发生率,结果示在双腔起搏器植入后的6 个月AHRE 率为18%, 该研究ROVT 组和RVA 组术后新发房颤的发生率分别为13.33%、16.67%,与Mittal S 等研究结果相似。起搏器植入后ROVT 组术后新发房颤第一次发生时间晚于RVA组, 术后12 个月RVOT 组左心室射血分数高于RVA组, 左心室舒张末内径低于RVA 起搏组并且RVA 组较ROVT 组更为显著。 考虑RVA 组心功能指标劣于ROVT 组的原因不仅仅是由于异常的心室激动顺序和不利的血流动力学影响, 还可能与新发房颤后心房激动的同步性遭到破坏、 显著的心室律不规则进一步加重血流动力学障碍,使心功能恶化[10-12]相关。 该研究结果表明DDD 模式下, 相较于RVA 部位起搏,ROVT 起搏可以延缓新发房颤的发生和心功能不全的发展。
DDD 模式下右室ROVT 部位起搏较RVC 起搏可以减少术后新发房颤和心功能不全的发生,改善预后,提高生活质量。 该实验所纳入对象仅为单中心,且样本量小,随访时间较短,研究数据有一定的偏倚和误差,因此只能说明一种趋势。 该研究缺乏对右室其他部位起搏对房颤及心功能的影响进行比较分析, 相关结果还需进一步的临床试验研究。

