重组人干扰素α2a治疗难治性白塞综合征的疗效及安全性
侯云霞,刘金晶,杨云娇,李璐,郁欣,史婧,孙鹿希,郑文洁
白塞综合征(Behçet syndrome,BS)是一种病因不明的多系统受累的慢性自身免疫性疾病,其发病机制主要包括中性粒细胞活化、内皮细胞功能障碍、高凝状态等[1-2],多种促炎细胞因子过度表达,包括白介素2(interleukin,IL-2)、IL-6、IL-8、IL-10、IL-12、IL-17、IL-18、干扰素-γ(interferon γ,IFN-γ)、肿瘤坏死因子α(tumor necrosis factor α,TNF-α)等均参与发病[3]。对于BS治疗除传统的皮质类固醇激素及免疫抑制剂等药物, 还有通过抑制上述细胞因子而发挥作用的生物制剂,目前国内用于BS的生物制剂主要有TNF-α抑制剂、IL-6拮抗剂、IFN-α2a等。IFN-α2a治疗白塞病葡萄膜炎(Behçet disease Uveitis,BDU)研究较多且效果肯定[4],但其应用于BS其他器官受累的治疗经验较少,多为个案报道,中国尚未见相关报道,本研究探讨9例顽固性黏膜溃疡、血管、神经受累的难治性BS患者应用IFN-α2a的疗效及安全性,为难治性BS的治疗提供一定经验。
1 对象与方法
1.1 对象
回顾性分析2014年11月到2019年7月在北京协和医院接受IFN-α2a治疗的9例重症和(或)难治性BD患者的临床资料,收集其临床表现、影像学资料、实验室检查、IFN-α治疗前后的用药情况及疾病转归等。所有患者均符合2013年白塞病国际研究组标准(international criteria for Behçet’s disease,ICBD)[5]。
1.2 统计学处理
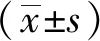
2 结果
2.1 一般情况
共纳入9例患者(男7例,女2例),平均年龄(36.55±5.03)岁,病程(122±84.45)个月,有复发性口腔溃疡者9例,皮肤病变7例,外阴溃疡7例,关节炎2例,中柩神经系统受累4例(均为脑实质受累,其中1例为脊髓型,表现为播散性脊髓炎,2例为脑干病变,1例为右枕叶病变;同时并发颅内静脉窦血栓2例),血管病变2例[1例为多发静脉血栓,包括上下腔静脉、颈静脉、下肢深静脉;另1例为多发下肢动脉狭窄、闭塞,包括右足背动脉、左腘、胫前、后动脉、足背动脉狭窄,同时有反复下肢深静脉血栓(deep vein thrombosis, DVT)伴发血栓后综合征]。9例患者病程中有全葡萄膜炎受累者4例(表1)。
2.2 既往治疗及IFN-α2a联合治疗
2.2.1 既往治疗
在使用IFNα-2a之前,9例患者均接受了皮质类固醇激素与免疫抑制剂联合常规治疗(表2),但均效果欠佳。3例顽固性黏膜溃疡患者经激素(glucocorticoids,GCS)先后联合多种免疫抑制剂/调节剂,如沙利度胺(thalidomide,THD)、环磷酰胺(cytoxan,CTX)、甲氨蝶呤(methotrexate,MTX)、秋水仙碱(colchicine,COL)、艾拉莫得(iguratimod,IGU)、环孢素(cyclosporin a,CsA)等治疗,患者仍有反复黏膜溃疡(且1例伴有反复下肢结节性红斑)。3例神经系统受累患者经激素联合CTX、吗替麦考酚酯(mycophenolate mofetil,MMF)、MTX、羟氯喹(hydroxychloroquine,HCQ)、COL治疗,且1例接受过短期的托法替布(tofacitinib,TOF)治疗,2例疗效欠佳,仍有神经系统病情进展,另1例患者联合托珠单抗(tocilizumab,TCZ)(每次8 mg/kg)治疗后,脊髓病变有一定控制,但出现巨大肛周溃疡不愈合,且经费困难,换用IFN-α2a。2例血管受累者经激素联合CTX、CsA治疗无效,其中1例急性上腔静脉综合征无缓解,头颈部肿胀明显,1例为血栓后综合征皮肤溃疡。另有1例患者存在多器官受累(皮肤黏膜、神经系统、全葡萄膜炎、颅内静脉窦血栓),先后应用激素联合硫唑嘌呤(azathioprine, AZA)、CTX、CsA、THD、HCQ等多种药物,疗效均较差。以上患者病程中4例出现治疗相关不良反应,包括激素相关股骨头坏死1例,肝酶升高2例,THD过敏反应1例,手足麻木1例。4例同时并发葡萄膜炎患者,应用IFN-α2a时眼炎处于稳定期。

表1 患者一般情况、临床表现、治疗Table 1 General characteristics,clinical manifestation, treatment
DVT:深静脉血栓
4例患者患有慢性乙型肝炎病毒感染,均为乙肝表面抗原、乙肝e抗体、乙肝核心抗体三项阳性,恩替卡韦抗病毒治疗中,1例患者因并发肺结核而接受4联抗结核治疗。
2.2.2 IFN-α2a联合治疗
IFN-α2a初始剂量为300万IU隔日一次,皮下注射,应用3~6个月后依据病情再进行剂量调整。IFN-α2a联合治疗时,1例患者未用激素,仅继续之前的免疫抑制剂,其余患者均联合激素及免疫抑制剂治疗,8例患者继续之前的免疫抑制剂,1例患者依据病情更换了免疫抑制剂,随访过程中,依据病情逐渐减量激素及免疫抑制剂。
2.3 疗效及随访
平均随访(9.78±2.72)个月后,所有患者临床症状均有改善,皮质类固醇激素使用剂量及免疫抑制剂应用种类均较前减少,随访3、6个月和末次随访时中位泼尼松剂量从10(0,60)mg分别减到7.5(0,25)mg(P=0.011)、 5(0,15)mg(P=0.012)和 4.375(0,12.5)mg(P=0.018),中位免疫抑制剂种类从2(1,3)种逐渐减少,3个月时为1(0,3)(P=0.008),6个月时为1(0,2)种(P=0.007),末次随访中位免疫抑制剂种类为1(0,1)种(P=0.014)。1例(12.5%)患者停用激素,3例(33.3%)患者停用免疫抑制剂。
2.4 安全性
所有患者均未发生严重的不良反应,4例患者出现白细胞减低,其中1例IFNα2a调整为300 万IU,每2周1次后白细胞恢复正常,其余3例均为一过性减低;1例患者有间断发热,但均为低热,能耐受;无肝酶升高,1例患者连续应用IFN-α2a 12个月出现轻度抑郁表现(NO.2),停药后症状改善,未观察到甲功异常。
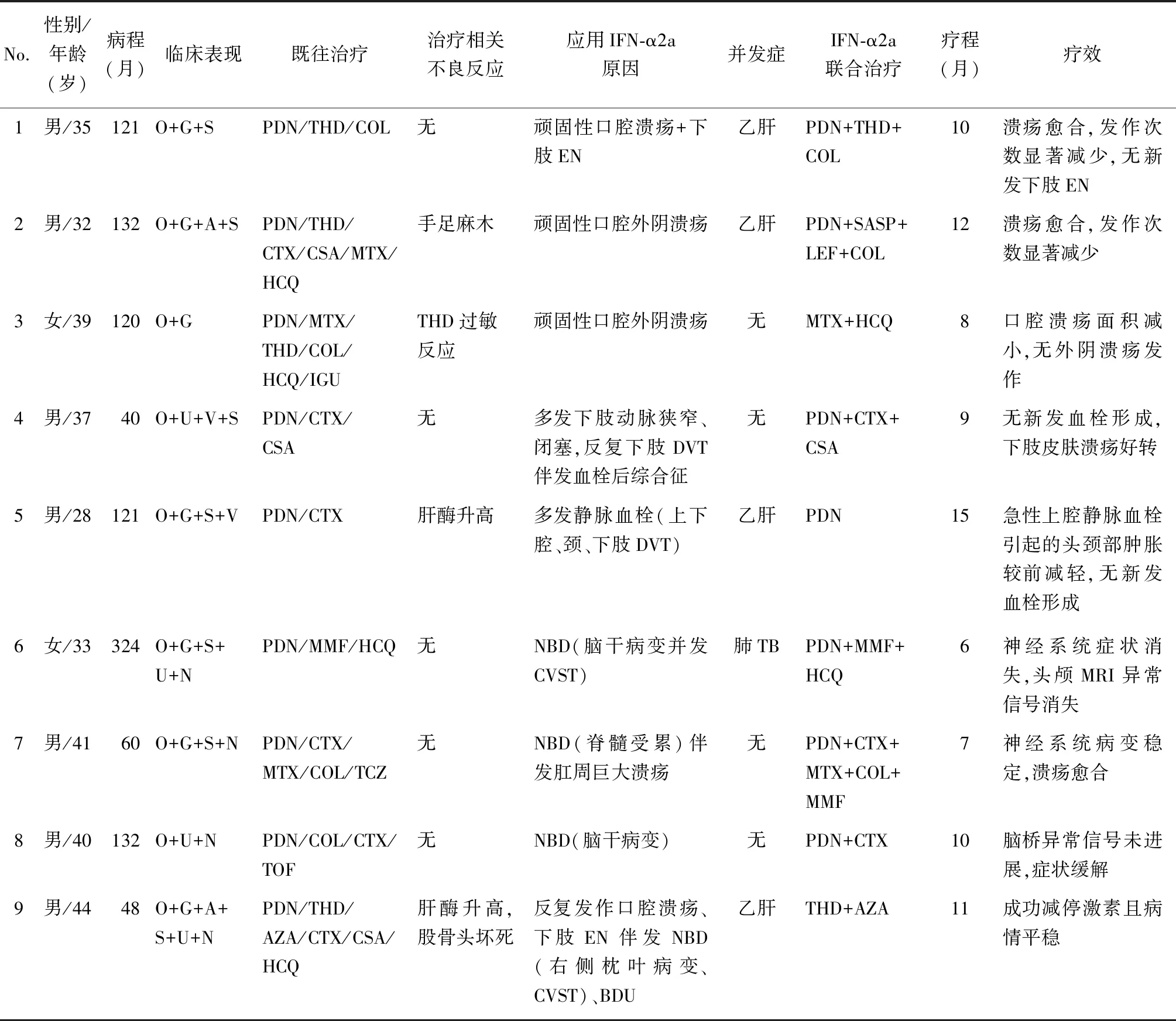
表2 干扰素α2a治疗难治性BS疗效Table 2 Effect of interferon α2a on refractory BS
A:关节炎; G:生殖器溃疡; O:口腔溃疡; S:皮肤病变; U:葡萄膜炎; V:血管病变; N:神经病变; NBD:神经白塞; BDU:白塞葡萄膜炎; CVST:颅内静脉窦血栓; DVT:下肢深静脉血栓; EN:结节性红斑; PDN:泼尼松; CTX:环磷酰胺; MTX:甲氨蝶呤; HCQ:羟氯喹; THD:沙利度胺; CSA:环孢素; AZA:硫唑嘌呤; MMF:吗替麦考酚酯; IGU:艾拉莫得; TCZ:托珠单抗; TOF:托法替布; COL:秋水仙碱
3 讨论
本研究探讨了对传统激素联合免疫抑制剂治疗无效的难治性BS患者加用IFN-α2a的疗效及安全性。本组患者临床主要表现为顽固性黏膜溃疡、严重血管或神经系统受累,经激素联合多种免疫抑制剂积极治疗后临床无明显改善,部分患者出现药物相关不良反应,且4例并发乙肝病毒感染,1例并发肺结核。接受IFN-α2a治疗后,平均随访(9.78±2.72)个月,所有患者临床症状均有改善,且有一定的皮质类固醇激素和免疫抑制剂的节约效应,同时无明显不良反应。
BS是一种病因未明的慢性复发性血管炎性疾病,目前认为,在遗传易感背景下,病毒、细菌感染等触发因素,启动天然免疫,继而激活获得性免疫,导致T细胞稳态破坏,最终导致持续性炎症和组织损伤。活动性BS患者外周血Th1和Th17细胞升高[6-7],调节性T细胞(Treg)数量减少[8]。IFN-α2a可显著降低BS患者外周血Th17细胞数,升高Treg细胞数[9]。同时可升高外周血IL-10和IL-35水平[10-11],以抑制Th1和Th17细胞功能,并放大Treg的免疫应答。另外,IFN-α2a可降低CD4+T细胞和单核细胞表面Toll样受体的表达,从而减弱天然免疫应答[11]。中性粒细胞过度活化与浸润是BS急性炎症反复发作的主要原因。IFN-α2a可抑制中性粒细胞的吞噬作用和自由基的产生[9]。γδT细胞是黏膜炎症中的重要免疫细胞,在BS的发病机制中发挥重要作用[12]。活动BS患者的外周血Vγ9Vδ2 型T细胞比例较健康对照增加[13],BDU患者房水中可产生被异戊烯焦磷酸分枝杆菌(IPP)特异性激活的TCRVγ9Vδ2型的T细胞[14-15],而IFN-α2a可减少γδT细胞的数量[16]。 综上,IFN-α2a可通过影响Toll样受体表达、天然免疫细胞(中性粒细胞、γδT细胞)和获得性免疫细胞(T细胞)活化等多重机制,改善BS患者免疫系统失衡。
皮肤黏膜受累是BS的主要特征,表现为反复口腔、外阴溃疡,皮肤结节红斑、毛囊炎,影响生活质量,沙利度胺可用于治疗BS患者严重口腔、生殖器溃疡及皮肤病变,但可出现过敏反应、致畸、周围神经病等不良反应。传统糖皮质激素联合免疫抑制剂治疗是BS合并器官受累主要的治疗选择,但是长期应用会出现严重的不良反应,且部分患者无效。TNF-α抑制剂对于难治性BS疗效肯定,但部分患者存在反应差、不耐受、疗效减退和相对禁忌证等诸多问题。近年来,越来越多的研究证实IFN-a2a可用于难治性BS的治疗[4, 17-18]。且IFN-α2a的费用要明显低于TNF-α抑制剂。而且对于一部分同时并发乙肝、结核的患者,TNF-α抑制剂为禁忌,更加优选IFN-α2a。
已有IFN-α2a治疗BS的报道多针对难治性、复发性BDU患者,且IFN-α2a治疗BDU也已写入《2018年最新白塞综合征临床管理EULAR指南》[19]。对于IFN-α2a治疗BS其他器官受累的报道相对较少,仅为个案报道和小规模研究,主要用于顽固性皮肤、黏膜病变[20-21],神经系统受累[22]。Ozguler[23]新近报道了IFN-α2a可预防BS并发下肢DVT复发并促进血管再通。本团队前期对IFN-α2a联合激素和免疫抑制剂治疗难治性复发性BDU的有效性和安全性进行评价,研究显示,IFN-α2a同激素与免疫抑制剂联用可有效降低眼炎复发率,减少激素的用量、免疫抑制剂的种类和剂量,且应用IFN-α2a期间本组患者未出现严重不良反应,自身抗体持续阴性[4]。在此基础上,首次在国内对BS并发顽固性皮肤黏膜受累、血管、神经受累的难治BS患者应用IFN-α2a进行疗效和安全性评估。接受IFN-α2a治疗后,平均随访(9.78±2.72)个月,3例顽固性皮肤黏膜受累患者,口腔及外阴溃疡发作频率均明显减少,且1例对抑制新发下肢结节性红斑有效;2例并发血栓的血管受累患者均无新发血栓出现,其中1例反复血栓引发下肢皮肤溃疡好转,另1例急性上腔静脉血栓伴发的头颈部肿胀明显好转;3例神经系统受累患者病变未再进展,其中1例症状缓解,1例症状消失且头颅影像学改善,1例脊髓病变控制且合并的巨大肛周溃疡完全愈合;1例多系统受累患者既往传统治疗过程中出现严重的药物不良反应(肝酶升高及股骨头坏死),应用IFN-α2a后病情进一步缓解,且成功减停激素。与应用IFN-α2a治疗前相比,所有患者的临床症状均有改善,皮质类固醇使用剂量及免疫抑制剂种类均减少,且1例(12.5%)患者停用激素,3例(33.3%)患者停用免疫抑制剂。
有研究提示IFN-α2a与硫唑嘌呤联合应用可出现严重的骨髓抑制[24],本研究中4例患者出现白细胞减低,其中1例调整用药剂量后白细胞恢复正常,其余3例均为一过性减低。1例患者有间断发热,但均为低热,能耐受。文献有报道应用IFN-α2a后出现抑郁及甲状腺功能异常[25-27],本研究中1例患者连续应用IFN-α2a 12个月出现轻度抑郁表现,停药后症状改善,未观察到甲功异常。肝酶升高也有报道[7, 28],但本研究患者均未出现。
本研究亦有一定局限性,主要为单中心回顾性研究,样本量有限,且随访时间尚短,有必要进一步开展前瞻性对照试验研究以明确IFN-α2a用于难治性白塞病的治疗潜力。综上所述,IFN-α2a对于皮肤黏膜、血管、神经受累的难治性BS有效,有利于糖皮质激素及免疫抑制剂减量。

