原发性醛固酮增多症与原发性高血压糖脂代谢和尿酸水平的比较
流行病学研究显示,近年来原发性醛固酮增多症(primary aldosteronism,PA)的发生率明显上升[1]。临床上PA的发生能够导致病人心血管临床意外的发生,增加了病人远期的病死风险[2]。过度的醛固酮释放,能够通过醛固酮受体的激活,影响脂质的代谢过程,导致体内脂蛋白代谢紊乱,并显著增加低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)、总胆固醇(total cholesterol,TC)及三酰甘油(triglyceride,TG)的浓度;原发性的醛固酮的显著释放,还能够导致体内血管内皮细胞损伤,加剧动脉血管内皮下泡沫细胞的沉积,促进粥样斑块的形成和血管狭窄;醛固酮系统的激活过度,能够导致肾脏入球小动脉的持续性痉挛和肾脏组织的缺血性再灌注损伤,增加了尿蛋白的漏出[3]。部分研究者报道了PA病人体内血脂代谢紊乱和肾功能损伤情况[4],但缺乏与原发性高血压(essential hypertension,EH)的对比分析。为了进一步揭示PA的临床病情特征,为临床上PA病人的早期临床干预提供参考,本研究选取2013年1月—2018年1月在我院治疗的PA病人80例,探讨PA病人血脂代谢紊乱和靶器官损害情况,现报道如下。
1 资料与方法
1.1 一般资料 选取2013年1月—2018年1月在我院治疗的PA病人80例(PA组),同时按照性别、年龄(相差3岁内)、高血压病程(相差2年内)进行匹配,选取EH病人80例(EH组)。纳入标准:①PA病人符合卧位血浆醛固酮/肾素活性比值(ARR)>40和直立位ARR>25,同时卡托普利试验和(或)静脉盐水负荷试验显示高醛固酮水平不受限制;原发性高血压诊断符合高血压病防治指南中的标准[5];②病人及家属知情同意。排除标准:①近2个月服用过受体阻断剂、血管紧张素转换酶抑制剂、血管紧张素Ⅱ受体拮抗剂、利尿剂等药物;②合并有感染、心功能不全、肝肾功能不全等疾病。PA组和EA组性别、年龄等一般资料比较差异无统计学意义(P>0.05)。详见表1。

表1 两组一般资料比较
注:1 mmHg=0.133 kPa。
1.2 方法 胰岛素抵抗指数(homeostasis model assessment resistance index,HOMA-IR)计算方式:空腹血糖水平(FPG,mmol/L)×空腹胰岛素水平(FINS,mU/L)/22.5。采集病人入院后静脉血,离心后收集上清液,采用化学发光法检测尿微量白蛋白排泄率(UAER)、糖基化血红蛋白(HbA1c)水平,检测仪器为美国Bio-Bad全自动酶标仪,配套试剂盒购自罗氏检测公司;采用全自动生化法检测TG、TC、LDL-C、游离脂肪酸(FFA)、尿酸(UA)水平,配套试剂盒购自南京碧云天生物检测公司。病人进行颈部血管超声检查,采用德国西门子公司生产的SEQ-520型超声诊断仪器进行诊断,探头频率设置为10 MHz,沿着颈总动脉、动脉分叉、颈内动脉,分别测量颈总动脉和颈内动脉中膜厚度。比较两组脂糖代谢指标、UA、靶器官损害指标[UAER、左心室质量指数(LVMI)]、颈总动脉及颈内动脉中膜厚度水平。将PA病人ARR与糖脂代谢指标、UA、靶器官损害指标以及颈总动脉及颈内动脉中膜厚度进行相关分析。

2 结 果
2.1 两组糖脂代谢及UA水平比较 PA组TG、TC、LDL-C、FFA、FINS、UA和HOMA-IR水平明显低于EH组(P<0.05),而ARR明显高于EH组(P<0.05);PA组和EH组HDL-C、FBG、HbA1c水平比较,差异无统计学意义(P>0.05)。详见表2。
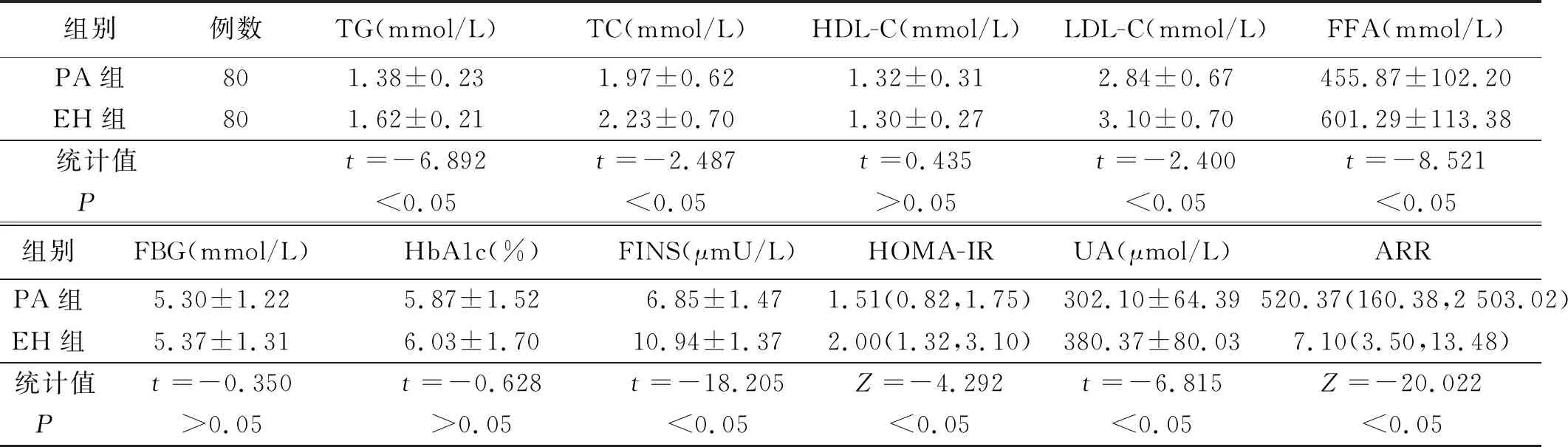
表2 两组脂糖代谢及UA水平比较
2.2 两组靶器官损害指标比较 PA组UAER和LVMI明显高于EH组(P<0.05)。详见表3。
表3两组靶器官损害指标比较[M(P25,P75)]
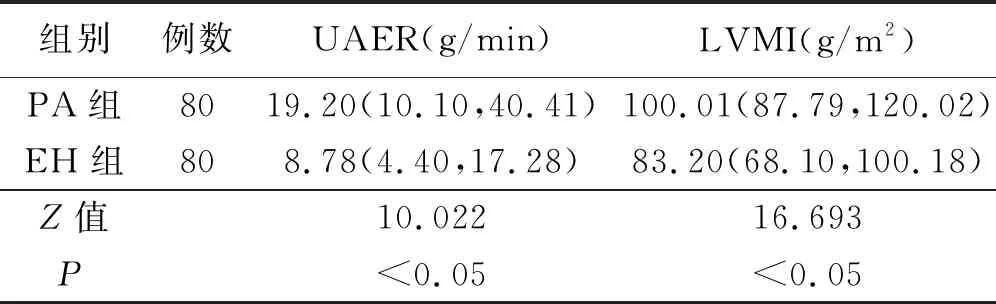
组别例数UAER(g/min)LVMI(g/m2)PA组8019.20(10.10,40.41)100.01(87.79,120.02)EH组808.78(4.40,17.28)83.20(68.10,100.18)Z值10.02216.693P<0.05<0.05
2.3 两组颈总动脉及颈内动脉中膜厚度比较 PA组颈总动脉和颈内动脉中膜厚度明显高于EH组(P<0.05)。详见表4。

表4 两组颈总动脉及颈内动脉中膜厚度比较(±s) 单位:mm
2.4 相关分析 ARR与UA呈负相关(r=-0.322,P<0.05),与UAER、颈总动脉及颈内动脉中膜厚度呈正相关(r值分别为0.572、0.343、0.310,P<0.05)。
3 讨 论
在合并有相关家族史或者基因突变的病人中,肾上腺皮质功能亢进的风险可显著上升,特别是在合并下丘脑-垂体-肾上腺系统病变的病人中,PA的发生风险可进一步上升。PA的发生不仅影响水钠代谢,同时还能够导致病人心血管意外或者脑血管意外的发生,增加病人的生存预后恶化的风险[6]。现阶段临床上PA治疗后的病情缓解率仍然较低,治疗后的病情进展速度仍然较快,靶器官的损害风险持续性维持在较高的水平[7]。而本研究对于PA与EH的对比性分析研究,具有两个方面的现实意义:①能够为疾病的早期预防和病情控制提供依据;②能够为PA或者EH病人临床转归提供评估指标。虽然部分研究者关注了在PA病人中血脂代谢或者血糖代谢水平的改变情况,认为其血脂总体水平较低,而胰岛素抵抗程度也较轻[8],但缺乏对于PA病人与EH病人在肾脏、心脏及动脉管壁等靶器官损害方面的对比研究。
PA组TG、TC、LDL-C、FFA、FINS、UA和HOMA-IR均明显低于EH组,差异有统计学意义(P<0.05),提示PA病人的血脂代谢紊乱程度较低,体内的胰岛素抵抗程度较轻,通过汇集分析不同的相关文献,认为这主要与以下几个方面有关[9-11]:①PA病人肝脏对于胆固醇的逆向转运能力仍然较高,促进了体细胞对于LDL-C或者FFA的摄取和利用,导致血脂指标下降;②PA病人体内的氧化应激程度较轻,炎症信号通路的上调程度较低,进而减轻了胰岛B细胞的损伤程度,降低了胰岛素抵抗程度。周宇清等[12]通过分析62例PA病人的生化指标,发现PA病人体内的LDL-C较EH病人下降25%以上,同时胰岛素抵抗程度也明显下降。ARR在EH病人或者PA病人中均明显上升,但鉴于疾病的本身特点,PA病人的ARR上升更明显,这主要由于疾病的病因不同,过度释放的醛固酮能够显著增加血清中游离醛固酮水平,并降低生理活性肾素的水平,导致ARR水平的上升。LVMI和UAER是评估PA病人靶器官损害的重要指标,PA组UAER及LVMI水平均明显高于EH组,提示了PA病人的心脏及肾脏的损害更明显,靶器官损害程度的上升主要考虑与醛固酮上升诱导的肾脏系膜、基底膜组织的代偿性增生有关,而心脏损害程度的增加主要与醛固酮对于心肌细胞及间质成分重塑性改变的促进作用有关[13-14]。PA组病人的颈总动脉和颈内动脉中膜厚度均明显高于EH组,提示了PA病人心血管累及表现更为明显,血管内皮厚度的增加可导致缺血性心脑血管疾病发生风险上升,而其机制主要由于醛固酮的过度释放能够导致血管内皮下纤维增生,从而增加了血管内膜的厚度[15]。ARR是评估病人醛固酮水平的重要指标,相关分析可见,ARR与UA呈负相关,与UAER、颈总动脉及颈内动脉中膜厚度呈正相关,进一步提示了PA的表达与病人靶器官损害的关系。
综上所述,相比于EH病人,PA病人体内的血脂代谢、血糖代谢紊乱程度较轻,但肾脏及心脏或者动脉管壁的损害程度较高。临床上应该在早期及时干预,从而提高PA病人的临床转归水平。

