杨木预水解液中化学组分质量浓度的P因子调控
刘海梅, 赵 思, 冯年捷
(湖北工业大学 材料与化学工程学院, 湖北 武汉 430068)
木质纤维预水解是指通过加压使水在高温条件下保持液态,利用此状态水具有的特殊性质有效地对结构稳定的木质纤维生物质资源进行水解。因木质纤维预水解过程具有低成本和环境友好性[1],已广泛用于半纤维素抽提[2]。然而,木质纤维预水解液中半纤维素的分离、利用仍存在困难[3]。预水解过程中半纤维素会发生进一步降解,生成糠醛等副产物[4];同时,与部分溶出的木质素形成木质素-碳水化合物复合体(LCC)[5]。尽管已有研究人员利用超滤[6]、絮凝[7]、酸析[8]和树脂吸附[6]等方法处理预水解液,但非糖组分的去除率仍不足60%。预水解液中化学组分的复杂性和多样性,限制了其分离和利用,阻碍了预水解液中高附加值产物的工业化应用。因此,为实现预水解液中化学组分的高效分离和利用,有必要综合分析预水解液中化学组分质量浓度的变化规律。首先,本研究通过分析预水解温度和预水解时间对杨木预水解液中固形物、木质素、木糖和葡萄糖质量浓度的影响;其次,将制浆中的P因子应用到木质纤维预水解中,把影响预水解最大的两个因素(温度和时间)拟合为单一变量,结合碳水化合物的活化能,计算出木质纤维预水解的P因子,以期实现预水解液中化学组分质量浓度的调控,从而为预水解液的高效利用提供基础数据。
1 实 验
1.1 原料与仪器
杨木(PopulustomentosaCarr.),取自湖北省农科院。取杨木木质部,风干,切片,用微型植物粉碎机粉碎,取粒径0.25~0.38 mm杨木粉,苯/乙醇(体积比2∶1)抽提6 h,蒸馏水洗涤3次,P2O5真空干燥,即得脱脂绝干杨木粉,备用。脱脂绝干杨木粉含Klason木质素22.5%、酸溶木质素2.4%、葡聚糖48.2%和木聚糖20.5%。
FZ102微型植物粉碎机,天津泰斯特仪器有限公司;Parr 4530高压反应釜,美国伊利诺斯州Parr仪器公司。
1.2 杨木预水解
取50 g脱脂绝干杨木粉与500 mL蒸馏水混合均匀,加入高压反应釜中,400 r/min连续搅拌,以1.8 ℃/min升温至所需温度(170~210 ℃),反应一定时间(30~120 min)后,降至室温,过滤分离。取30 mL滤液,用于测定预水解液中固形物的质量浓度;另取50 mL滤液,50 ℃减压浓缩,冻干,用于分析预水解液中木质素、木糖和葡萄糖的质量浓度。
1.3 P因子计算
依据阿伦尼乌斯方程和杨木碳水化合物糖苷键断裂活化能,给出P因子计算公式[9],如下式所示:
式中:VT—温度T时的反应速率,mol/(L·s);V373K=1 mol/(L·s);T0—初始温度,303 K;T—任意时刻的温度,K;t1—由T0升温至T所需的时间,h;t2—T温度下的预水解时间,h。

表1 杨木预水解实验设计及相应的P因子
1.4 P因子的设置
表1为不同预水解温度和时间条件下的P因子。P因子可将反应温度和保温时间拟合为单一变量,通过研究P因子对预水解液中化学组分质量浓度的影响,可以实现各化学组分质量浓度的调控。
1.5 化学组分分析
固形物含量按照美国制浆与造纸工业技术协会(TAPPI)标准方法(T650om- 2009)测定;Klason木质素、酸溶木质素、木糖和葡萄糖含量参照美国National Renewable Energy Laboratory分析方法测定[10]。
1.6 数据处理
采取2组平行实验,取平均值,通过Origin 8.0软件拟合曲线。
2 结果与讨论
2.1 工艺条件对预水解液中化学组分的影响
2.1.1固形物 图1为固形物质量浓度与预水解温度和时间的关系。由图可知,固形物质量浓度随预水解温度的升高而增大,随预水解时间的延长而增大。相对于延长预水解时间90 min,升高温度20 ℃ 对固形物质量浓度的影响更为显著。

图1 温度、时间对预水解液中固形物的影响Fig.1 The effect of temperature and time on solid content in prehydrolysis liquor
2.1.2木质素
2.1.2.1总木质素 图2(a)为总木质素质量浓度与预水解温度和时间的关系,总木质素为Klason木质素与酸溶木质素之和。由图可知,总木质素质量浓度随预水解温度的升高而增大,随预水解时间的延长而增大。相对于延长时间90 min,升高温度20 ℃ 对总木质素质量浓度的影响更显著。
2.1.2.2Klason木质素 图2(b)为Klason木质素质量浓度与预水解温度和时间的关系。由图可知,相同时间条件下,当温度升高20 ℃时,Klason木质素质量浓度增大约0.56 g/L;相同温度条件下,当时间延长90 min时,Klason木质素质量浓度增大约0.44 g/L。由此可见,相对于延长时间90 min,升高温度20 ℃略有利于Klason木质素质量浓度的增大。
2.1.2.3酸溶木质素 图2(c)为酸溶木质素质量浓度与预水解温度和时间的关系。由图可知,酸溶木质素质量浓度随预水解温度的升高而增大,随预水解时间的延长而增大。相对于延长时间90 min,升高温度20 ℃对酸溶木质素质量浓度的影响更显著。

a.总木质素 total lignin; b.Klason 木质素Klason lignin; c.酸溶木质素 acid soluble lignin
2.1.3糖
2.1.3.1总糖 图3(a)为总糖质量浓度与预水解温度和时间的关系,总糖为木糖和葡萄糖之和。由图可知,170 ℃条件下,总糖质量浓度随时间延长略有增加;190 ℃条件下,总糖质量浓度随时间延长急剧降低;210 ℃条件下,总糖质量浓度随时间延长逐渐趋于稳定。较高温度条件下,总糖质量浓度的降低,与木糖糠醛化和假木质素的生成有关[4]。
2.1.3.2木糖 图3(b)为木糖质量浓度与预水解温度和时间的关系。相同预水解时间条件下,木糖质量浓度随温度的升高均有一定程度的降低。170 ℃条件下,木糖质量浓度随时间延长略有降低;190 ℃条件下,木糖质量浓度随时间延长急剧降低;210 ℃条件下,木糖质量浓度随时间延长逐渐趋于稳定。
2.1.3.3葡萄糖 图3(c)为葡萄糖质量浓度与预水解温度和时间的关系。相同预水解时间条件下,葡萄糖质量浓度随温度的升高均有一定程度的增大。170和190 ℃条件下,葡萄糖质量浓度随时间延长而增大;210 ℃条件下,葡萄糖质量浓度随时间延长趋于稳定。由此可见,预水解过程中,仅非结晶区纤维素可发生水解[2]。
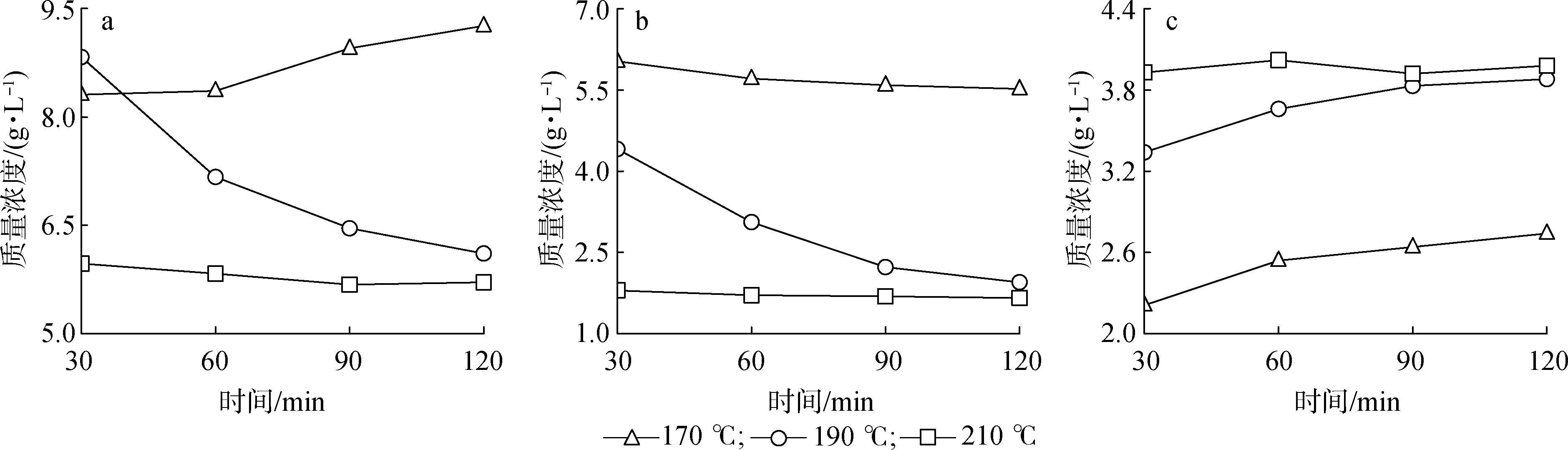
a.总糖total sugar; b.木糖xylose; c.葡萄糖glucose
2.2 预水解液中化学组分的P因子调控

图4 P因子对预水解液中固形物质量浓度的影响Fig.4 The effect of P factor on solid content in prehydrolysis liquor
2.2.1固形物 由图4可知,随P因子增加,固形物质量浓度呈指数增大。根据曲线斜率交汇处,可分为快速增长(P因子<1 600)和慢速增长(P因子>1 600)两个阶段。快速阶段,固形物质量浓度迅速增至18.9 g/L(P因子=1 309);慢速阶段,固形物质量浓度继续增至27.3 g/L(P因子=22 657)。由图可知,木质纤维原料中化学组分主要在快速增长阶段溶出,继续增大P因子,溶出有限。
2.2.2木质素
2.2.2.1总木质素 由图5(a)可知,随P因子增加,总木质素质量浓度呈指数增大,且分为快速增长阶段(P因子<3 000)和慢速增长阶段(P因子>3 000)。快速阶段,总木质素质量浓度迅速增至4.17 g/L(P因子=1 926);慢速阶段,总木质素质量浓度继续增至6.66 g/L(P因子=22 657)。预水解初期以小分子木质素溶出为主;随P因子增加,木质素发生一定程度的碎片化,如β-O- 4断裂等[7],木质素进一步溶出。同时,部分降解溶出的木质素重新吸附在纤维表面[11]。
2.2.2.2Klason木质素 由图5(b)可知,随P因子增加,Klason木质素质量浓度呈指数增大,且分为快速增长阶段(P因子<2 700)和慢速增长阶段(P因子>2 700)。快速阶段Klason木质素质量浓度迅速增至1.38 g/L(P因子=1 926);慢速阶段Klason木质素质量浓度继续增至2.31 g/L(P因子=22 657)。
2.2.2.3酸溶木质素 由图5(c)可知,随P因子增加,酸溶木质素质量浓度可分为快速增长阶段(P因子<3 600)和慢速增长阶段(P因子>3 600)。快速阶段,酸溶木质素质量浓度迅速增至3.23 g/L(P因子=3 214);慢速阶段,酸溶木质素质量浓度继续增至4.36 g/L(P因子=22 657)。比较图5(b)和图5(c)可知,杨木预水解液中木质素主要以酸溶木质素形式存在,这一结果与文献[12]研究报道一致。同时,酸溶木质素质量浓度的快速增长阶段P因子范围较广,可达3 600,而Klason木质素对应P因子为2 700。预水解过程中,杨木化学组分的不断溶出,使木质纤维微观结构发生了一定变化,产生大量开放小孔,提高了与酸性水解液介质的接触面积,促进了酸溶木质素的溶出[13]。

a.总木质素total lignin; b.Klason木质素Klason lignin; c.酸溶木质素acid soluble lignin
2.2.3糖
2.2.3.1总糖 图6(a)为总糖质量浓度与P因子的关系。由图可知,P因子<1 500时,总糖质量浓度随P因子增加而增大;P因子>1 500时,总糖质量浓度随P因子增加而减小。P因子=1 309时,总糖质量浓度达最大值,为9.26 g/L。
2.2.3.2木糖 由图6(b)可知,随P因子增加,木糖质量浓度呈指数减小,且分为快速减小阶段(P因子<3 300)和慢速减小阶段(P因子>3 300)。快速阶段,木糖质量浓度迅速减至3.06 g/L(P因子=3 214);慢速阶段,木糖质量浓度继续减至1.66 g/L(P因子=22 657)。
2.2.3.3葡萄糖 图6(c)为葡萄糖质量浓度与P因子的关系。由图可知,随P因子增加,葡萄糖质量浓度可分为快速增长阶段(P因子<2 400)和慢速增长阶段(P因子>2 400)。快速阶段,葡萄糖质量浓度迅速增至3.34 g/L(P因子=1 926);慢速阶段,葡萄糖质量浓度继续增至3.98 g/L(P因子=22 657)。
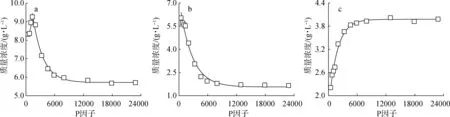
a.总糖total sugar; b.木糖xylose; c.葡萄糖glucose
由此可见,P因子对杨木预水解液中化学组分的质量浓度具有调控作用。固形物、总木质素、Klason木质素、酸溶木质素和葡萄糖的质量浓度均随P因子的增加呈指数增大。木糖的质量浓度随P因子的增加呈指数减小。总糖的质量浓度在P因子1 309时达到最大值,为9.26 g/L。
3 结 论
3.1预水解液中固形物、木质素和葡萄糖质量浓度随预水解温度升高和预水解时间延长而增大;木糖质量浓度随预水解温度升高而减小,随预水解时间延长而减小。
3.2P因子对杨木预水解液中化学组分的质量浓度具有调控作用。随P因子增加,固形物、木质素和葡萄糖质量浓度呈指数增大;而木糖质量浓度呈指数减小。

