糖化血红蛋白分析仪基于风险的多级室内质量控制方案的设计
李婷婷,柯培锋,曹顺旺,黄宪章(广州中医药大学第二附属医院 a.省部共建中医湿证国家重点实验室,b.检验医学部,广州 510120)
美国临床和实验室标准协会(Clinical and Laboratory Standards Institute,CLSI)和国内学者均介绍了风险管理的原理以及如何设计和选择基于风险的室内质量控制(internal quality control,IQC)方案[1-3]。IQC设计传统上着重于对IQC规则和IQC结果个数的选择,以实现较高的误差检出率(probability of error detection,Ped)和较低的假失控率(probability of false rejection,Pfr)。Westgard和Barry等已经开发了多种多样的IQC设计工具[4-7],然而这些工具并不是基于患者风险。Parvin等先后开发了基于患者风险的IQC软件[8-10],Westgard对这些软件进行了优化,建立了西格玛度量IQC批长度列线图[11-12],其中批长度指的是检测系统在其正确度和精密度预期稳定的区间内的标本量[13]。
CLSI C24-Ed4文件建议,对于持续检测的系统,IQC样品应随着患者标本定期检测,第1个IQC称为起始IQC,后续还需定期执行由2个IQC组成的夹心式IQC,用于验证2个IQC结果中间的患者结果是否可报告,这便是多级IQC设计。本研究旨在通过改进之前相关学者开发的IQC工具并利用其确定夹心IQC的批长度,从而为本实验室2种检测HbA1c的分析仪设计基于风险的多级IQC方案。
1 材料与方法
1.1HbA1c正确度验证样品 由国家卫生健康委临床检验中心提供的新鲜冰冻EDTA-K2抗凝全血,此样品按照CNAS-GL03[14]文件评价均匀性和稳定性,满足室间质量评价要求。2018年:每支0.15 mL,共2个批号,批号分别为201811和201812,每个批号各3支。2017年:每支0.10 mL,共2个批号,批号分别为201711和201712,每个批号各3支。-70 ℃保存。
1.2仪器和试剂 Sebia Capilarys 2 flecx piercing(简称“Sebia Capilarys 2FP”)糖化血红蛋白分析仪及其原装配套试剂、校准品和质控品(批号20026)购自法国西比亚公司;Trinity Biotech Premier Hb 9210TM(简称“Premier Hb 9210”)糖化血红蛋白分析仪及其原装配套试剂和校准品购自爱尔兰三一生物科技公司,其质控品购自美国Bio-Rad实验室,批号为33910。
1.3方法
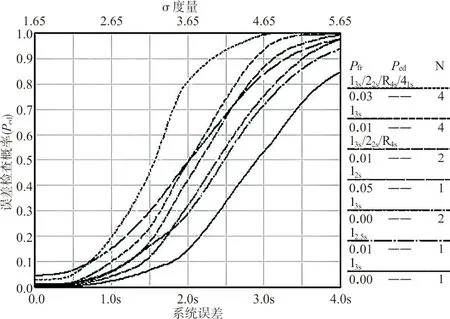
1.3.1评价错误结果对患者危害风险和IQC批长度 利用西格玛度量IQC批长度列线图[15](图1)设计IQC批长度。以西格玛度量画一条垂直于x轴的竖线,竖线与每个质控程序对应直线的交点的纵坐标值为该西格玛水平下选用该质控程序的批长度。例如5σ水平质控程序“13sN1”的批长度为50个患者标本。

注:MR N4表示13s/22s/R4s/41s多规则,每个IQC活动有4个质控检测结果;13sN4表示13s单规则,每个IQC活动有4个质控检测结果;MR N2表示13s/22s/R4s多规则程序,每个IQC活动有2个质控检测结果;13sN2表示13s单规则程序,每个IQC活动有2个质控检测结果;12sN1表示12s单规则程序,每个IQC活动有1个质控检测结果;12.5sN1表示12.5s单规则程序,每个IQC活动有1个质控检测结果;13sN1表示13s单规则程序,每个IQC活动有1个质控检测结果。
图1西格玛度量IQC批长度列线图
1.3.2IQC方案设计的具体步骤 (1)定义检测程序的质量要求,例如允许总误差(allowable total error,TEa)(HbA1c的TEa来源于国家卫生健康委临床检验中心室间质量评价的标准,为7%),最大工作量(1个工作日分析患者标本的最大量,本实验室HbA1c的最大工作量是200个标本),以及期望的报告区间(即2次患者结果报告之间间隔的标本数,本实验室HbA1c的报告区间是50个标本)。利用IQC数据获得检验程序的不精密度,用变异系数(coefficient of variation,CV)来表示;正确度用偏倚(Bias)表示。(2)计算σ,σ=(TEa-|Bias|)/s(单位同为浓度单位或同为百分比单位)[16]。(3)在列线图(图1)中画一条垂直线代表观察到的西格玛度量。(4)通过读取垂直线与IQC程序线的交点对应的y轴数据来估计候选IQC程序最大的批长度。(5)确定起始IQC程序,选择批长度比分析仪最大工作量大且最接近最大工作量的IQC程序,其质控规则和质控个数(Ns)通过图1列线图的图例确定。对于这种关键点的IQC程序,其Ped要高,根据功效函数图其Ped应该有≥0.9的概率发现关键的系统误差。(6)确定夹心IQC设计,选择批长度比HbA1c期望的报告区间大且最接近报告区间的IQC程序。根据功效函数图[17](图2),保证Pfr较低,最好Pfr≤5%;(7)制定IQC方案用于确定每次夹心IQC之间检测的患者标本数和质控品个数。
注:s,标准差;Pfr,假失控率;Ped,误差检查率;N,质控结果个数
图2含西格玛度量的IQC功效函数图
1.3.3Bias和CV的获取[16](1)Bias:通过国家卫生健康委临床检验中心组织的正确度验证计划来评价2种HbA1c检测系统的偏倚。严格按照国家卫生健康委临床检验中心提供的操作指南处理样品,并于每个规定的测定日期检测每批号各1瓶,重复检测5次,取每个批号15个结果的平均值用于评价偏倚。国家卫生健康委临床检验中心生化室(国际临床化学HbA1c实验室网络一级参考方法认证实验室)以IFCC HbA1c参考方法(液相色谱串联质谱法)为质量评价材料定值。本实验室Trinity Premier Hb 9210和Sebia Capilarys 2FP检测系统分别参加了2017年和2018年国家卫生健康委临床检验中心组织的正确度验证计划。(2)CV:来自日常的IQC数据,取正确度验证样品测定日期所用质控品批号的累积在控CV(时间段为:2017年2月1日至2017年6月30日和2018年2月1日至2018年6月30日)。
2 结果
2.12种HbA1c检测系统的Bias和CV2017年Premier Hb 9210、2018年Sebia Capilarys 2FP分析仪的正确度验证结果均满足国家卫生健康委临床检验中心标准(靶值6%)。正确度验证和IQC数据见表1。
2.2制定基于风险的IQC方案 5σ和5.35σ水平下各IQC程序的最大批长度及Ped和Pfr见表2。
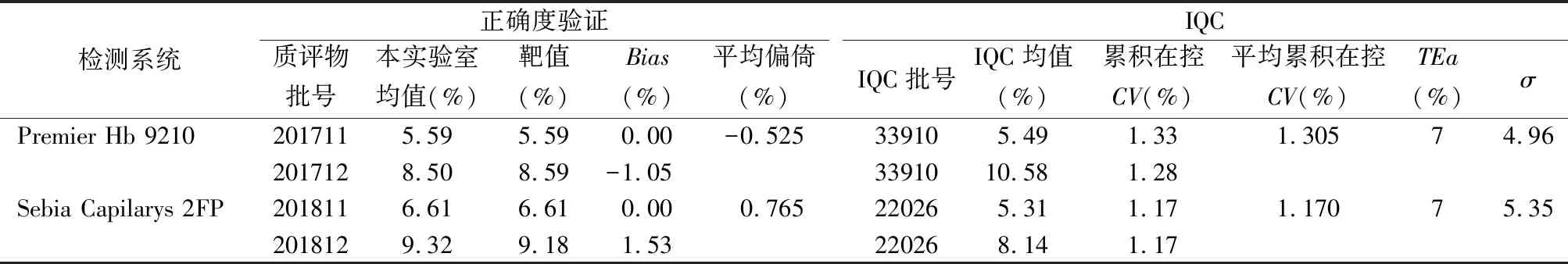
表1 2种HbA1c分析仪正确度验证计划和IQC数据列表
注:平均偏倚等于2次偏倚的算术平均值,平均累积在控CV等于2个水平累积在控CV的算术平均值,σ的计算用平均偏倚和平均累积在控CV。
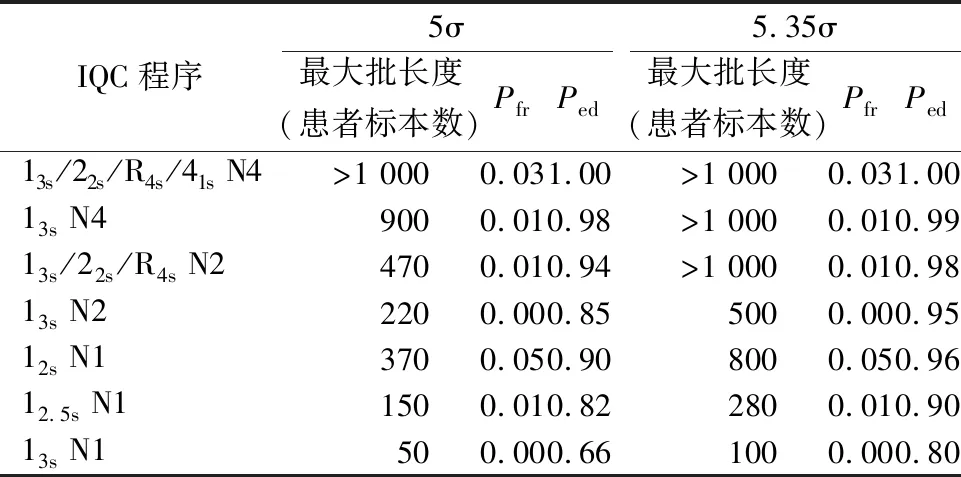
表2 5σ和5.35σ水平下各IQC程序的性能特征表
注:表2中数据通过图1和图2综合得到。当检测系统的西格玛水平为5σ时,在图1中画一条通过横坐标5σ并垂直x轴的直线,这条直线与每个质控程序曲线交点的纵坐标即为该质控程序的批长度,比如该直线与13sN1程序直线交点的纵坐标是50,那么13sN1的批长度是50;然后在图2中也画一条通过横坐标5σ并垂直x轴的直线,该直线与13sN1程序曲线交点的纵坐标即为Ped(Ped=0.66),从图2右侧图例可知13sN1程序的Pfr=0.00。
根据不同西格玛水平下IQC程序性能,制定不同工作量不同西格玛水平下检测系统的IQC方案见表3。
表3中2个案例以及本实验室均采用2水平质控品(C1,C2),因为这能满足ISO 15189:2012[13,18]等管理文件的要求。在案例1中,最大工作量是1 000个患者标本,这2个水平质控品在起始IQC中检测2次(13s/22s/R4s/41sN4),但在后续每隔200个患者标本的IQC中只检测1次(13sN2)。在案例2中,最大工作量是500个患者标本,2水平质控品在起始IQC中只检测1次(13s/22s/R4sN2),接下来每125个患者标本的IQC中每个水平交替只检测1次(12.5sN1)。本实验室Premier Hb 9210分析仪的最大工作量是200个患者标本,起始IQC的2个水平质控品只检测1次(13s/22s/R4sN2),接下来每50个患者标本的IQC中只需对1个水平质控品检测1次(13sN1)。Sebia Capilarys 2FP分析仪起始IQC的2个水平质控品只检测1次(13sN2),接下来每50个患者标本的IQC中只需对1个水平质控品检测1次(13sN=1)。最后,在表3中提供了IQC在控时IQC开支的估计,由于质控品跟患者标本以同样方式检测,检测1个质控品消耗的试剂量跟患者标本相同,所以IQC开支与质控品检测数成正比,因此3种选择的IQC开支分别占总成本的1.4%、1.2%和3.0%。
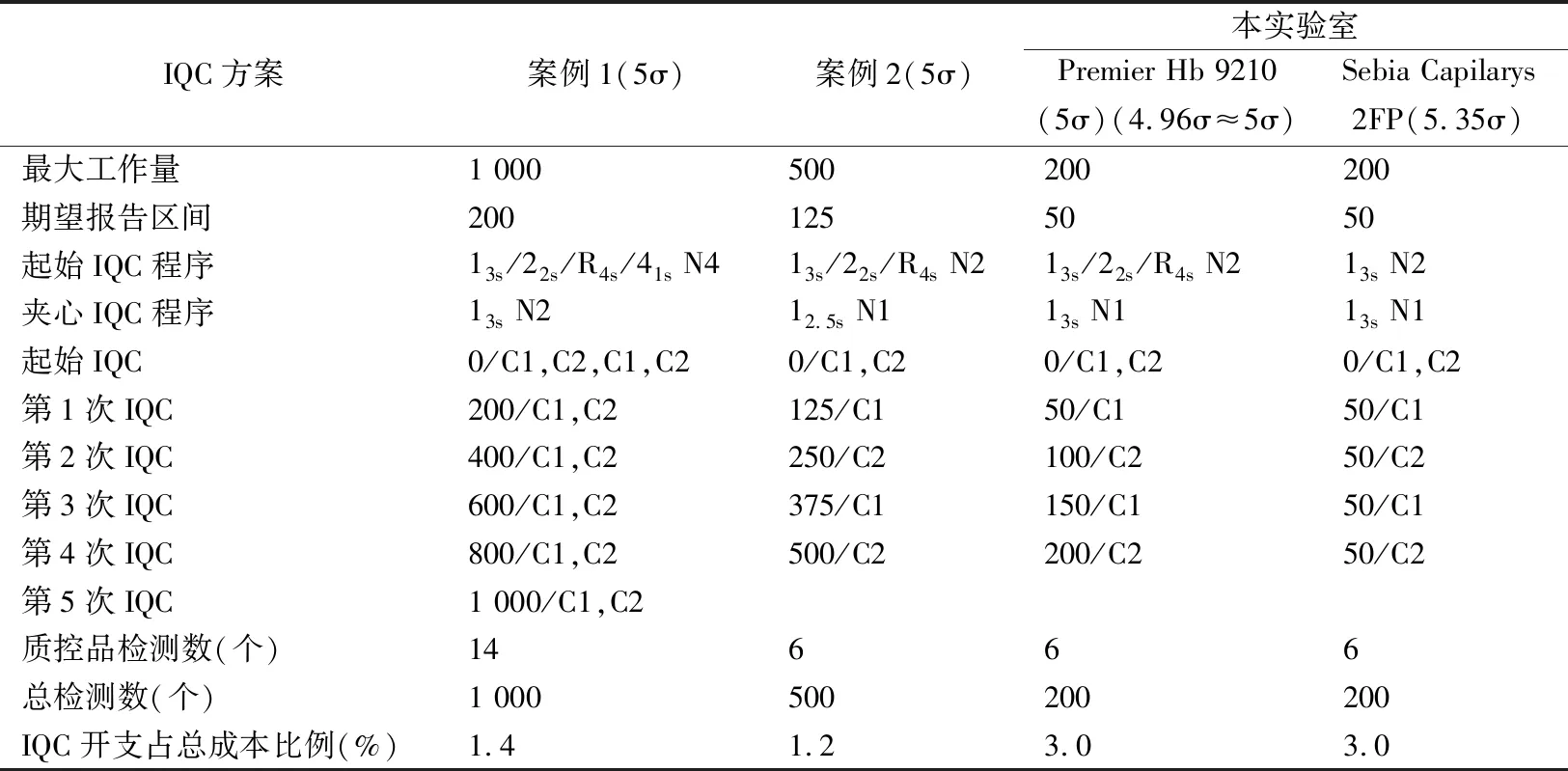
表3 案例1、案例2和2种HbA1c分析仪的IQC方案
注:C1和C2表示2个不同浓度水平质控品;IQC表示室内质量控制。报告区间:即2次患者结果报告之间间隔的标本数,本实验室HbA1c的报告区间是50个标本。以案例1举例说明IQC方案表制定步骤:(1)检测系统的最大工作量是1 000,质量是5σ水平,由于批长度要大于最大工作量,因此从表2可知只能选择13s/22s/R4s/41sN4作为起始IQC程序,且Ped=1.0,大于0.9,满足要求;同理,实验室定义报告区间是200,查表2可知批长度大于200且与200最接近的是批长度=220对应的质控程序13sN2,该质控程序Pfr=0.00,小于5%,满足要求。(2)质控程序选择好之后,再设计质控检测计划,在检测开始时使用起始IQC程序,然后每间隔200个标本使用夹心IQC程序。
3 讨论
2017年Westgard针对IQC情况做了全球性调查,结果显示50%的实验室只在检测开始前做1次质控,另外50%的实验室虽然在一天中做了2次及以上质控,但时间间隔没有理论依据,缺乏一致性。中国实验室的IQC情况也类似[19]。因此,有必要建立客观的标准指导实验室设计多级IQC方案。
设计多级IQC的重要原则是起始IQC要求较高的Ped,用于监控的夹心IQC可使用更简单的规则,质控结果数(N)可以更小。理论上,作为监控的IQC程序其Pfr应该非常低,这样才能使假失控频率降低。IQC程序不能既有较高的Ped又有较低的Pfr,多级IQC可允许一个程序具有高的Ped,另外一个程序具有较低的Pfr。设计的关键取决于错误的高发生率是期望的(起始IQC),还是低发生率是期望的(夹心IQC)[15,17]。在选择Premier Hb 9210检测系统起始IQC规则时,其西格玛度量是5σ,与工作量(200个患者标本)接近的IQC规则是“13sN2”(批长度220),但是其Ped稍微低于期望值0.9,因此选择具有更大批长度的多规则IQC程序(13s/22s/R4sN2)。我们在设计夹心IQC时应使患者风险在报告区间内最小。
多级IQC设计的成本高效益取决于检测程序的西格玛水平。具有5σ或更大的检测系统可以使用简单的IQC设计,容纳较大的工作量,并保持低成本。比如具有6σ的检测程序,绝大部分IQC程序的批长度都>1 000个患者标本,除了规则“13sN1”大约为370个患者标本。其起始IQC可利用“13sN2”规则,接下来的夹心式IQC可使用“13sN1”规则。可选择任何370左右大小的报告区间,IQC成本可能低至每1 000个标本检测5个质控物。对于4σ检测程序,其IQC程序要求更多的质控结果,需要多规则,批长度将更短。对于<3.5σ的程序,甚至需要更复杂、花费更多的IQC策略[16]。因此为了降低IQC成本,最好选择性能较好的检测系统。
西格玛度量IQC批长度列线图为选择适当的IQC规则、IQC结果个数和批长度提供了一种实用的、客观的工具。本研究中列线图只提供了7种常用的IQC程序,对于超出这7种程序之外的情况,无法获得批长度,虽然这7种IQC程序基本能满足实验室的需求,但完善更多IQC程序的批长度列线图仍是本研究下一阶段需要做的工作。

