利福喷汀与利福平治疗肺结核的临床疗效对比
丁 敏 王 伟 李美荣
肺结核是发病率较高、传染性极广的慢性传染病,多发于免疫力低下的老年群体,病变部位主要是侵犯下气道、胸膜、气管、支气管,发生渗出、增殖等结核病变,从而引起肺功能损伤或障碍,严重者更会影响到呼吸道通气功能。患者多表现为咳嗽、咳痰、发热等常见症状,可能伴随乏力、呼吸困难等并发症状[1]。该疾病一旦发作,将会严重影响患者的呼吸功能,降低免疫能力,从而降低患者的生活质量,危及生命安全,因此必须及时治疗并采取高敏感度的药物进行对症治疗。临床多采用药物联合治疗为主,常规一线药物包括吡嗪酰胺、异烟肼等药物,存在一定的不良反应,联合利福霉类药物是临床首选方案,利福喷汀、利福平均为该类药物,可以有效治疗肺结核,但是其安全性及不良反应存在一定的争议[2]。基于此,为了研究不同抗结核方案的安全性与有效性,本研究对利福喷汀与利福平的治疗效果进行对比分析。
1.临床资料
选取2018年6月至2019年6月期间本院收治的78例肺结核患者,按不同的用药方案进行平均分组,观察组给予利福喷汀治疗,对照组给予利福平。观察组39例,男性23例、女性16例,年龄为55~75岁,平均年龄为(60.29±2.43)岁;对照组39例,男性21例、女性18例,年龄为56~73岁,平均年龄为(59.82±2.56)岁。两组患者的一般资料差异均无统计学意义(P>0.05),具有可比性。
诊断标准:符合《肺结核基层诊疗指南(2018年)》[3]中关于肺结核的诊断标准:患者表现出明显的咳嗽、持续2周以上咳痰、咯血等呼吸系统症状以及发热等全身症状,可能伴随呼吸困难、乏力、食欲降低等症状;经过临床X线检测,存在浸润、增殖、纤维钙化性病变的多态性或同时存在以上特征,病变密度不均匀、边缘较清晰,病变进展速度较慢,出现空洞和传播灶的可能性较大。
纳入标准:①符合上述临床症状及影像学诊断标准;②取痰液样本,经结核菌培养显示为阳性;③年龄为20~80岁;④患者签署知情同意书。
排除标准:①根据结核菌培养显示,对试验用药存在耐药反应;②合并肝肾功能、血液系统等重大疾病;③排除疑似病例;④患者精神异常或依从性差或精神异常。
2.治疗方法
两组均给予常用抗结核病药物治疗,包括异烟肼(生产厂家:四川康特能药业有限公司,国药准字:H51021127,0.1g),成人剂量为1次/d,0.3g/d;乙胺丁醇(生产厂家:北大医药股份有限公司,国药准字:H50020501,0.25g),成人剂量为口服0.75g/d,1次/d;吡嗪酰胺(生产厂家:常州制药厂有限公司,国药准字:H32023303,0.25g),成人剂量为口服30mg/(kg·d),每周2次,每次最高不超过4g。
对照组在此基础上联合利福平(生产厂家:河南全宇制药股份有限公司,国药准字:H41023132,0.15g),成人口服,体重<50kg服用450mg/d,体重≥50kg为600mg/d。
观察组联合利福喷汀(生产厂家:河北爱尔海泰制药有限公司,国药准字:H20133047,0.15g),0.6g/次/d,体重<55kg服用剂量需要进行删减,一周2次,两组均连续治疗6月。
3.指标判定
3.1 观察指标 ①肺部功能:应用肺功能测定仪(来源:日本捷斯特CHESTAC-8800)检测治疗前后的肺部功能相关指标,包括FVC、FEV1、TLC指标。②相关因子表达:应用酶联免疫吸附法(ELISA)以及试剂盒(来源:美国R&D公司)检测治疗前后的相关因子表达水平,操作方法如下:采集3ml空腹静脉血,进行常规血清处理,应用ELISA法检测白介素6(IL-6)、干扰素γ(IFN-γ)、CA125。③安全性评价:观察两组患者的不良反应发生率。不良反应包括皮疹、胃肠道反应、药物引起肝损伤、白细胞减少等症状。
3.2 疗效评价标准 参照《肺结核化学疗法》[4]制定临床疗效:根据患者的临床主要症状(咳嗽、咳痰、发热等症状)、痰菌转阴情况、影像学检测病变范围改善情况进行评估。病变吸收=(治疗前病灶部位相加-治疗后病灶部位相加)/治疗前病灶部位相加和。①痊愈:咳嗽、咳痰等呼吸症状及全身伴随发热症状消失;连续3次痰菌检查转阴未复阳;病灶吸收≥50%。②有效:呼吸、全身症状的频率及程度有所缓解,3次痰菌检查阳性率明显下降;病灶吸收处于30%~50%。③无效:呼吸、全身症状的频率及程度无变化甚至加重,3次痰菌检查均为阳性;病灶吸收<30%或出现扩散。有效率=1-无效率。
4.统计学方法
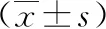
5.结果
5.1 两组患者治疗前后的肺部功能对比 两组治疗后的肺部功能指标(FVC、FEV1、TLC)均出现明显上升,且观察组的上升效果明显优于对照组,P<0.05,差异有统计学意义,见表1。
5.2 两组患者治疗前后相关因子表达对比 经过治疗后,观察组的相关因子表达(IL-6、IFN-γ、CA125)明显低于对照组,P<0.05,差异有统计学意义,见表2。

表2 两组患者治疗前后相关因子表达对比情况
5.3 两组治疗安全性评价对比 观察组的不良反应发生率明显低于对照组,P<0.05,安全性更高,差异有统计学意义,见表3。
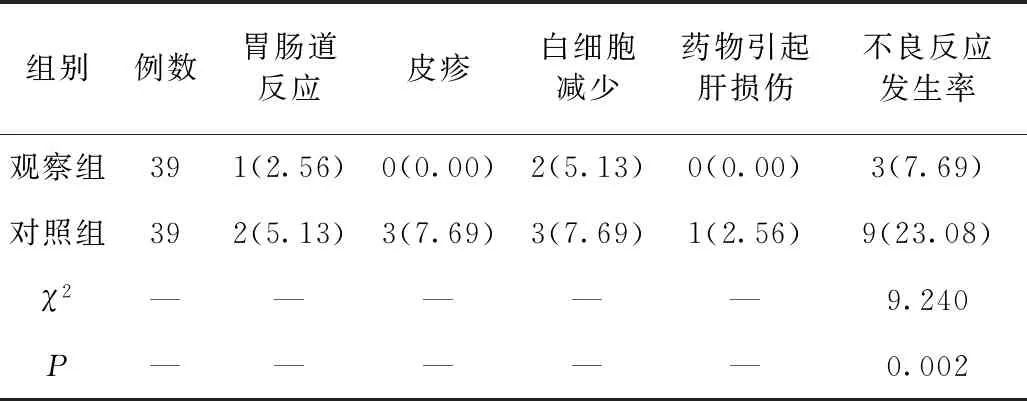
表3 两组治疗安全性评价对比 单位:例(%)
5.4 两组患者的临床疗效对比 观察组的有效率为94.87%,明显高于对照组的有效率(74.36%),P<0.05,差异有统计学意义,见表4。
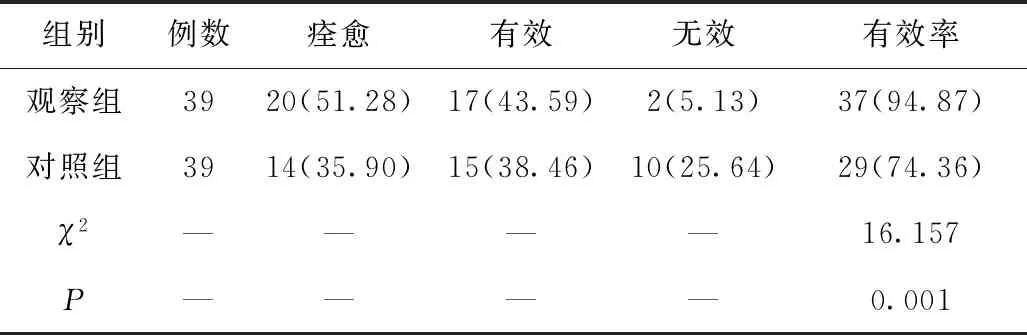
表4 两组患者临床治疗效果对比情况 单位:例(%)
6.讨论
肺结核的潜伏期较长,难以通过非特异性症状及时发现[5],而在潜伏期中患者的身体机能、免疫力均会产生不同程度的改变,随着病情进展,治疗难度也会增加,因此有必要探索更理想的治疗手段。临床治疗主要采用联合规律性用药,但是基础用药的敏感性不高,且产生不良反应、耐药情况的风险较高[6]。本研究显示应用利福喷汀治疗效果显著,可以有效改善患者的临床症状及肺部功能,安全性高。
利福平是临床一线抗结核半合成广谱抗菌药物,应用较广泛,对多种病原菌有较强的抑菌效果,主要是同归口服吸收药效,通过结合聚合酶从而抑制结核杆菌的生成,达到杀菌效果[7]。联合常规抗结核药物具有一定的治疗效果,但出现胃肠道不适、皮疹等不良反应的概率较大,长期服用对肝损伤的影响较大[8]。随着医药技术的发展,利福喷汀等二线抗结核药物的应用逐渐广泛,且副作用较小。利福喷汀是利福平衍生物,同样属于半合成利福霉素类药物,具有广谱杀菌、药效吸收较快等优势,利福喷汀的作用机制是通结合结核杆菌的RNA多聚酶,减少磷酸酯链形成,从而抑制结核杆菌的一系列转录、蛋白质合成过程,达到有效的抑菌效果[9]。结核杆菌对利福喷汀的药物敏感性较高,主要是由于利福喷汀对原核细胞多聚酶有较高的选择性,经过口腔服用,机体会迅速吸收药物,促使其广泛分布在血液、循环系统、器官组织中,且穿透力较强,进入肝脏细胞,与血清蛋白快速结合,加速肝脏组织的代谢与循环过程[10]。临床研究发现在肝脏内该药物的浓度最高,可以充分发挥治疗作用。该药物的主要成分利福霉素对结核杆菌有强抑制作用,不管是处于血液浓度半衰期或高峰期,其药效及抗菌活性远高于利福平;同时利福喷汀药物不易被肠道吸收,对胃肠道的刺激较小,安全性更高。利福喷汀的药物疗效较理想,无须长期服用,可以减少肝脏的长期过度负荷[11]。
本研究结果显示,两组治疗后的肺部功能指标(FVC、FEV1、TLC)均出现明显改善,且观察组的改善效果明显优于对照组(P<0.05)。可能是由于利福喷汀抑菌消炎,缓解肺部功能的炎症反应,降低肺部负荷,改善肺部功能指标[12]。经过治疗后,观察组的相关因子表达(IL-6、IFN-γ、CA125)明显低于对照组(P<0.05)。白细胞介素-6具有诱导淋巴细胞分化产生抗体的作用,IFN-γ可以增强免疫作用。结核病有多种免疫细胞参与,而细胞因子进行信号传递参与反应[13]。利福喷汀具有强抑菌效果,通过抑制结核杆菌达到缓解或降低炎症反应,恢复人体免疫作用[14]。CA125是高分子量糖蛋白,在肺结核疾病中具有高表达,利福喷汀的敏感性高于对照组,经过有效治疗后,肺部组织恢复正常,该因子的释放降低。观察组的不良反应发生率明显低于对照组(P<0.05),因为利福喷汀的蛋白结合率较高,进入人体肝脏细胞中浓度较高,半衰期较长,可以减少服用频率及浓度,间歇性用药可以降低肝脏组织的负荷及损伤,从而降低不良反应[15]。观察组的有效率明显更高(P<0.05),可能是利福喷汀具有抑制结核杆菌蛋白质合成的作用,达到理想的抑菌效果,抗菌能力高于利福丁2~10倍,治疗效果理想,同时对原核细胞多聚酶具有高选择性,加快药效分布与发挥,从而促进肝脏细胞代谢与循环,降低药物副作用。
综上所述,相较于利福平,利福喷汀治疗肺结核临床效果显著,可有效改善咳嗽、咳痰、发热等相关症状,改善肺部功能,降低相关因子表达,安全性更高,值得临床推广。

