肾透明细胞癌卵巢转移2例
吴俊秀 赵明 魏海彬 白虹 张大宏 张琦
肾细胞癌起源于近端小管,是最常见的肾脏肿瘤,占所有成人恶性肿瘤的3%[1];其中肾透明细胞癌是最常见的类型,男女发病比约为2∶1[2]。肾透明细胞癌易转移至肺、骨骼、肾上腺等,但是卵巢转移非常少见,关于肾透明细胞癌卵巢转移的病例鲜有报道[2-6]。浙江省人民医院近5年来收治了2例肾透明细胞癌卵巢转移患者,现将诊治经过报道如下。
例1女,52岁。因“外院体检发现双侧肾占位10 d”于2017年10月30日至浙江省人民医院就诊。患者偶有左侧腰部隐痛不适,程度较轻,无畏寒、发热,无腰腹痛,无血尿,无恶心、呕吐等不适。外院B超检查示:左肾下极见中等回声占位,大小约44 mm×40 mm,右肾皮质内见稍高回声,大小约10 mm×9 mm。CT检查示:左肾下极富血供占位性病变,考虑肾透明细胞癌的可能性大。无肿瘤家族史。入院查体:神志清,精神可,皮肤巩膜无黄染,心肺听诊无明显异常;腹平软,无压痛及反跳痛,包块未及,肠鸣音正常,无移动性浊音,无肾区叩痛,输尿管行径处无压痛点,膀胱充盈一般,外生殖器无殊,双下肢无水肿,病理征阴性。B超检查示:左肾实质可见偏低回声团,切面大小约52 mm×34 mm,边界清,内回声欠均匀,右肾实质可见偏高回声团,切面大小约11 mm×10 mm,边界清,内回声欠均匀,集合系统未见分离。结合病史初步诊断:(1)左肾占位性病变;(2)右肾错构瘤。与患者沟通后,10月31日行达芬奇辅助腹腔镜左肾部分切除术,手术顺利,患者恢复良好。术后病理检查提示肾透明细胞癌,免疫组化染色结果示:CAIX(+)、PAX-8(+)、TFE3(-)、TFE-B(-)、E-cadherin(-)、EMA(+)、Vimentin(灶性 +)、Inhibin(-)、P504S(+)、CAM5.2(+)、RCC(-)、CK7(-)、CD10(+)、CD117(-)、CK19(-)。术后9个月,外院复查B超示:左卵巢可见偏低回声团,边界清,内回声欠均匀,考虑卵巢囊肿;同时行腹腔镜左侧附件切除术+子宫肌瘤切除术+取环术,术后病理检查提示转移性透明细胞癌。2018年10月19日至浙江省人民医院复查,与患者沟通同意后行基因检测,结果显示存在VHL变异,遂予以索拉非尼治疗,目前随访未发现疾病有进展。
例2女,40岁。因“左下腹疼痛2 d”于2016年9月26日至浙江省人民医院就诊。患者2 d前出现持续性左下腹胀痛,约1 h后自行缓解,后出现阵发性左下腹痛,无放射痛,无恶心、呕吐,无发热、腹泻,无排尿困难,遂至当地医院就诊,CT检查示:左肾肿瘤。无肿瘤家族史。入院查体:神清,精神可,皮肤巩膜无黄染,心肺听诊无明显异常,腹平软,左下腹压痛,无反跳痛,包块未及,肠鸣音正常,无移动性浊音,无肾区叩痛,输尿管行径处无压痛点,膀胱充盈一般,双下肢无水肿,病理征阴性。肾动脉CT血管造影检查示:左肾外侧见团块状影,大小约51.7 mm×48.5 mm,增强后不均质强化,内见斑片状低密度坏死。结合病史初步诊断:(1)左肾恶性肿瘤。与患者沟通后,于9月29日行腹腔镜左肾癌根治术,手术顺利,患者恢复良好。术后病理检查提示肾透明细胞癌,免疫组化染色结果示:PAX-8(弱 +)、TFE3(-)、E-cadherin(+)、EMA(部 分 +)、Vimentin(+)、Inhibin(-)、P504S(部分+)、CAM5.2(部分 +)、RCC(-)、CK7(-)、CD10(+)、CD117(-)、CK19(-)。随后 2 年定期复查。2019年5月31日外院复查CT时发现盆腔占位(外院CT检查示:盆腔左侧见一类圆形软组织肿块,大小约38mm×44 mm,考虑卵巢转移性肿瘤),遂至浙江省人民医院妇科就诊。患者无恶心、呕吐,无畏寒、发热,无腹痛等不适,月经规律。入院查体:左附件区增厚感,无压痛,右附件区未及肿块,无压痛。腹部增强CT检查示:左侧附件区见动脉期明显强化肿块影,大小约42 mm×39 mm,静脉期减低,盆腔内积液,盆腔淋巴结未见肿大,见图1。盆腔增强MRI检查示:左侧附件区可见大小约40 mm×44 mm团块影;T2WI高信号及更高信号影,其内见低信号分隔,T1WI等、低信号,DWI高信号,ADC部分低信号,增强后实性成分强化明显、持续强化,囊性成分强化不明显,边界欠清晰。初步诊断:(1)盆腔肿物;(2)左肾恶性肿瘤术后。6月11日行腹腔镜妇科晚期恶性肿瘤减灭(左侧附件切除术+右侧卵巢活检+大网膜部分切除术+腹膜多点活检)+肠粘连松解术,手术顺利,患者恢复良好。术后病理检查提示:(1)左侧附件肿块转移性肾透明细胞癌;(2)右侧卵巢未见癌转移。免疫组化染色结果示:PAX-8(+)、PAX-2(弱 +)、CD10(+)、CAIX(+)、Vimentin(+)、CK7(-)、Napsin A(-)、HNF1β(+)、P504S(灶 +)、ER(-)、PR(-)、WT1(-),见图2。与患者沟通同意后行基因检测,结果显示存在VHL变异。术后6个月行PET-CT检查,未发现转移,目前尚处于观察随访中,未给予索拉非尼治疗。
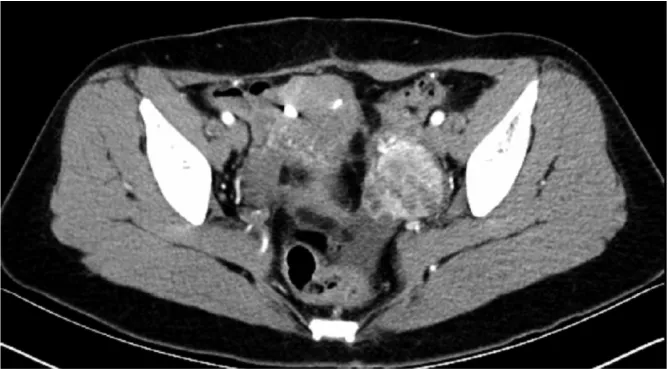
图1 腹部增强CT检查所见

图 2 免疫组化染色结果所见[a:CAIX(+);b:PAX-8(+);c:CD10(+);×100]
讨论研究表明,肾细胞癌卵巢转移是指肾静脉的癌栓转移至卵巢血管[7]。绝经后是发病高峰期,可能归因于卵巢萎缩和血液灌注减少导致血管硬化,使得癌栓易在此处停留[8]。国外病例报道左、右肾透明细胞癌发生卵巢转移的数量无明显差异,而且发生双侧、同侧、对侧卵巢转移的数量也无明显差异[2-4]。肾透明细胞癌卵巢转移患者多数无明显症状及体征,少数患者可触及腹部肿块,少数可出现体重减轻、发热、疲劳、无力、腹胀、腹痛、阴道出血、月经不规则[2]。国内报道的2例肾细胞癌卵巢转移患者均无明显临床症状[5-6],而本文报道的2例患者也无明显症状。X线检查示子宫前方包块,内见粗细不均的纤维光带;超声检查示盆腔内实性包块,界清,形态欠规整,内部回声不均匀,其内见多处不规则液性暗区,与子宫后壁分界不清;PET-CT检查示附件区囊实性肿物[5-6]。而本文报道的1例患者B超检查示偏低回声团,边界清,内回声欠均匀;1例患者CT检查示类圆形软组织肿块,动脉期明显强化,静脉期减低。可见,影像学检查在肾透明细胞癌卵巢转移诊断中的作用有限。但病理学检查具有较好的诊断价值。在显微镜下,肾透明细胞癌可见囊性、实性、管状和乳头状区域,特征是肿瘤细胞周围存在丰富的血管网;肿瘤细胞胞质清晰或嗜酸性,核仁突出;在中央核区,肿瘤细胞通常缺乏明显的多形性[2]。肾透明细胞癌主要表达 PAX-8、PAX-2、EMA、Vimentin、CD10、低分子量细胞角蛋白、波形蛋白[9]。本文报道的2例患者免疫组化结果显示,肿瘤细胞表达PAX-8、EMA、Vimentin、P504S、CAM5.2、CD10。研究表明,肾透明细胞癌的发生、发展是由许多基因参与的[9]。VHL是抑癌基因,而肾细胞癌中存在VHL基因突变[10]。VHL位于染色体3P25-26区[11],具有调节转录和细胞周期、稳定细胞相关生长基因的功能,其缺失、突变和超甲基化与肾细胞癌的发生相关[12]。本组2例患者均存在VHL变异。
在治疗方面,手术是目前主要的方法,常用的术式为子宫加双侧输卵管卵巢切除[2]。靶向药物治疗是一种新型的治疗方式,其中血管内皮生长因子抑制剂贝伐单抗、舒尼替尼、索拉非尼等已用于治疗肾细胞癌转移[13]。Anagnostou等[8]报道了1例肾透明细胞癌卵巢转移患者接受手术后使用干扰素治疗,9个月后发现疾病进展,随后使用舒尼替尼治疗,病情稳定,总生存期超过4年。本文报道的1例患者在卵巢转移灶切除术后给予索拉非尼,目前疾病未进展。转移性肾细胞癌患者的预后较差,5年生存率仅 5%~10%[13]。Koufopoulos等[2]报道卵巢转移发现间隔为3个月~21年,部分患者还存在其他部位转移,9例患者发病后2~17年内发生疾病进展,10例患者病死。而本文报道的1例患者术后9个月发现卵巢转移,1例患者术后33个月发现卵巢转移,目前均未见疾病进展。
综上所述,肾透明细胞癌发生卵巢转移的情况较为少见,术前症状及相关检查不能确诊,主要依靠病理学检查确诊。手术是目前的主要治疗方法,辅助治疗也有一定的作用。

