血清Hcy在慢性心衰患者中的表达与超声指标的相关性研究
任锋 ,姚旗 ,王宏伟
(南阳市中心医院,1.超声科;2.供应室;3.检验科,河南 南阳 473000)
心力衰竭[1](heart failure,HF)又称心衰,是一种心脏循环障碍症候群,主要由心脏舒张或收缩功能异常引起。慢性心衰[2,3](CHF)是指持续存在的心力衰竭状态,其在我国发病率达0.9%,就诊后1年内死亡率达22.1%,就诊后5年内生存率不足20.0%,对患者生命造成极大威胁。CHF患者临床症状体征不具备特异性,多由运动耐力下降出现端坐呼吸、阵发性夜间呼吸困难或乏力而就医,因此寻找早期诊断的客观指标对CHF患者预后改善尤为重要。高半胱氨酸(Hcy)[4,5]是蛋氨酸代谢过程中产生的含硫基氨基酸,可促进氧自由基产生,损伤血管内皮细胞(VEC),引发动脉粥样硬化(AS),从而增加心血管疾病发病风险。有研究[6]认为Hcy是CHF发生的危险因素,但目前缺乏相关研究验证此观点。本研究检测血清Hcy在慢性心衰患者中的水平,分析其与CHF患者超声心功能指标的相关性,旨在探讨Hcy与CHF之间的关系,为CHF诊治提供新的方向。
1 对象与方法
1.1 研究对象 经本院伦理委员会批准,选择2017年12月-2018年12月我院心内科收治的CHF患者72例作为CHF组,男43例,女29例;平均年龄(62.80±10.64)岁;按照美国纽约心脏病协会(New York Heart Association,NYHA)心功能分级为Ⅱ级25例、Ⅲ级29例、Ⅳ级18例;心脏原发疾病为扩张性心肌病10例、冠心病26例、风湿性心脏病14例、高血压性心脏病22例。另选同期在我院健康体检者72例作为Ctrl组,男45例,女27例;平均年龄(61.91±10.39)岁。纳入标准:⑴CHF组入选者均符合CHF诊断标准,且经实验室检查、影像学检查及心电图等证实;⑵入组前半个月内无严重创伤;⑶CHF组患者NYHA分级均在Ⅱ~Ⅳ级;⑷未合并恶性肿瘤或脑血管疾病(CVD);⑸所有入选者对本研究内容知情同意。排除标准:⑴合并肝肾肺等器官组织严重功能不全;⑵合并感染性疾病;⑶依从性不好者;⑷合并血液系统疾病或全身免疫性疾病;⑸近期发生心肌梗死或甲亢;⑹入组前半个月内服用抗癫痫、抗炎症或激素类药物。两组年龄、性别比较差异无统计学意义(P>0.05)。
1.2 研究方法 所有研究对象入院后,采用欧姆龙电子血压计(广州市疗康医疗器械有限公司)测量收缩压(SBP)、舒张压(DBP),采集晨起外周静脉血4 ml置于肝素抗凝管 (上海恒远生物科技有限公司中静置0.5h,用离心机 (德国艾本德股份公司)4000 r/min离心5 min,分离血清,采用西门子ADVIA 24 00全自动生化分析仪检测血清Hcy、低密度脂蛋白胆固醇(LDL-C)、甘油三酯(TG)、总胆固醇(TC)水平,采用Philip-siE33心脏彩色多普勒超声诊断仪检测超声心功能指标:包括左室后壁厚度(LVPWT)、室间隔厚度(IVST)、左室射血分数(LVEF)、左室舒张末期内径(LVEDd),所有操作由同一名经验丰富医师严格按照操作说明书进行。
1.3 统计学方法 采用spss22.0软件进行统计分析。计量资料两组间采用t检验,多组间比较采用单因素方差分析,多重比较采用SNK-q检验;相关性分析采用Pearson相关。P<0.05为差异具有统计学意义。
2 结果
2.1 两组常规指标比较 CHF组LDL-C水平及SBP、DBP与Ctrl组比较差异无统计学意义 (P>0.05);CHF组TC水平明显低于Ctrl组,差异有统计学意义 (P<0.05);CHF组TG水平明显高于Ctrl组,差异有统计学意义(P<0.05),见表 1。
表1 两组常规指标比较()

表1 两组常规指标比较()
指标 Ctrl组(n=72)SBP(mmHg)DBP(mmHg)TC(mmol/L)LDL-C(mmol/L)TG(mmol/L)P 136.50±15.88 75.61±7.55 4.76±1.11 2.75±0.80 0.96±0.29 CHF 组(n=72) t 137.59±13.60 77.79±8.19 3.67±0.79 2.52±0.76 1.39±0.68 0.442 1.660 6.788 1.768-4.935 0.659 0.096<0.001 0.079<0.001
2.2 两组血清Hcy水平及超声心功能指标比较CHF 组血清 Hcy水平及 LVPWT、IVST、LVEDd明显高于 Ctrl组,差异有统计学意义(P<0.05);CHF组LVEF明显低于Ctrl组,差异有统计学意义(P<0.05),见表 2。
表2 两组血清Hcy水平及超声心功能指标比较()

表2 两组血清Hcy水平及超声心功能指标比较()
指标 Ctrl组(n=72)Hcy(μmol/L)LVPWT(mm)IVST(mm)LVEDd(mm)LVEF(%)P 9.80±3.39 8.19±0.92 8.11±0.80 40.19±8.18 61.12±4.68 CHF 组(n=72) t 25.65±6.30 9.11±1.59 9.81±1.95 51.40±5.61 39.79±3.20-18.799-4.249-6.781-9.590 31.924<0.001<0.001<0.001<0.001<0.001
2.3 不同心功能分级CHF患者血清Hcy水平比较心功能分级为Ⅲ级的CHF患者血清Hcy水平显著高于Ⅱ级,差异有统计学意义(P<0.05);心功能分级为Ⅳ级的CHF患者血清Hcy水平显著高于Ⅲ级,差异有统计学意义(P<0.05),见表 3。
表3 不同心功能分级CHF患者血清Hcy水平比较()

表3 不同心功能分级CHF患者血清Hcy水平比较()
注:与Ⅱ级比较,aP<0.05;与Ⅲ级比较,bP<0.05
分组 例数Ⅱ级Ⅲ级Ⅳ级25 29 18 FP/ /Hcy(μmol/L)21.49±5.80 26.71±6.19a 31.31±6.38ab 13.812<0.001
2.4 CHF患者血清Hcy水平与各超声指标的相关性 CHF患者血清Hcy水平与LVPWT、IVST无相关性 (P>0.05),CHF患者血清Hcy水平与LVEDd呈正相关(P<0.05),CHF患者血清Hcy水平与LV EF 呈负相关(P<0.05),见表 4、图 1。

表4 CHF患者血清Hcy水平与各超声指标的相关性
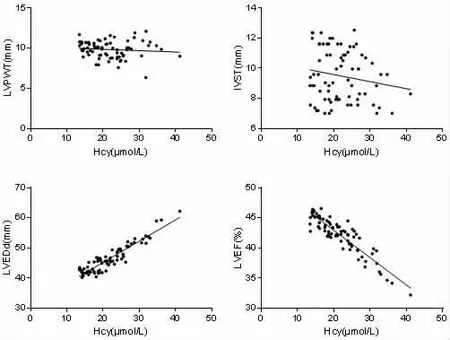
图1 CHF患者血清Hcy水平与各超声指标的相关性
3 讨论
CHF是高血压性心脏病、风湿性心脏病、心肌炎、冠心病(CHD)等心脏疾病病情发展的终末阶段[7],其发病机制涉及心室重构、炎症损伤、神经内分泌失调等,呼吸道感染、严重心率失常、心脏负荷过大、不当活动及情绪等亦为CHF的常见诱发因素[8]。临床上常以减低心脏负荷、消除淤血、增加心输出量、延缓心脏重构作为CHF治疗目标[9],以降低CHF病死率,但由于CHF早期症状无特异性,部分患者就诊时病情已处于严重阶段,因而尽早诊治是降低CHF病死率和改善预后的关键。
有研究[6]认为血清Hcy与CHF发生有密切联系,Hcy为一种含硫氨基酸,蛋氨酸代谢过程中的中间产物,其可破坏VEC,诱导血管内平滑肌细胞增生,导致血管内皮增厚,引起血管舒缩功能障碍,从而促进AS形成[10]。Hcy还可通过氧化应激(OS)损伤血管,使血小板黏附聚集,促进炎症损伤及血栓形成,从而参与CHF进展,增加心血管事件(MACE)风险[11]。有研究证实[12]维生素E水平降低、药物使用等因素可引起Hcy升高,而Hcy水平过高易引起高血压患者左心腔扩大伴舒张性、左心室肥厚、收缩性心功能不全,加重病情。且有研究显示[13]血清Hcy水平>15μmol/L的CHD患者5年内病死率(24.43%)明显高于血清Hcy水平<9 μmol/L的CHD患者(3.75%),研究还显示CHD患者血清Hcy水平每下降3.0 μmol/L,则发生缺血性心脏病、静脉血栓、脑血管意外(CVA)的机率分别下降16.33%、26.03%、23.95%。本研究中,CHF组血清Hcy水平及LVPWT、IVST、LVEDd 明显高于 Ctrl组,LVEF明显低于Ctrl组,LVEF与心肌收缩能力有关,心肌收缩能力越强,LVEF越高,正常情况下LVEF≥50%,若小于此值即提示心功能不全[14]。此外,不同心功能分级CHF患者血清Hcy水平存在明显差异,这与国外文献报道相符[15],说明hHcy水平与CHF严重程度显著相关,可作为CHF预后的独立预测因子。目前Hcy引起CHF具体机制尚不清楚,我们猜测Hcy可能通过激活基质金属蛋白酶(MMP)诱导炎症因子、氧自由基释放,造成心肌细胞自我凋亡、胶原增生及心肌间质纤维化,使心肌结构重构,引起心脏功能障碍而发生CHF。同时,Pearson相关性分析显示,CHF患者血清Hcy水平与LVEDd呈正相关,CHF患者血清Hcy水平与LVEF呈负相关,说明CHF患者血清Hcy水平与超声心功能指标相关,提示血清Hcy有望成为反映CHF病情变化的有效指标。
综上所述,血清Hcy在慢性心衰患者中的水平显著升高,且随着心功能分级的增加而增加,同时其水平与LVEDd呈正相关,与LVEF呈负相关。

