胃炎灵颗粒剂微生物限度检查方法验证
马海玲,张咏梅,沈花,钱伟
胃炎灵颗粒剂为医院制剂,由白芍、香附、枳实、川楝子、柴胡、党参、黄芪及白术等中药组成,功能疏肝理气、清肝泄热、解痉止痛。临床治疗胆汁反流性胃炎疗效显著。本方多药合用,疏肝郁,安中焦,使脾胃升清降浊气化复常。
中药制剂在生产中的各个环节极易被微生物污染,影响药品的质量及安全,因此药品的微生物检验和微生物限度控制是保障药品安全性的一项重要举措[1]。微生物计数法包含平皿法、薄膜过滤法以及最可能数法,平皿法是微生物计数方法中最常用且应用较广的一种试验方法。本研究于2018年8—12月参考2015版《中华人民共和国药典》四部通则1105(微生物计数法)和1106[2](控制菌检查法)建立胃炎灵颗粒剂的微生物限度检查方法,并对该方法进行验证,以保证胃炎灵颗粒剂的质量,提高检测效率。
1 仪器与材料
1.1 仪器Milliflex Plus全自动微生物过滤系统(密理博公司)、BHC-1300ⅡA2型生物安全柜(苏净集团苏州安泰空气技术有限公司)、HH-B11-500BS-Ⅱ电热恒温培养箱(上海跃进医疗器械有限公司)、LMQ-C51L立式灭菌器(山东新华医疗器械股份有限公司)、Transferpette-S移液器(德国普兰德公司)、HH-W21-600S电热恒温水浴箱(上海跃进医疗器械厂)、MJ-150-Ⅱ霉菌培养箱(上海索谱仪器有限公司)、AUX220电子天平(日本岛津公司)。
1.2 菌种枯草芽孢杆菌[CMCC(B)63501-2a18]、铜绿假单胞菌[CMCC(B)10104-2a16-1]、金黄色葡萄球菌[CMCC(B)26003-5a23-1]、大肠埃希菌[CMCC(B)44102-3a28-1]、白色念珠菌[CMCC(B)98001-2a11]、黑曲霉[CMCC(B)98003-2a11],以上菌种均购于中国食品药品检定研究院,均为第三代。
1.3 培养基胰酪大豆胨液体培养基(批号20161223)、麦康凯液体培养基(批号20161222)、沙氏葡萄糖液体培养基(批号20160204)、胰酪大豆胨琼脂培养基(批号20161219)、麦康凯琼脂培养基(批号20161107)、沙氏葡萄糖琼脂培养基(批号20161123)、PH7.0氯化钠-蛋白胨缓冲液(批号20161108),上述培养基均购于青岛高科园海博生物技术有限公司,培养基适用性试验符合2015版《中华人民共和国药典》规定。4-甲基伞形酮葡糖苷酸培养基(批号20170721),购于北京牛牛基因技术有限公司。
1.4 样品胃炎灵颗粒剂(规格:10克/袋;批号170206、170814、180319),自制。
2 方法与结果
2.1 菌液制备(1)将枯草芽孢杆菌、铜绿假单胞菌、金黄色葡萄球菌接种至胰酪大豆胨液体培养基中,32℃培养24 h。吸取1 mL枯草芽孢杆菌、铜绿假单胞菌、金黄色葡萄球菌的胰酪大豆胨液体培养物,加9 mL PH7.0无菌氯化钠-蛋白胨缓冲液,采用10倍系列稀释,使菌落数不大于100 CFU/mL。(2)将白色念珠菌接种至沙氏葡萄糖液体培养基中,25℃培养48 h。取1 mL白色念珠菌的沙氏葡萄糖液体培养物,加9 mL PH7.0无菌氯化钠-蛋白胨缓冲液,采用10倍系列稀释,使菌落数不大于100 CFU/mL。(3)将黑曲霉接种至沙氏葡萄糖琼脂斜面培养基中,25℃培养7 d,取斜面培养物,用5 mL含0.05%(mL/mL)聚山梨酯80的PH7.0无菌氯化钠-蛋白胨缓冲液洗脱,制备成孢子混悬液[3]。吸取1 mL混悬液,加9 mL含0.05%(mL/mL)聚山梨酯80的PH7.0无菌氯化钠-蛋白胨缓冲液,采用10倍系列稀释,使孢子数不大于100 CFU/mL。
2.2 供试品溶液的制备从同一批次的两个不同包装中共称取胃炎灵颗粒剂10 g,加入PH7.0无菌氯化钠-蛋白胨缓冲液至100 mL,混匀,作为1∶10的供试品溶液。
2.3 需氧菌总数计数方法的验证
2.3.1 常规法
2.3.1.1 试验组 取5份9.9 mL 1∶10供试液,分别加入2.1项下的相应稀释级别的5种试验菌株菌悬液0.1 mL,混匀,使最终试验组中菌落数不大于100 CFU/mL。分别吸取1 mL上述含菌供试液于平皿中,平行操作制备2块平皿,加入胰酪大豆胨琼脂培养基,混匀,32℃倒置培养,培养结束后计数。
2.3.1.2 菌液对照组 取5份9.9 mL PH7.0无菌氯化钠-蛋白胨缓冲液,分别加入2.1项下的相应稀释级别的5种试验菌株菌悬液0.1 mL,混匀,使最终菌液对照组中菌落数不大于100 CFU/mL。其余操作同2.3.1.1试验组。
2.3.1.3 供试品对照组 取9.9 mL 1∶10供试液,加入PH7.0无菌氯化钠-蛋白胨缓冲液0.1 mL,不加菌悬液,混匀。其余操作同2.3.1.1试验组。
2.3.1.4 回收率测定结果 试验组平均菌落数与供试品对照组平均菌落数的差值与菌液对照组平均菌落数的比值即为各试验菌株的回收率[4-6]。结果见表1。
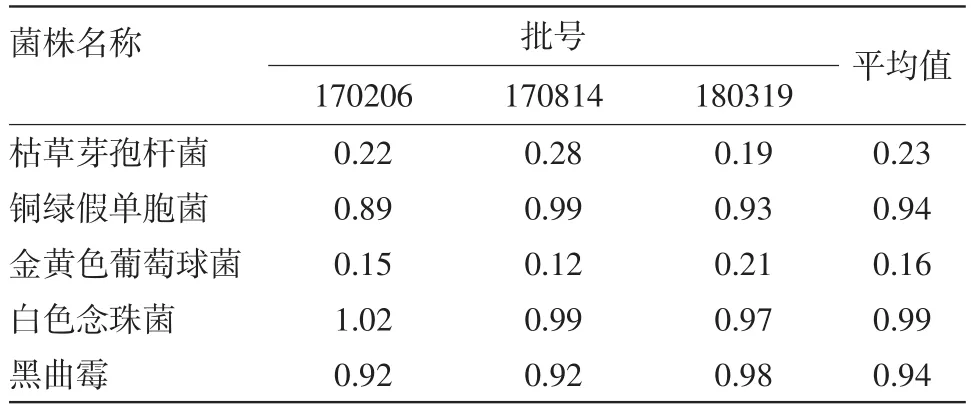
表1 常规法测定不同批号胃炎灵颗粒剂需氧菌总数回收率结果
由结果可知,铜绿假单胞菌、白色念珠菌、黑曲霉的回收率均在0.50~2.00范围内。枯草芽孢杆菌、金黄色葡萄球菌的回收率分别为0.23、0.16,均低于0.50,常规法不适宜用于需氧菌总数的测定,需更换检测方法。
2.3.2 培养基稀释法
2.3.2.1 试验组 取2份9.9 mL 1∶10供试液,分别加入相应稀释级别的枯草芽孢杆菌和金黄色葡萄球菌菌悬液0.1 mL,混匀,使最终试验组中菌落数不大于100 CFU/mL。吸取0.2 mL含菌供试液于平皿中,平行操作制备5块平皿,加入胰酪大豆胨琼脂培养基,混匀,32℃倒置培养,培养3 d结束后测定5块平皿菌落数之和。
2.3.2.2 菌液对照组 取2份9.9 mL PH7.0无菌氯化钠-蛋白胨缓冲液,分别加入相应稀释级别的枯草芽孢杆菌和金黄色葡萄球菌菌悬液0.1 mL,混匀,使最终菌液对照组中菌落数不大于100 CFU/mL。其余操作同2.3.2.1试验组。
2.3.2.3 供试品对照组 取9.9 mL 1∶10供试液,加入PH7.0无菌氯化钠-蛋白胨缓冲液0.1 mL,混匀,不加菌悬液。其余操作同2.3.2.1试验组。
2.3.2.4 回收率测定结果 结果见表2。
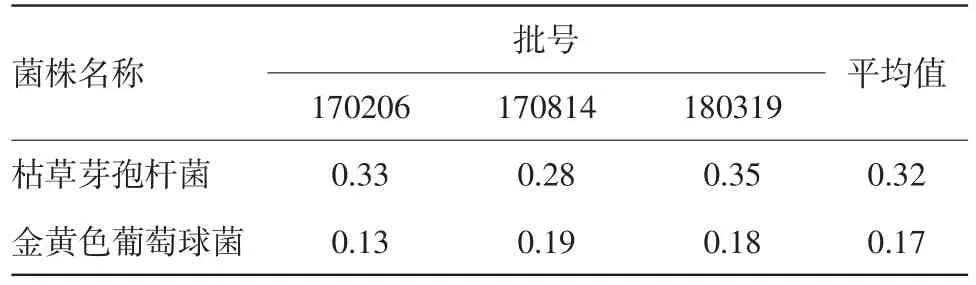
表2 培养基稀释法测定不同批号胃炎灵颗粒剂枯草芽孢杆菌、金黄色葡萄球菌回收率结果
由结果可知,枯草芽孢杆菌、金黄色葡萄球菌的回收率分别为0.32、0.17,均低于0.50,培养基稀释法不适宜用于上述2种试验菌的检测,需更换检测方法。
2.3.3 薄膜过滤法
2.3.3.1 试验组 取10 mL 1∶10供试液,用100 mL PH7.0无菌氯化钠-蛋白胨缓冲液冲洗,冲洗3次,在最后1次冲洗液中分别加入相应稀释级的枯草芽孢杆菌和金黄色葡萄球菌菌悬液0.1 mL,过滤,取出滤膜,使菌面朝上放置于预制的胰酪大豆胨琼脂培养基平板上,置于32℃培养箱中倒置培养3 d后计数。
2.3.3.2 菌液对照组 分别取枯草芽孢杆菌和金黄色葡萄球菌菌悬液0.1 mL,用100 mL PH7.0无菌氯化钠-蛋白胨缓冲液冲洗菌悬液,过滤,取出滤膜。其余操作同2.3.3.1试验组。
2.3.3.3 供试品对照组 取10 mL 1∶10供试液,用100 mL PH7.0无菌氯化钠-蛋白胨缓冲液冲洗,不加菌悬液,冲洗3次,过滤,取出滤膜。其余操作同
2.3.3.1 试验组。
2.3.3.4 回收率测定结果 结果见表3。

表3 薄膜过滤法测定不同批号胃炎灵颗粒剂枯草芽孢杆菌、金黄色葡萄球菌回收率结果
由结果可知,枯草芽孢杆菌和金黄色葡萄球菌的回收率在0.50~2.00范围内,说明薄膜过滤法可用于胃炎灵颗粒剂需氧菌总数的计数。
2.4 霉菌和酵母菌总数计数方法的验证
2.4.1 试验组 取2份9.9 mL 1∶10供试液,分别加入相应稀释级别的白色念珠菌菌悬液、黑曲霉孢子悬液0.1 mL,混匀,使最终试验组中菌落数不大于100 CFU/mL。分别吸取1 mL上述含菌供试液于平皿中,平行操作制备2块平皿,加入沙氏葡萄糖琼脂培养基,混匀,25℃倒置培养5 d后计数。
2.4.2 菌液对照组 取2份9.9 mL PH7.0无菌氯化钠-蛋白胨缓冲液,分别加入相应稀释级别的白色念珠菌菌悬液、黑曲霉孢子悬液0.1 mL,混匀,使最终菌液对照组中菌落数不大于100 CFU/mL。其余操作同2.4.1试验组。
2.4.3 供试品对照组 取9.9 mL 1∶10供试液,加入PH7.0无菌氯化钠-蛋白胨缓冲液0.1 mL,不加菌悬液,混匀。其余操作同2.4.1试验组。
2.4.4 霉菌和酵母菌总数回收率测定结果 结果见表4。

表4 常规法测定不同批号胃炎灵颗粒剂霉菌和酵母菌总数回收率结果
由结果可知,白色念珠菌、黑曲霉的回收率均在0.50~2.00范围内,说明常规法可用于胃炎灵颗粒剂霉菌和酵母菌总数的计数。
2.5 控制菌检查方法的验证
2.5.1 菌液制备 将大肠埃希菌接种至胰酪大豆胨液体培养基中,置于32℃培养箱中培养24 h,吸取1 mL大肠埃希菌的胰酪大豆胨液体培养物,加9 mL PH7.0无菌氯化钠-蛋白胨缓冲液,采用10倍系列稀释,使菌落数不大于100 CFU/mL。
2.5.2 供试品溶液的制备 同2.2项。
2.5.3 大肠埃希菌检查方法适用性试验
2.5.3.1 试验组 取9.9 mL 1∶10供试液,加入0.1 mL大肠埃希菌菌悬液,两者混匀后接种至100 mL胰酪大豆胨液体培养基中,32℃培养24 h。取上述培养物1 mL接种至100 mL麦康凯液体培养基中,42℃培养48 h。取麦康凯液体培养物,在麦康凯琼脂培养基上划线接种,32℃倒置培养72 h[7]。观察结果。
2.5.3.2 供试品对照组 取10 mL 1∶10供试液接种至100 mL胰酪大豆胨液体培养基中,其余操作同2.5.3.1试验组。
2.5.3.3 阳性对照组 取大肠埃希菌菌悬液0.1 mL,接种至100 mL胰酪大豆胨液体培养基中,其余操作同2.5.3.1试验组。
2.5.3.4 阴性对照组 取10 mL PH7.0无菌氯化钠-蛋白胨缓冲液接种至100 mL胰酪大豆胨液体培养基中[8],其余操作同2.5.3.1试验组。
2.5.4 结果判断 见表5。

表5 控制菌检查结果
由结果可知,试验组、阳性对照组有菌落生长,鉴定试验呈阳性,可判定检出大肠埃希菌;供试品对照组、阴性对照组无菌落生长。说明胃炎灵颗粒剂的控制菌检查可采用常规法。
3 讨论
胃炎灵颗粒剂为中药复方制剂,通过多味药的协同作用发挥药效,成分复杂,其中某一成分的抑菌作用都有可能会影响微生物限度检查方法的准确性[9]。采用常规法和培养基稀释法测定5种试验菌的回收率时,金黄色葡萄球菌和枯草芽孢杆菌的回收率均低于0.50。大量研究表明白芍、黄连、栀子、蒲公英、土茯苓均对金黄色葡萄球菌有抑制作用[10-15]。黄芪、党参、甘草均对金黄色葡萄球菌、枯草芽孢杆菌有抑制作用[16-17]。处方中的大量抑菌成分抑制了供试液中菌落的生长,以致测得回收率低于0.50。
采用薄膜过滤法时,枯草芽孢杆菌和金黄色葡萄球菌的回收率分别为0.87、0.97,处于0.50~2.00范围内,符合标准要求,说明处方中的大量抑菌成分已随冲洗液冲洗滤过去除。在微生物检查过程中确保被检样品的抑菌活性被消除,才能真实的反应检验结果。因此本试验最终选择薄膜过滤法进行胃炎灵颗粒剂的需氧菌总数测定是可行的。
黑曲霉在胰酪大豆胨琼脂培养基和沙氏葡萄糖琼脂培养基上培养时,菌落蔓延迅速至黑色厚绒状,难以计数。为避免黑曲霉菌落计数误差,在琼脂培养基培养1 d后开始逐日计数,而非培养结束后才开始计数。
本研究经过试验验证,建立了胃炎灵颗粒剂的微生物限度检查方法,结合胃炎灵颗粒剂的生产工艺,参考2015版《中华人民共和国药典》四部通则1107,进行胃炎灵颗粒剂的微生物限度检查时,采用薄膜过滤法测定胃炎灵颗粒剂的需氧菌总数,要求每1克胃炎灵颗粒剂中需氧菌总数不得超过1 000 CFU;采用常规法测定霉菌和酵母菌总数,要求每1克胃炎灵颗粒剂中霉菌和酵母菌总数不得超过100 CFU;采用常规法检查控制菌,要求每1克胃炎灵颗粒剂中不得检出大肠埃希菌。

