鞘膜内应用鼠神经生长因子及甲泼尼龙治疗大鼠坐骨神经离断伤的实验研究
王春生 毕秋玲 张锁连 胡婠静 李靖年(通讯作者)
(1 滨州医学院附属烟台业达医院,山东 烟台 264006;2 大连医科大学附属第二医院骨科)
周围神经损伤经显微外科修复后的再生问题是影响神经功能恢复的瓶颈,如何提高其治疗效果一直是实验和临床的研究热点。鼠神经生长因子(mouse nerve growth factor mNGF)可促进损伤神经的修复和再生,目前mNGF已通过肌肉注射全身用药的方式用于临床,有研究认为mNGF局部用药的疗效较全身用药更佳[1]。甲泼尼龙可通过抑制脂质过氧化而对神经细胞及其突起发挥保护作用,单独应用mNGF或甲泼尼龙治疗周围神经损伤已有较多治疗有效的研究,神经鞘膜内联合应用mNGF及甲泼尼龙治疗周围神经损伤是一种新的用药方式,本文建立大鼠动物实验模型,研究这种用药方式治疗周围神经离断伤的疗效,近期治疗效果满意,报告如下。
资料与方法
1 一般资料
1.1 主要试剂及仪器:10%氯氨酮、鼠神经生长因子(商品名苏肽生)、手显微外科器械、徕卡M520-F40手术显微镜(德国)、丹迪Keypoint4型肌电图仪(丹麦)、徕卡切片机、OLYMPUS-Cf3光学显微镜。
1.2 动物分组:健康成年清洁级Wistar大鼠30只,雌雄不拘,体质量200-250 g(由济南朋悦实验动物繁育中心提供),随机分成3组:鼠神经生长因子与甲泼尼龙药物组(A组),甲泼尼龙药物组(B组),生理盐水对照组(C组),每组动物10只。纳入标准:无任何传染性疾病,无足部溃疡性疾病,精神良好,行动灵敏。
2 动物模型和手术过程:每组实验动物称重量后,行腹腔注射麻醉(麻醉药物为氯胺酮,剂量为40mg/kg,使用生理盐水稀释成浓度为4mg/m1),约5分钟后达成麻醉。所有实验大鼠取左大腿后侧至臀区剪去毛,大鼠俯卧固定在鼠板上,取大腿后内侧切口,碘伏消毒,切开皮肤,切口长约2.0cm,打开皮肤后可见一条明显的白线,为肌肉间的筋膜,沿此白线将其剪开一个小口,深入血管钳沿白线方向钝性分离,分开白线后可见两块肌肉之间的坐骨神经干,距梨状肌下缘1.0cm处使切口与水平面呈约45°角斜行切断坐骨神经,再行神经显微外科吻合术,在10倍显微镜下按切口形状无旋转用8-0显微缝线行神经外膜吻合术,无张力下缝合4针。A组鞘膜内注射鼠神经生长因子与甲泼尼龙(mNGF10μg/kg与甲泼尼龙10mg生理盐水稀释成0.1ml液体),B组鞘膜内注射甲泼尼龙(甲泼尼龙10mg生理盐水配成0.1ml液体),C组鞘膜内注射0.1ml生理盐水。缝合切口,构成神经离断伤模型。待麻醉苏醒后,动物放回饲养笼正常喂养。动物模型为同一组手术医师进行,具有可比性。
3 观察指标:(1)大体形态。主要观察大鼠存活状态、切口的愈合情况、足底溃疡及愈合情况;取材时观察神经吻合处有无炎症、与周围组织有无粘连及有无神经瘤形成等。(2)神经电生理及组织学指标。神经电生理:各组均在术后12周取实验神经检测神经传导速度、评价神经功能恢复的情况。组织学观察,取手术侧坐骨神经切口远端5.0mm处神经横断面,制成石蜡切片,作HE染色,镜下观察切片中有髓轴突数目和髓鞘厚度的组织学变化。
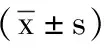
5 结果
5.1 大体形态:所有动物均存活至取材,生命体征平稳,无惊厥、瘫痪、呼吸抑制、腹泻。术后第2天可正常进食,体质量逐渐增加。术区切口无红肿、化脓等感染征象。术后全部切口1期愈合,所有动物术后左下肢跋行明显,随时间延长,mNGF与甲泼尼龙药物组术后平均约8个周左下肢行走功能恢复,而甲泼尼龙组与生理盐水组平均需约9、10个周恢复。术后2周起,各组术侧足趾均出现红肿,未见足底溃疡出现。取材时坐骨神经缝合处各组未见炎症反应,与周围组织未见明显粘连,吻合处稍膨大。两用药组切口感染率并没有因使用甲泼尼龙激素而增加。
5.2 神经电生理指标:术后12周以相同麻醉及手术下暴露左侧坐骨神经,采用Keypoint4型肌电图仪测定坐骨神经传导速度(NCV),测量结果及统计分析见表1。
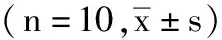
表1 造模后12周各组鼠损伤坐骨神经干的传导速度
坐骨神经干传导速度,A组分别与B、C 组比较,均有P<0.05,差异有显著性,A组神经干传导速度快于B、C2组。
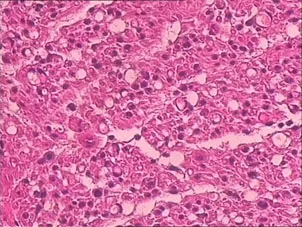
5.3 组织学指标:术后12周在光镜下观察结果:mNGF与甲泼尼龙组(A组),四周观察可见神经由大小不等的神经束组成,外被有神经束膜和外膜,平直排列,可见稀疏的雪旺细胞的胞核;神经纤维的排列和数目有所恢复,排列较整齐,空泡变性不明显,可见分化完好的毛细血管,并见具有完整鞘膜的神经纤维,鞘膜增厚,与正常神经纤维差异不大;甲泼尼龙组(B)可见轻度水肿变性,具有完整鞘膜神经纤维,髓鞘较薄,可见无髓轴突,可见空泡变性;对照组(C)见神经纤维排列紊乱,方向性不好,成不规则型,成纤维细胞和雪旺细胞增殖明显,神经束间有较多的肉芽组织形成,明显水肿及空泡变性,见少量毛细血管形成。见图1(A、B、C)。
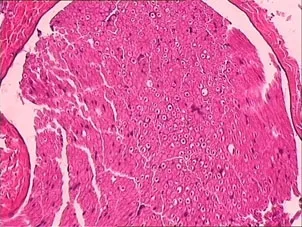
A组
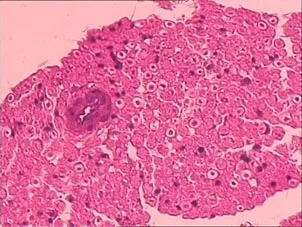
B组
C组
图1各组鼠损伤坐骨神经纤维形态(苏木精-伊红染色,×40)A为mNGF与甲泼尼龙组,B为甲泼尼龙组,C为生理盐水组。
5.4 免疫组织化学与电镜指标:术后12周免疫组化切片,在光学显微镜放大400倍的镜视下计数有髓神经纤维数目,随机抽取各组切片5个视野,取其平均数,做统计学分析;电镜下(见图2),随机抽取各组每个切片5个视野,在相同条件下,计算每个视野内5个有髓神经纤维髓鞘厚度,并取其平均数,做统计学分析(见表2)。
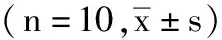
表2 各组鼠损伤坐骨神经有髓神经纤维数目及髓鞘厚度的比较结果
有髓神经纤维计数及髓鞘厚度比较,A组分别与B、C 组比较,均有P<0.05,有显著性差异,A组有髓神经纤维计数及髓鞘厚度均大于B、C2组。
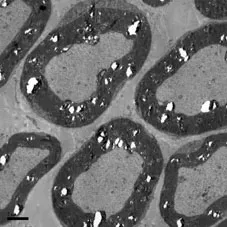
A组
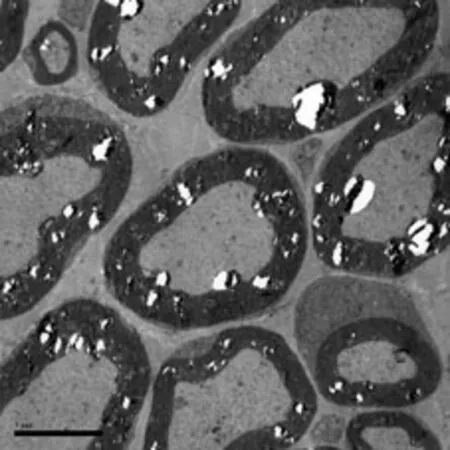
B组

C组
a为mNGF与甲泼尼龙组;b为甲泼尼龙组;c为生理盐水对照组
讨 论
1 用药背景:随着显微外科技术的发展,现已可利用成熟的显微外科技术行神经束膜吻合修复离断的周围神经,但修复后的神经再生仍是一个极其缓慢、持续的过程,在再生轴突生长至效应器前,运动终板、感觉终器退变和肌肉萎缩已经产生。因此,周围神经损伤的修复是目前国内、外基础与临床研究的重要课题。NGF能促进感觉、运动神经纤维的再生及再生神经血管的生成[2],在神经元的再生、生长、分化中起着重要作用。Levi和Cohen在1986年由于在NGF研究上的巨大贡献,共同获得了诺贝尔生理医学奖。NGF的主要作用可概括为:(1)促髓鞘形成;(2)趋使神经轴突定位于合适的靶细胞,形成功能性连接;(3)维持神经元存活;(4)促进神经轴突再生,并决定其生长方向[3]。NGF的临床给药途径目前主要有全身给药和局部给药。NGF生物半衰期短,属于多肽蛋白质,为维持体内有效浓度需要长期反复给药。有学者改进用药方法以增加其作用时间,避免NGF被迅速降解,包括:(1)在损伤神经周围1次性给药;(2)靶肌肉注射;(3)局部通过微渗透泵缓慢释放;(4)通过转基因技术将表达神经营养因子的细胞移植到损伤局部[4]。但有研究表明周围神经损伤早期局部给予NGF治疗可以吸收,24小时后局部给药通过吻合口吸收治疗无临床意义[5]。周围神经损伤后局部会产生相应的免疫反应,血-神经屏障被破坏致局部水肿和炎性细胞聚集,在一定程度上阻碍神经纤维的再生。甲泼尼龙是一种强抗脂过氧化药物,能够减少抗体生成及炎症反应,抑制免疫反应,抑制纤维组织及疤痕增生[6],促进神经元再生及功能恢复。治疗周围神经损伤如采用和脊髓损伤同样的大剂量激素静脉给药的方式,考虑到激素的严重不良反应的风险及经济上的因素,临床上应用尚缺乏可行性。甲泼尼龙的鞘膜内应用既能减轻神经局部的炎症反应,有效发挥免疫抑制作用及保护其效应神经元,抑制纤维组织增生和炎症渗出,又可以避免大量用药的不良反应。综上考虑,我们将mNGF及甲泼尼龙联合应用于神经修复后的鞘膜内治疗周围神经切割伤,建立大鼠坐骨神经离断伤的动物模型,近期治疗效果满意。术后12个周时,综合分析损伤神经传导速度、有髓神经纤维数目及髓鞘厚度的变化,提示鞘膜内应用mNGF及甲泼尼龙的观察组疗效优于两对照组。而术后伤口感染、疼痛、过敏及全身不良反应的发生率,观察组并未增加。
2 疗效分析:形态学标志、电生理和功能恢复情况可作为衡量再生神经成熟的3个指标。神经成熟的主要形态学标志是轴突直径和髓鞘厚度,有较成熟的有髓神经纤维为神经的有效再生。Nakamura等[7]研究发现神经生长因子不仅能促进神经髓鞘化,使再生纤维髓鞘生长完整、增厚;而且能促进神经束面积、神经纤维密度增加。在本动物模型实验中,根据实验组组织学及免疫组织化学结果,mNGF及甲泼尼龙神经鞘膜内应用可促进神经纤维的生长、神经髓鞘的形成。电生理指标中,神经传导速度是神经传导性和兴奋性的定量检测方法[8],在本研究中,观察组损伤神经传导速度快于两对照组,说明观察组用药方法可更有效的促进损伤周围神经的修复与再生。功能恢复的评定根据实验动物跛行恢复所需时间比较,观察组跛行恢复快于两对照组。综合以上理论和动物实验疗效分析,鞘膜内应用mNGF及甲泼尼龙可有效促进损伤周围神经的功能恢复。分析神经鞘膜内注射mNGF及甲泼尼龙后产生疗效的机理有以下几个方面:(1)NGF作为一种逆转运生长因子与其膜受体形成复合物后,外源性的NGF被损伤的轴突逆行运输至相应神经元胞体,经复杂的合成代谢过程,促使再生轴突髓鞘化及延长,以恢复受损神经的功能[9]。(2)近神经胞体端轴突中NGF含量在周围神经损伤后急剧下降,NGF受体含量作为代偿而升高[10]。经补充外源性NGF后,在再生轴突前方NGF浓度梯度诱导下生长锥向前生长,促使再生轴突成熟髓鞘化、促其与靶器官建立联系,促进神经再生及功能恢复[11]。Long等[12]亦发现周围神经损伤后,因内源性NGF缺乏,不能满足神经再生需要,需补充外源性NGF。在本研究观察组中,于神经损伤早期鞘膜内注射外源性NGF,可在一定程度上满足神经再生的需要。(3)在受损神经鞘膜内局部应用甲泼尼龙后,可抑制纤维增生及免疫应答,吻合处疤痕组织的增生减少,可使再生神经轴突易于穿过神经吻合处,早期到达靶器官,也可抑制神经吻合口处神经瘤的形成。(4)在观察组1次性神经鞘膜内注射mNGF后可维持损伤神经局部微环境中缺乏的NGF有效浓度,提高受体与神经生长因子的生物利用率,而液体的扩张作用利于神经的轴浆流动及减少受损神经内粘连。
综上所述,mNGF及甲泼尼龙鞘膜内应用的用药方式治疗大鼠坐骨神经离断伤的近期疗效满意,安全性好,能有效的促进离断周围神经的修复与再生,为该用药方式应用于临床提供动物实验支持,可作为临床周围神经离断伤显微外科吻合术中鞘膜内用药方式。由于本组的样本量较小,且鞘膜内mNGF及甲泼尼龙的用药剂量选择尚需要进行大样本、多中心、长期的研究及随访,进一步观察疗效和安全性、控制药物副作用。

