川楝子提取物中川楝素在大鼠体内的药代动力学研究
于娇妍 王庆伟 石 磊 赵 军 张瑞涛 张 旸 徐 媛
空军军医大学第二附属医院药剂科,陕西西安 710038
川楝子是楝科Meliaceae 植物川楝Melia toosen-dan 的干燥成熟果实(又名金铃子等)[1-3],一般用作理气、驱虫药,以四川产为道地药材,因此叫做川楝子[4-6]。研究表明,川楝子有镇痛、抗炎、抗菌、抗病毒、抑制呼吸中枢等作用,川楝子中四环三萜类化合物川楝素为其主要成分,是迄今为止发现的唯一抗肉毒毒素的天然化合物,能够抑制多种肿瘤细胞生长,或诱导其调亡[7-13]。早期的研究主要集中于川楝素及川楝子不同提取部位的研究。目前对川楝子研究显示川楝素可能是其主要的药效和毒性成分[12,14-17]。
中药药代动学是近年发展非常迅速的学科,它在借鉴化学药物药动学方法和原理(如血药浓度法)的基础上,根据中药“整体观、系统观”的特点发展了生物效应药动学方法以间接推算药动学参数[17-20],因此本研究通过对川楝子中川楝素血药浓度的测定来研究川楝子在大鼠体内的药代动力学特点,进一步阐明川楝子的药理作用。
1 对象与方法
1.1 实验仪器
高效液相色谱(岛津LC-30)和质谱仪(API 4000,AB);TGL-20MV 离心机(湖南郝西公司);电子分析天平(CP225D,Sartorius,十万分之一);UMV-1 多管涡旋混合器(优晟联合科技有限公司);超纯水机(Milli-QAdvantageA10,Milipore)。
1.2 实验试剂
川楝子中药材(西安饮片厂);川楝子醇提物(3.57 g 生药/mL);川楝素对照品(上海源叶生物,批号:Z11N7B24613,纯度>98%);对乙酰氨基酚对照品(中国药品生物制品检定所,批号:100018-200408);甲醇、乙腈为色谱纯;其余试剂均为分析纯。
1.3 实验动物
清洁级健康雄性SD 大鼠,8~12 周,体重为250 g,购买于第四军医大学实验动物中心[合格证号:SCXK(军)2007-007],通过动物伦理学审核,饲养条件:室温(25±2)℃,相对湿度为(50±10)%,每天交替12 h 光照,自由饮水。
1.4 溶液的配置
1.4.1 川楝素储备液及工作液的制备 精密称取川楝素对照品3.06 mg,置于10 mL 棕色容量瓶中,加甲醇溶解定容至刻度,即得306 μg/mL 的储备液;取川楝素储备液适量,甲醇稀释成浓度为10.2、102.0、204.0、408.0、816.0、1224.0、1632.0、3060.0 ng/mL 系列工作液用于标准曲线样品的制备,另取适量储备液制备成浓度为30.6、1224.0、2040.0 ng/mL 的低、中、高质量浓度的质控样品。
1.4.2 内标储备液及工作液的制备 精密称取对乙酰氨基酚对照品4.13 mg,置于10 mL 棕色容量瓶中,加甲醇溶解定容至刻度,即得413 μg/mL 的对乙酰氨基酚储备液。取内标储备液适量,加甲醇稀释成浓度为2070 ng/mL 内标工作液。
1.5 检测条件
色谱条件:ZORBAX Eclipse Plus C18色谱柱(4.6 mm×100 mm,3.5 μm),柱温25℃,流动相:乙腈-0.01%甲酸溶液(梯度洗脱,0~4 min:乙腈5%~55%;4~6.5 min:乙腈55%;6.5~9 min:乙腈55%~5%),流速:0.6 mL/min,进样体积:5 μL。质谱条件:扫描方式为多反应检测扫描(MRM);离子化方式为电喷雾离子源(ESI);喷雾电压:3500 V;毛细管温度:350℃;负离子模式:川楝素:m/z573.3→m/z 531.3,碰撞能(CE)为-25 eV;去簇电压(DP)为-116 eV,对乙酰氨基酚(内标):m/z 150.1→m/z 107.0,CE:-27 eV,DP:-64 eV,见图1。
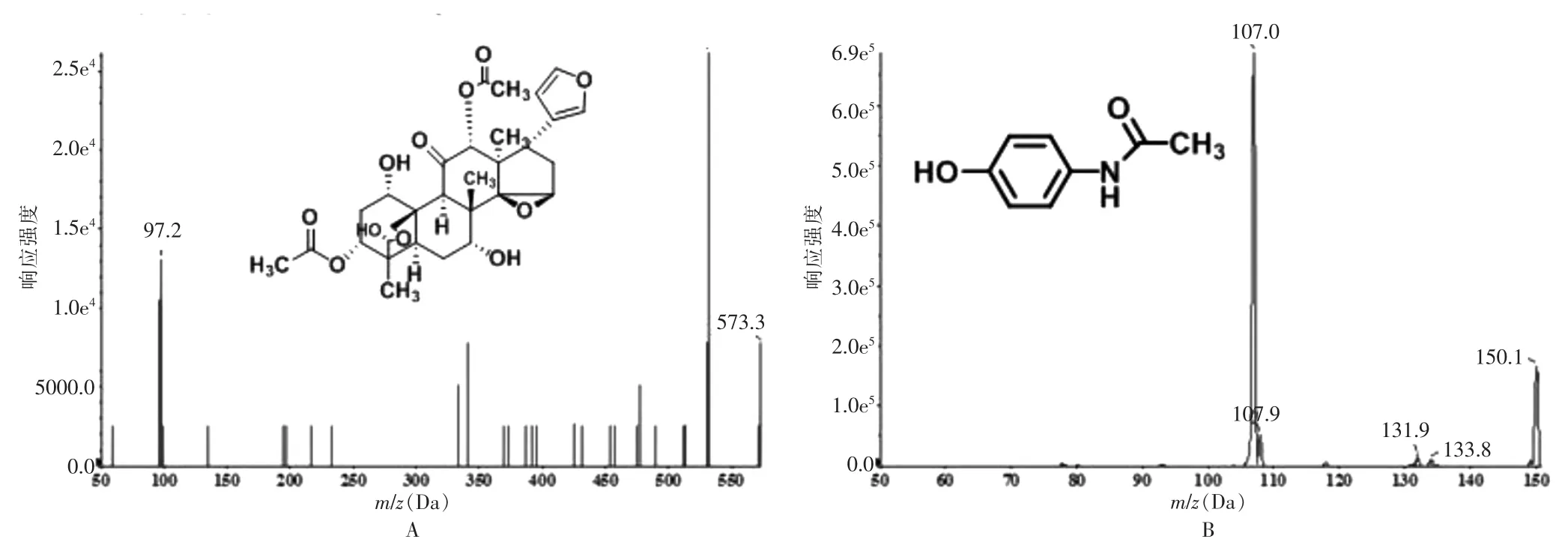
图1 LC-MS/MS 二级质谱图
1.6 实验分组及处理
1.6.1 实验分组和样品采集 取雄性SD 大鼠24 只,按体重随机分为三组,每组8 只。给药前12 h 禁食不禁水,分别按照15、30、60 g 生药/kg(川楝素剂量为330、660、1320 μg/kg)灌胃大鼠川楝子提取物,给药后0、0.083、0.167、0.25、0.5、1、2、4、6、8、12、24 h 眼 眶 静脉丛取血0.25 mL,4℃,12 000 r/min 离心10 min 离心半径5 cm,上清液(血浆样品)-20℃储存备用。
1.6.2 样品处理方法 精密吸取血浆样品100 μL,加入10 μL 内标液,2500 r/min 涡旋5 min 使混匀,再加入400 μL 甲醇,2500 r/min 涡旋5 min,静置3 min,离心(12 000 r/min,4℃,10 min 离心半径)取上清至1.5 mL EP 管中,减压抽干,残渣加100 μL 复溶液(50%乙腈-0.01%甲酸),2500 r/min 涡旋5 min 复溶,离心(12 000 r/min,4℃,10 min 离心半径5 cm)取上清液,进LC-MS 测定。
2 结果
2.1 专属性实验
取空白血浆,加川楝素供试品,加内标和川楝素供试品,给药后血浆加内标样品,按“1.6.2”项下方法,处理样品,进样测定。空白血浆无干扰,川楝素为双峰,依据药典以双峰之和计算。见图2。

图2 LC-MS/MS 色谱图
2.2 线性关系考察
制备川楝素浓度分别为1.02、10.20、20.40、40.80、81.60、122.40、163.20、306.00 ng/mL的血浆样品,加10 μL 内标液,处理后测定。测得的川楝素与内标峰面积的比值Y 对浓度(X)进行加权回归(x-1)得回归方程为Y=0.0185 x+0.0162(r=0.9953),川楝素血药浓度在1.02~306 ng/mL 范围内线性良好,最低定量限为1.02 ng/mL。
2.3 精密度与准确度
制备川楝素浓度为3.06、122.40、204.00 ng/mL 的血浆样品各6 份,处理后连续进样6 次,得日内精密度,连续进样6 天,得日间精密度,精密度和准确度均符合要求。见表1。
表1 大鼠血浆中川楝素的精密度与准确度(,n=6)

表1 大鼠血浆中川楝素的精密度与准确度(,n=6)
2.4 提取回收率和基质效应
制备川楝素浓度为3.06、122.40、204.00 ng/mL 的血浆样品各6 份,进样分析,以加入量和测得量计算提取回收率。配制川楝素低、中、高浓度分别为3.06、122.40、204.00 ng/mL 的甲醇溶液各6 份;川楝素浓度为3.06、122.40、204.00 ng/mL 的血浆样品各6 份,处理后测定。计算基质效应。见表2。
表2 大鼠血浆中川楝素的提取回收率与基质效应(%,,n=6)

表2 大鼠血浆中川楝素的提取回收率与基质效应(%,,n=6)
2.5 稳定性实验
制备川楝素浓度为3.06、122.40、204.00 ng/mL 的血浆样品各6 份,分别在25℃室温放置24 h、4℃冰箱放置7 d、-20℃冰箱反复融冻3 次,处理后进样。结果显示血浆样品稳定性良好。见表3。
2.6 药代动力学实验
按照“1.6”项下方法采集并处理血浆样品,“1.5”项下液质条件进样分析,采用DAS 2.0 软件计算药代动力学参数。与低剂量组、中剂量组比较,高剂量组Cmax和AUC(0~t)升高,CLz/F、Vz/F 降低,差异有统计学意义(P<0.05),见表4。绘制浓度-时间曲线(C-T曲线),见图3。
3 讨论
实验考察了不同方法提取大鼠血浆样本中川楝素,因川楝素在有机溶剂中溶解度较高,因此比较了用乙酸乙酯萃取血浆中川楝素、乙腈和甲醇沉淀血浆蛋白的提取回收率,最后选择提取回收率最高的甲醇沉淀法处理血浆样品,并且经验证该方法稳定可靠。实验建立了LC-MS 法测定大鼠体内川楝素含量的方法,能够将川楝素的色谱峰分离,能反映样品的真实性,并且经验证所建方法简便、准确、灵敏。在计算的过程中,由于川楝素化学结构中存在醛-酮式结构的互变[21-24],因此在色谱图中出现双峰,依据药典以双峰面积之和计算。
表3 不同存储条件下含川楝素的血浆样品稳定性(,n=6)

表3 不同存储条件下含川楝素的血浆样品稳定性(,n=6)
表4 灌胃3 种剂量川楝子提取物药代动力学参数(,n=6)
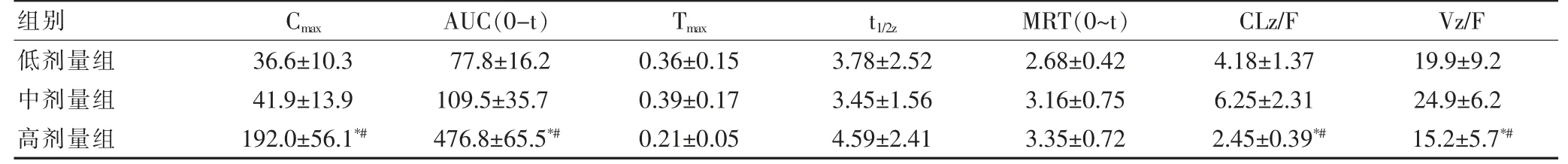
表4 灌胃3 种剂量川楝子提取物药代动力学参数(,n=6)
注:与低剂量组比较,*P<0.05;与中剂量组比较,#P<0.05。Cmax:最大血药浓度;AUC:药时曲线下面积;Tmax:达峰时;t1/2z:消除半衰期;MRT:平均滞留时间;CLz/F:清除;Vz/F:表观分布容积

图3 川楝素在大鼠体内的C-T 曲线(n=8)
川楝子不同给药剂量的药代动力学参数结果显示低、中、高3 种剂量(15、30、60 g 生药/kg)给药后MRT(0~∞)没有明显变化,Cmax,AUC(0~t),以及CLz/F和Vz/F 差异均有统计学意义。随给药剂量的增大,AUC(0~t)与剂量比例不成正比,说明川楝素在大鼠体内为非线性动力学过程。中剂量组的AUC(0~t)是低剂量组的1.4 倍,高剂量组的AUC(0~t)明显高于低、中剂量组,分别是中剂量组的4.4 倍,低剂量组的6.2 倍,说明大鼠给药剂量超过30 g 生药/kg 后,川楝素的生物利用度会大幅度提高,药代动力学过程异常。15、30 g 生药/kg 两组间比较,随给药剂量CLz/F 增大1.4 倍,说明肝肾清除川楝素功能正常,但是60 g生药/kg 给药后CLz/F 清除率显著降低,说明机体清除川楝素的能力降低,提示该剂量时肝肾代谢和排泄功能可能受损,机体内川楝素蓄积,与川楝子造成肝毒性有一定关系。因此,通过其改变川楝素在大鼠体内的药代动力学过程能够改善川楝子所致肝毒性。

