清热解毒分散片辅料处方优选
丁京伟,吴建明,赵 准,朱 婷,张凌俏,叶志学,李鹏飞,沈彩虹
(浙江维康药业股份有限公司,浙江 丽水 323000)
清热解毒片由金银花、玄参、地黄、连翘、栀子、甜地丁、黄芩等12味药材组方,有清热解毒功效,临床用于治疗热毒壅盛所致发热面赤、烦躁口渴、咽喉肿痛,以及流行性感冒、上呼吸道感染见上述证候[1]。为提高药物的生物利用度及便于服用,本研究中尝试将清热解毒片制成分散片[2-4],并优选其辅料处方。现报道如下。
1 仪器与试药
1.1 仪器
GM400E型湿法制粒机、FBD300E型沸腾干燥机(重庆瀚威迪科技有限公司);HGD-3500型固定料斗混合机(武汉恒达昌机械设备有限公司);GZPS-73型全自动高速双出料压片机(北京翰林航宇科技发展有限公司);BS124S型电子分析天平(德国赛多利斯股份有限公司);KQ500DB型超声波清洗器(昆山市超声仪器有限公司)。
1.2 饮片
生石膏(批号为 160206)、玄参(批号为 160118)、地黄(批号为 160111)、连翘(批号为 160127)、栀子(批号为 160122)、甜地丁(批号为 160108)、龙胆(批号为160126)、板 蓝 根 (批 号 为 160130)、麦 冬 (批 号 为160213),均购自亳州市华云中药饮片有限公司;金银花(批号为 20160101)、黄芩(批号为 20160109)、知母(批号为20160113),均购自安徽纪淞堂中药饮片有限公司。
1.3 试剂
绿原酸对照品(中国食品药品检定研究院,批号为110753-201716,含 量 99.3% )二 氧 化 硅 (批 号 为20160128)、低 取 代羟丙 纤 维素(LS-HPC,批号为160221),均购自安徽山河药用辅料股份有限公司;微晶纤维素(湖州展望药业有限公司,批号为160115);乙醇(湖南尔康制药股份有限公司,批号为100320160223)。
2 方法与结果
2.1 样品制备
取生石膏、金银花、玄参、地黄、连翘、栀子、甜地丁、黄芩、龙胆、板蓝根、知母、麦冬等12味药材各适量,黄芩、连翘粉碎成细粉,其余药材加水煎煮3次,第1次温浸 2.0 h 后煎煮 1.5 h,第 2 次煎煮 1.5 h,第 3 次煎煮1.0 h。分别滤过,合并滤液,减压浓缩至相对密度为1.30(60 ℃),加入上述细粉,烘干,打粉,药粉加入二氧化硅、LS-HPC及适量微晶纤维素混匀,用60%乙醇适量制粒,干燥,整粒,压成1 000片,即得。
2.2 条件选择
2.2.1 崩解剂类型[5-6]
分散片成型的关键是选择优质的崩解剂,其对分散片的崩解、分散、溶出效果至关重要。本试验中选择常用的交联羧甲基纤维素钠(cCMC-Na)、羧甲淀粉钠(CMS-Na)、LS-HPC、羧甲基纤维素钠(CMC-Na)作崩解剂,以崩解时限为指标比较崩解效果,结果依次为7,22,8,17 h。可见,cCMC-Na及 LS-HPC 崩解时限较短,且效果接近,但由于cCMC-Na为进口辅料,价格昂贵,从节约生产成本角度考虑,选择国产LS-HPC为崩解剂。
2.2.2 崩解剂加入方法
内加法:取药粉284.37 g、二氧化硅70 g、微晶纤维素5.63 g、崩解剂LS-HPC 140 g,放入湿法制粒机中混匀,喷入60%乙醇制成颗粒,经沸腾干燥机干燥,混合均匀后压制成1 000片。外加法:除LS-HPC在干燥后加入外,其余操作均同内加法。内外加法;除LS-HPC在制粒之前(98 g)和压片时(42 g)分2次加入外,其余操作均同内加法。
以崩解时限为考察指标,优劣顺序为外加法(110 s)<内外加法(95 s)<内加法(138 s),以外加法最优;以外观色泽为考察指标,优劣顺序为内加法(好)>内外加法(较差)>外加法(差),内外加法和外加法制粒后,外加辅料与颗粒不易混匀,且由于辅料与颗粒密度、流动性不同,而导致药片上下表面色泽不一致;内加法所制药片外观色泽较好,崩解时限符合要求,故采用内加法制粒。
2.2.3 填充剂类型[7]
结果见表1。可见,以微晶纤维素与二氧化硅为填充剂时,片剂崩解时限短,硬度较好,故以二者为填充剂。
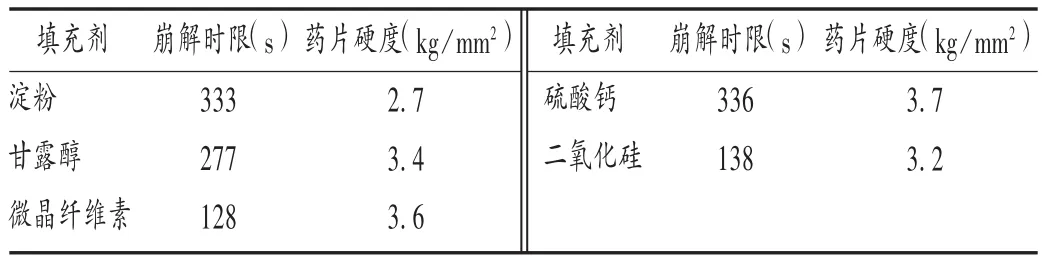
表1 填充剂筛选结果
2.2.4 黏合剂类型
结果见表2。可见,以60%乙醇为黏合剂效果较好。
2.3 处方优化
以崩解时限、可压性、硬度等作考察指标,对样品制备过程中影响较大的因素,如崩解剂LS-HPC、填充剂二氧化硅等的用量进行考察,筛选最佳处方。结果见表3。可见,处方三因其既符合分散片的质量要求,又符合本品工业化大生产的实际要求,最理想。按处方三工艺,制成 3 批样品(批号分别为 B161201,B161202,B161203)。

表2 黏合剂选择结果

表3 清热解毒分散片处方筛选
2.3 验证试验
2.3.1 溶出度测定
色谱条件:色谱柱为Agilent SB-C18柱(250 mm×4.6 mm,5 μm);流动相为乙腈 -0.4%磷酸溶液(10 ∶90,V/V);检测波长为 327 nm;流速为 1.0 mL /min;柱温为35℃;进样量为10 μL;理论板数按绿原酸峰计应大于3 000。色谱图见图1。

图1 高效液相色谱图
溶液制备:称取绿原酸对照品适量,精密称定,加50%甲醇制成每1 mL含80 μg的对照品溶液。取样品10片,研细,称取适量,精密称定,置具塞锥形瓶中,精密加入脱气蒸馏水250 mL,密塞,超声处理30 min(水温37℃,伴有振摇),取出,放冷,摇匀,滤过,续滤液经微孔滤膜(0.45 μm)滤过,即得供试品溶液。
方法学考察:按标准进行精密度、重复性、稳定性试验,结果均符合要求。
溶出度测定:取3批供试品溶液各10 μL,注入液相色谱仪,测定峰面积(A)并计算含量。取3批样品各6片,按溶出度测定法(2015年版《中国药典(二部)》附录ⅩC第三法),以脱气蒸馏水250 mL为溶剂,50 r/min离心 10 min,取样 2 mL,立即滤过,滤液经 0.45 μm 微孔滤膜滤过,取10μL注入液相色谱仪,测定峰面积(A1),计算样品含量。按公式A1/A×100%计算溶出度。结果显示溶出效果良好(溶出度不低于70%)。详见表4。

表4 样品溶出度测定结果(%,n=6)
2.3.2 性状
本品性状为棕黄色分散片,气微,味苦。
2.3.3 分散均匀性
按崩解时限检查法[2015年版《中国药典(四部)》通则0921]检查,不锈钢丝网的筛孔内径为710 μm,水温为15~25℃。取3批样品,每批各2片,均在3 min内全部崩解(崩解时限分别为 139 s,141 s,118 s),并通过筛网。结果显示,样品分散均匀性良好。
3 讨论
分散片为新型固体口服制剂,遇水能迅速崩解,形成均匀的黏性混悬液。它兼具片剂和液体制剂的独特优势,具有服用方便,崩解迅速,吸收快,生物利用度高[8],特别适用于吞服困难的患者。其遇水后须在尽可能短的时间(<3 min)内崩解为很小的颗粒,并形成均匀的混悬液,因此需加入较大量的优质崩解剂和助悬剂。崩解剂不溶于水且吸湿性强,通过毛细管作用或膨胀作用使水分子易渗入片剂,吸水后粉粒膨胀而不溶解,不形成胶体溶液,不阻碍水分子的继续渗入,故不会影响片剂的进一步崩解。本试验结果表明,LS-HPC为适合的崩解剂。但应用多种优质崩解剂效果均欠佳,这是因为浸膏粉制粒黏性较强,而常用于分散片的崩解剂多有吸湿性,故使浸膏粉吸湿性增强,黏性增加,而使片剂难以崩解,因此应选择一定辅料作填充剂,以降低浸膏粉的吸湿性,便于制粒及降低崩解剂的用量。本试验中经筛选,最终选择微晶纤维素与二氧化硅为填充剂。
压片法通常分为粉末直接压片和湿法制粒压片。前法虽崩解时限较后法短,但粉末流动性极差,吸潮性强,加入润滑剂则会,大幅延长崩解时限。后法可压性强,能有效提高药片的硬度及耐磨性。
综上所述,优选的处方辅料类型及比例适宜,崩解时限符合要求,可为清热解毒分散片的工业化生产提供参考。

