低取代羟丙纤维素吸附茶黄素的热动力学研究
涂云飞
(1.浙江省茶资源跨界应用技术重点实验室,浙江 杭州 310016;2.中华全国供销合作总社杭州茶叶研究院,浙江 杭州 310016)
0 引言
茶黄素(Theaflavins,TFs)是红茶中一类具有苯骈罩酚酮结构多酚,主要包括:茶黄素(Theaflavin,TF)、茶黄素-3-单没食子酸酯(Theaflavin-3-Gallate,TF-3-G/TF3)、茶黄素-3'-单没食子酸酯(Theaflavin-3'-Gallate,TF-3'-G/TF3')、茶黄素-3,3'-双没食子酸酯(Theaflavin-3,3'-Gallate,TF-3,3'-G/TFD),现已成为红茶品质高低的象征,精制富集纯化茶黄素成为红茶深加工领域研究的热点[1-6]。大孔吸附树脂现已被广泛应用于黄酮、皂苷、生物碱类等天然化合物的纯化中,富集茶黄素亦不例外[7-8]。然而,大孔吸附树脂一般会残留危害人体的合成前体,在长期使用过程中树脂降解产物使得原本绿色安全的茶黄素具有安全隐患。绿色制备的需求与呼声在行业中越来越强。
低取代羟丙纤维素为纤维素基质上接入羟丙基,与Sephadex LH-20 有相仿的结构组成,并且具有分离精制茶黄素的属性,其材质安全、质优、价廉。本实验考察低取代羟丙纤维素对茶黄素的吸附行为及其热力学性质,以期得到相关规律和热力学参数,同时从热力学的角度研究其吸附法纯化茶黄素的可行性,为茶黄素的分离纯化提供理论参考依据。
1 材料与方法
1.1 主要仪器与试剂
Waters 高效液相色谱仪(配备1525 泵,2487紫外可见检测器,717-plus 自动进样器,Breeze 控制软件);色谱柱(Phenomenex Luna,Phenyl-Hexyl,5 μm,250 mm×4.6 mm 与Waters Symmetry,5 μm,150 mm×4.6 mm);JB/T5374 型电子分析天平(梅特勒-托利多仪器(上海)有限公司);HH-6 型水浴锅(常州朗越仪器制造有限公司);TDZ4A-WS 离心机(湖南赛特湘仪离心机仪器有限公司);低取代羟丙纤维素(安徽山河药用辅料股份有限公司);乙腈(分析纯,纯度≥99%,国药集团化学试剂有限公司);冰醋酸(分析纯,纯度≥99%,国药集团化学试剂有限公司);乙醇(分析纯,纯度≥99%,杭州化学试剂有限公司);甲醇(分析纯,纯度≥99%,国药集团化学试剂有限公司);市售茶黄素粗品;纯净水(实验室自制)。
1.2 茶黄素粗品溶液的制备
将市售茶黄素粗品配制成0.5%浓度。配制时,以含有0.05%醋酸的5%乙醇水溶液溶解,并充分搅拌均匀后,静置离心,取上层清液备用。
1.3 低取代羟丙纤维素不同规格的筛选
低取代羟丙纤维素预处理时,将不同规格的低取代羟丙纤维素与0.5%的茶黄素溶液按1∶50的固液比进行24 h 的振荡吸附,离心取上层清液进行分析。
1.4 吸附等温线的测定
取预处理好的低取代羟丙纤维素0.1 g(5 份),于50 mL 具塞三角瓶中,分别加入10 mL不同浓度(0.5~3 mg·mL-1)的茶黄素粗品溶液,恒温水浴振荡24 h 达到吸附平衡,离心,测定上层清液平衡液中茶黄素含量,根据(1)式计算不同浓度下低取代羟丙纤维素对茶黄素的吸附量。以吸附平衡液中茶黄素的平衡浓度Ce为横坐标,低取代羟丙纤维素上茶黄素的平衡吸附量Qe为纵坐标,绘制等温吸附曲线。同时再于4 ℃、25 ℃进行实验,从而得到不同温度下低取代羟丙纤维素对茶黄素的吸附等温线。

式中:V 为吸附液的体积(mL);m 为低取代羟丙纤维素的干态质量(g);Qe为平衡吸附量(mg·g-1);C0为吸附前溶液中茶黄素的质量浓度(mg·mL-1);Ce为吸附平衡时溶液中茶黄素的质量浓度(mg·mL-1)。
1.5 茶黄素的检测
采用高效液相色谱法:柱温为35 ℃,检测波长为278 nm,进样量10 μL。
2 结果与讨论
2.1 检测茶黄素液相色谱分离条件的建立
根据高效液相色谱的建立条件规则,首先采用儿茶素测定国际标准(ISO 14502-2)推荐色谱柱(Phenomenex Luna,Phenyl-Hexyl,5 μm,250 mm×4.6 mm)。并控制有机相(含2%醋酸的80%乙腈)不变,水相由纯水过渡至含0.2%醋酸的7.5%乙腈水溶液,进行梯度条件洗脱。

表1 高效液相色谱梯度洗脱程序(苯基己基柱)
以上3 个高效液相色谱运行梯度洗脱程序(表1)得到的色谱图见图1。
从图1 可以看出,将国际标准中的水相改成纯水时,茶黄素组分获得较佳的分离度需要增加较多的洗脱时间;随着在纯水中添加有机溶剂乙腈,分离时间缩短,但分离度并未得到改善。当进一步在洗脱程序2 的水相中添加0.2%的醋酸,并调整洗脱时间的情况下,茶黄素各组分在高效液相色谱柱上的分离度有了明显的改善,分离度增大,同时,TF-3-G 附近分离出了一个杂质小峰。
为了缩短分析时间,实验进一步考察了采用Waters Symmetry 色谱柱的茶黄素分离情况。并控制水相为含5%乙酸乙酯及2%醋酸的水,有机相为纯乙腈,梯度洗脱程序见表2。

图1 茶黄素在苯基己基柱上不同梯度洗脱程序对应的高效液相色谱图

表2 高效液相色谱梯度洗脱程序(Waters Symmetry 柱)
以上2 个高效液相色谱的洗脱运行得到的色谱图见图2:

图2 茶黄素在Waters Symmetry 柱上不同梯度洗脱程序对应的高效液相色谱图
在由急速降低溶剂极性分离不是特别好的情形下,通过调整洗脱体系,增大洗脱过程中洗脱溶剂极性,虽然延长了洗脱时间,但茶黄素组分分离度得到明显改善,相比于Phenomenex Luna色谱柱,Waters Symmetry 色谱柱获得茶黄素的分离时间缩短了将近一半,且流动相配制更为方便。综合考虑色谱柱柱效及分析时间的长短,后续实验以Waters Symmetry 色谱柱对应的洗脱参数对茶黄素进行分析检测。
2.2 低取代羟丙纤维素吸附茶黄素规格的选择
如表3 所示,选取的3 种规格的低取代羟丙纤维素对茶黄素的吸附效果均较好,其中以规格1 的吸附能力最强,其次为规格2 与3。各规格中的低取代羟丙纤维素对酯型茶黄素的吸附率大于简单茶黄素,且TF-3'-G 与TF-3,3'-G 在低取代羟丙纤维素中的吸附率接近。
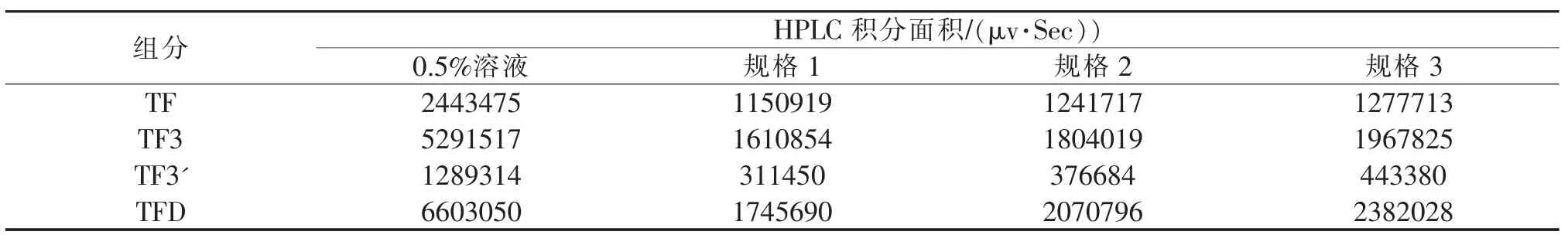
表3 不同规格低取代羟丙纤维素吸附茶黄素溶液平衡浓度
2.3 低取代羟丙纤维素对茶黄素的吸附等温线
通常在固液吸附体系中,目标产物随着温度及接触时间的延长,在吸附剂上的吸附量呈增长趋势,吸附等温线对于描述物质的吸附行为起到很重要的作用。当吸附达到平衡状态时,吸附等温线能够被用来预测目标物在固液中的分布状态。本实验以Langmuir 和Freundlich 方程来考察低取代羟丙纤维素对茶黄素的静态吸附行为。
在图3 中,随浓度升高,茶黄素类成分均出现吸附饱和:TF,TF3,TF3',TFD 分别在439 mg·L-1、824 mg·L-1、165 mg·L-1及1149 mg·L-1浓度时达到饱和。低取代羟丙纤维素吸附茶黄素的平衡吸附量Qe(mg/g)在不同温度条件下,随浓度的增加而增加,且低温更有利于其吸附,即与吸附在放热过程相稳合。
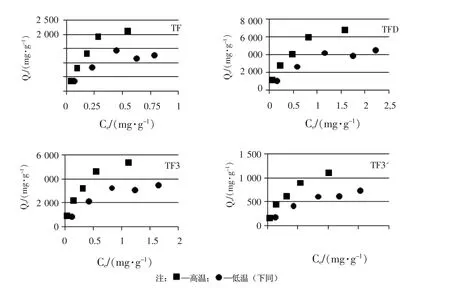
图3 茶黄素类在低取代羟丙纤维素上的吸附等温线
2.3.1 Langmuir 等温吸附模型
Langmuir 吸附等温线通常用来描述吸附剂液态吸附行为。该方程能够被用来预测吸附剂对目标产物的最大吸附量。Langmuir 吸附等温线基于吸附发生在吸附剂表面单分子层假设,忽略Absorbate 分子之间的相互吸附,公式表达如下:
1/Qe=1/Qm×[1+1/(KL×Ce)]
式中:Qe为每质量单位吸附剂平衡吸附量(mg·g-1),Ce为吸附平衡时溶液中茶黄素的质量浓度(mg·mL-1),Qm为每质量单位吸附剂理论最大平衡吸附量(mg·g-1),KL(L·g-1)为吸附等温线常数。
如图4 所示,其为茶黄素在低取代羟丙纤维素吸附时,1/Qe对1/Ce所作的不同温度下的线性图,其回归方程见表4。图4 表说明方程中斜率随温度增加而增加。各回归方程的R2>0.98,说明Langmuir 等温吸附模型适合描述不同温度下,四种茶黄素单体在低取代羟丙纤维素中吸附平衡过程。

图4 茶黄素类各单体Langmuir 吸附等温线
另外,Langmuir 方程拟合较好,说明吸附材料对酯型儿茶素及茶黄素的吸附是以单分子吸附为主,吸附是一动态过程。并且表4 中,除TF 外,Qm与KL值随温度增加而降低,而KL与吸附热量关联,即KL的值降高,越有利于目标产物茶黄素的吸附,故茶黄素的吸附主要为吸附放热过程。

表4 茶黄素各成分对应Langmuir 模型
2.3.2 Freundlich 等温吸附模型
通常情况下,Freundlich 拟合方程基于吸附发生在固体的异质表面和多层吸附行为。其表达式为:Qe=KF×Ce1/n或lnQe=lnKF+1/nlnCe
式中,KF与1/n 是该Freundlich 方程的常数。
如图5 所示,其为茶黄素在低取代羟丙纤维素中吸附时,lnQe对lnCe所作的不同温度下的线性图,其回归方程及各参数与回归系数见表5。

图5 Freundlich 等温吸附拟合模型
表5 中拟合的方程适合解释茶黄素在低取代羟丙纤维素上的吸附行为。Freundlich 方程中的常数1/n 涉及表面异质不均匀性。0<1/n<1,表明吸附是适合的;1/n=1 表明吸附是同种类的;1/n>1 表明拟合的模型不适合吸附行为的表述。KF与吸附能力有关,比较Langmuir 等温吸附模型与Freundlich 等温吸附模型,前者的拟合回归系数高于后者,即表明茶黄素类更适合Langmuir 同类单分子吸附模型。

表5 茶黄素各成分对应Freundlich 模型
2.3.3 吸附热力学参数考察
基于热动力学原理,能量属于守恒状态。并且在独立系统中,熵是目标物质是否能够被材料吸附的重要驱动力。实际考察应用中,能量与熵通常被用来考察过程是否会自发发生。在吸附过程中,热力学参数标准焓(ΔHθ)、标准熵(ΔSθ)及标准吉布斯自由能(ΔGθ)通常会被重点考察,热力学参数ΔHθ、ΔSθ及ΔGθ,可以作如下计算:
ΔGθ=-RT lnKL
lnKL=-ΔGθ/RT=ΔSθ/R-ΔHθ/RT
其中,R 是常数(8.314 J·(mol·K)-1)
方程中的ΔHθ、ΔSθ能够通过lnKL与1/T 所作回归方程的斜率与截距所得。茶黄素在低取代羟丙纤维素上的吸附热动力学如表6 所示。当吉布斯自由能为负值时,一般会表示吸附自由发生。标准焓为负值时,通常会表示吸附为放热反应,这与实验观察的一致(表6)。通常ΔHθ的值在2.1~20.9 kJ·mol-1与80~200 kJ·mol-1时,分别代表物理与化学吸附,表6 表明为茶黄素在低取代羟丙纤维素上的吸附为物理吸附。同时,标准熵为负值时,表示吸附质在固液界面很少自由运动,吸附较牢靠。标准熵值的改变与吸附剂吸附水的位点被取代相关。负的标准熵值通常揭示吸附剂表面吸附目标成分不强于水分子,故表6 中除TF 外,其它三种茶黄素单体在低取代羟丙上的吸附主要由焓驱动。另外,ΔHθ>0,表明低取低羟丙纤维素对茶黄素TF 的吸附亦为放热反应。

表6 茶黄素单体在低取代羟丙纤维素上的吸附热力学参数
3 结论
低取代羟丙纤维素能够作为价廉且有效的吸附剂,通过物理力的作用,从溶液中吸附茶黄素类成分。Langmuir 等温吸附模型能够较好拟合描述茶黄素在低取代羟丙纤维素上的吸附行为。通过静态吸附实验发现,三种低取代羟丙纤维素对茶黄素吸附是以单分子吸附为主,其对各成分均有较好的吸附,特别对双酯型茶黄素的吸附效果较好。

