基于化学计量学优选不同制法山楂叶提取物
赵胜男,姚建伶,韩 笑,潘海峰∗
(1.河北省中药研究与开发重点实验室/承德医学院中药研究所,河北 承德 067000;2.北京四环制药有限公司,北京 100025;3.承德护理职业学院,河北 承德 067000)
化学计量学是一门通过数学或统计学方法将对化学体系的测量值与体系的状态之间建立联系的学科,它的特点是可以最有效地获取体系有用的特征数据,并通过解析测量数据最大限度地从中提取有关物质的定性、定量、形态、结构等信息[1]。化学计量学不仅在数学领域应用广泛,在中药鉴别、质量控制等研究中也越来越被接受和使用[2-9]。本研究运用化学计量学对不同采集地山楂叶药材中采用面积归一化法所得15 种成分的峰面积比例进行统计;应用聚类分析与主成分分析得到30 批药材;利用判别分析建立质量数学表达式。
山楂叶具有活血化瘀、化浊降脂等功效,主要含有黄酮和有机酸类。其临床制剂品种很多,如山玫胶囊[10]、心安胶囊[11]、益心酮片[11]等,主要用于心脑血管方面疾病的治疗;近几年,对活血化瘀药物与血瘀证的相关研究已经成为现代学者主要领域之一。大量研究表明,血瘀证的发生与粘滞性异常和血液流变等生理病理改变有关,而其中的宏观流变学主要研究血液在不同切变率下的黏度表现[12]。本研究在选用符合上述质量数学表达式要求的药材基础上,同时选取的提取工艺以《中国药典》和成方制剂为准则,以最大限度得到黄酮类成分的提取思路为模型作用于血瘀模型大鼠,以全血黏度值为指标,在药材质量可追溯的基础上结合大鼠全血黏度值优选最佳山楂叶提取物制法,方法科学、更具有实用意义。
1 仪器与材料
1.1 仪器 安捷伦1200 型高效液相色谱仪(美国安捷伦公司);AG-245 型分析天平(瑞士梅特勒-托利多公司);LBY-N6K 型全自动血流变仪(北京市普利生仪器有限公司);KQ700 型超声波清洗器(昆山超声仪器有限公司)。
1.2 动物 Wistar 雄性SPF 级大鼠,体质量200~220 g,购于北京市维通利华实验动物技术有限公司,动物生产许可证号SCXK(京)2012-0001。
1.3 试剂 金丝桃苷(批号111521-200303),购于中国食品药品检定研究院;牡荆素鼠李糖苷(批号151024)、牡荆素葡萄糖苷(批号151103),购于上海融禾有限公司,上述对照品含有量≥98%。乌拉坦(20150401),购于天津光复精细化工研究所;盐酸肾上腺素(批号1505301),购于天津市金耀药业有限公司。乙腈、甲醇为色谱纯,购于美国Fisher 公司;水为娃哈哈纯净水;其他试剂为分析纯。
1.4 试药 山楂叶为蔷薇科植物山楂Crataegus pinnatifidaBge.的干燥叶,由承德民族师范学院董建新教授鉴定为正品,具体见表1。山楂叶制法A[10](模拟山楂叶成药山玫胶囊,山楂叶以50%乙醇为提取液)、山楂叶制法B(山楂叶药材加5 倍量50%乙醇,加热回流提取2 次,合并提取液用3 倍量水饱和正丁醇溶液提取3 次,合并的正丁醇提取液浓缩至干,即得)、山楂叶制法C[11](模拟山楂叶成药益心酮片,以山楂叶提取物D 为原料制成制剂)、山楂叶制法D(50%乙醇提取液,通过收集大孔吸附树脂柱不同体积分数乙醇洗脱液,回收乙醇得清膏)。
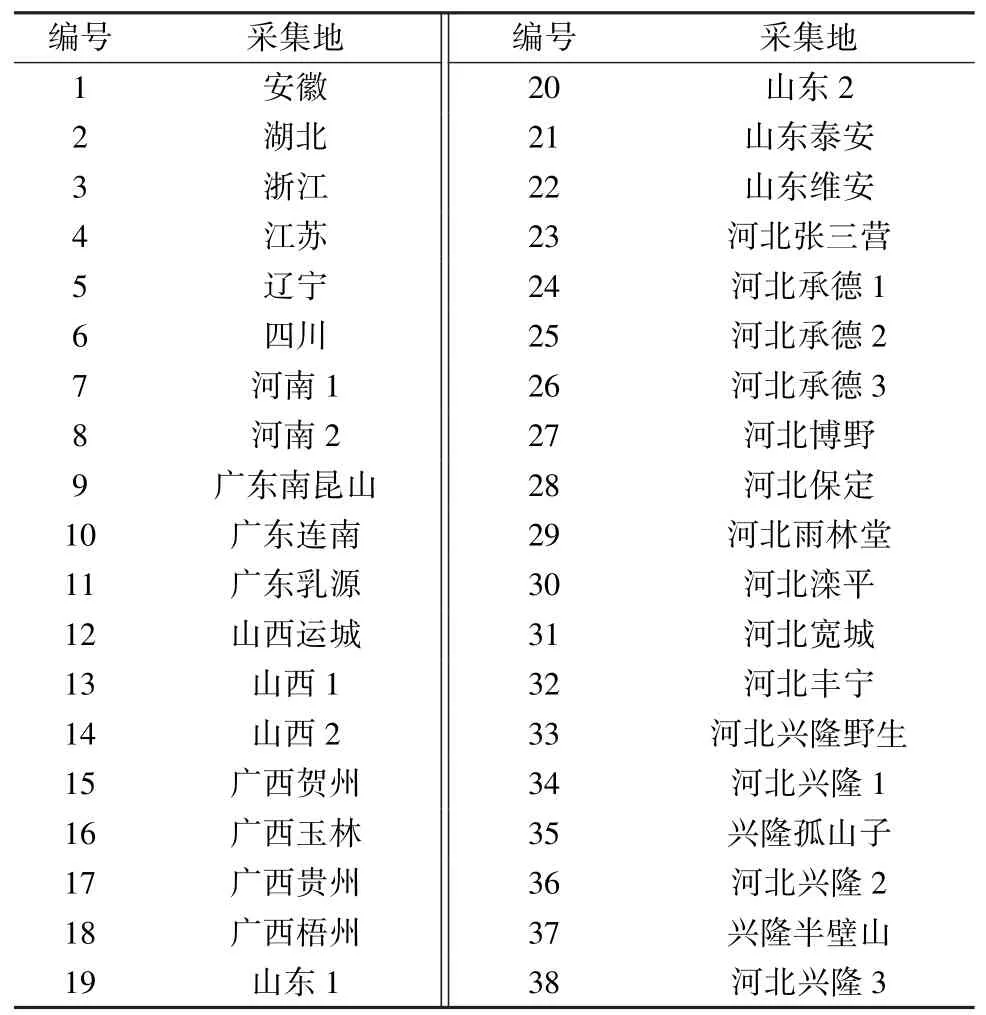
表1 样品信息
2 方法与结果
2.1 HPLC 法建立
2.1.1 色谱条件[13]Aglient Zorbax SB-C18柱(250 mm×4.6 mm,5 μm);流动相0.1%甲酸水(A)-乙腈(B)-四氢呋喃(C);梯度洗脱(0~5 min,10%~12% B;5~15 min,12%B;15~20 min,12%B,前20 minC 占0。20~23 min,12%~14% B;23~35 min,14% B;35~40 min,14%~20% B;40~50 min,20%~30% B;50~60 min,30%~60%B;60~65 min,60%~80%B,20 min 以后C 占8%);检测波长320 nm;体积流量1.0 mL/min;柱温30 ℃;进样量10 μL。
2.1.2 供试品溶液制备 精密称取山楂叶D(2015 年版《中国药典》方法)约0.05 g,置50 mL 具塞锥形瓶中,精密移取60%甲醇25 mL,精密称定质量,超声处理30 min,待冷却后补足减失质量,上清液以0.45 μm 微孔有机滤膜过滤,即得。
2.1.3 对照品溶液制备 精密称取金丝桃苷15.5 mg、牡荆素葡萄糖苷22.0 mg、牡荆素鼠李糖苷20.0 mg,置50 mL棕色量瓶中,甲醇溶剂定容,即得(质量浓度分别为0.31、0.44、0.40 mg/mL),密封备用。
2.1.4 样品测定方法 按“2.1.2”项下方法制备供试品溶液,在“2.1.1”项条件下进样,色谱图见图1。
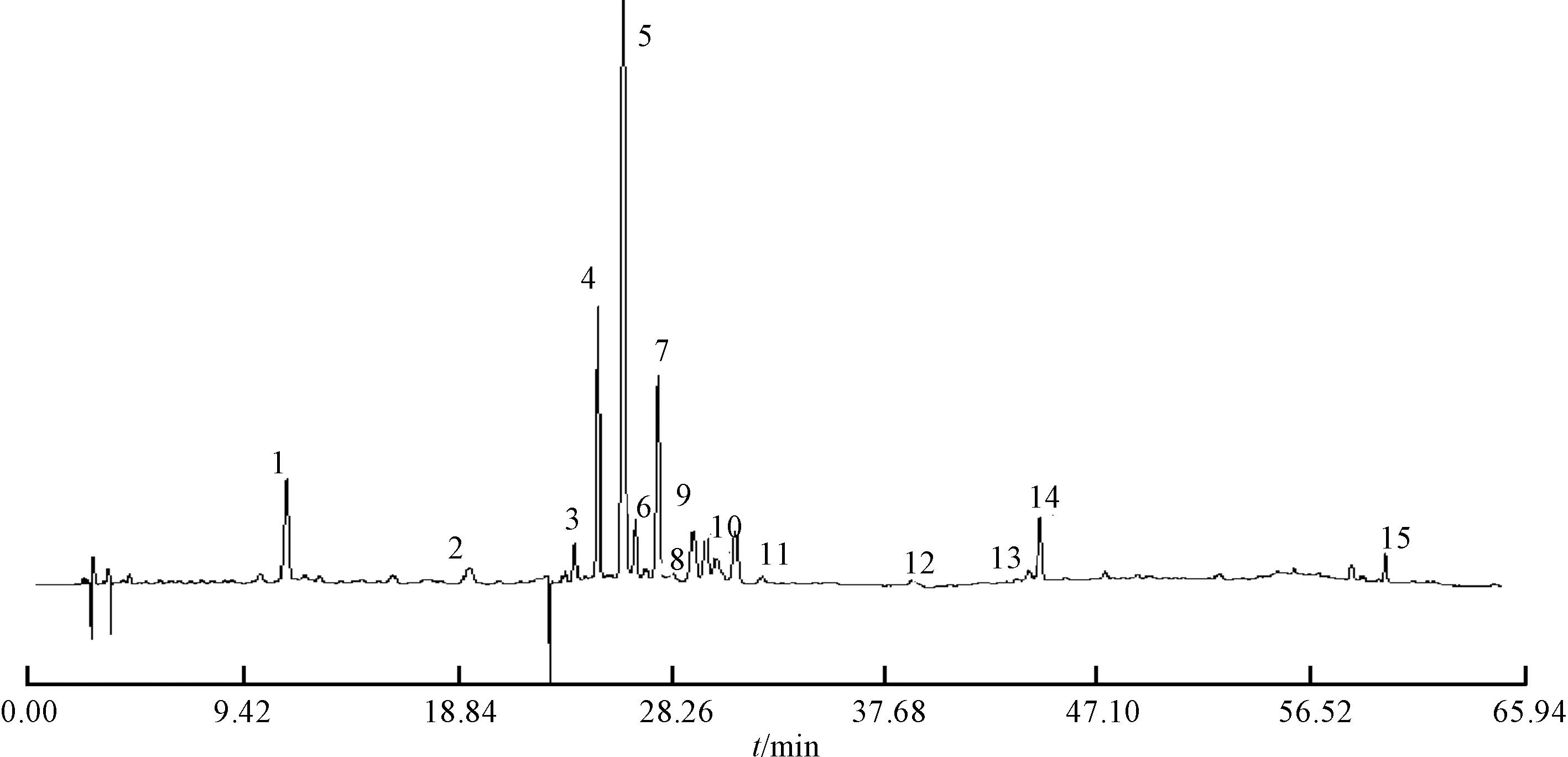
图1 各成分HPLC 色谱图
2.2 方法学考察
2.2.1 精密度试验 取“2.1.3”项下混合对照品溶液适量,在“2.1.1”项条件下连续进样测定6 次,测得金丝桃苷、牡荆素葡萄糖苷、牡荆素鼠李糖苷峰面积RSD 分别为1.88%、1.06%、0.95%,表明仪器精密度良好。
2.2.2 稳定性试验 取“2.1.2”项下供试品溶液(24号)适量,在“2.1.1”项条件下于0、2、4、8、12、24 h测定,测得金丝桃苷、牡荆素葡萄糖苷、牡荆素鼠李糖苷峰面积RSD 分别为1.45%、1.04%、0.78%,表明供试品溶液在24 h 内稳定性良好。
2.2.3 重复性试验 取同一批样品(24 号)适量,按“2.1.2”项 下 方 法 制 备 供 试 品 溶 液,平 行6 份,在“2.1.1”项条件下进样,测得金丝桃苷、牡荆素葡萄糖苷、牡荆素鼠李糖苷峰面积RSD 分别为1.49%、0.88%、0.52%,表明该方法重复性良好。
2.2.4 加样回收率试验 取同一批样品(24 号)适量,分别加入一定量的金丝桃苷、牡荆素葡萄糖苷、牡荆素鼠李糖苷,按“2.1.2”项下方法制备供试品溶液6 份,在“2.1.1”项条件下进样,测得金丝桃苷、牡荆素葡萄糖苷、牡荆素鼠李糖苷加样回收率分别为99.43%、99.66%、99.80%,RSD 分 别 为2.20%、1.16%、0.51%,结果 与2015 版《中国药典》标准符合。
2.3 主成分分析 采用SPSS19.0 软件中的因子分析,以降维思想为指导,对应用面积归一化法获得的不同采集地山楂叶中15 个成分的峰面积比例含有量进行处理。结果,前5 个成分的特征值均大于1,但总方差的累积贡献率为72.879%,偏小,若提取前8 个成分,累积贡献率可达87.279%>85%,表明前8 个主成分才可反映不同批次山楂叶的质量。再计算山楂叶药材的主成分得分,见图2,可知样品分为2 类,其中1 号样品处于2 类样品区域的交界处,并不能明确归类,为了保证山楂叶质量,剔除该批样品,所以9、11、21 及15~18 为Ⅰ类,其余30 批样品聚为Ⅱ类,而且由于Ⅰ类样品相对Ⅱ类样品数目较少,分散,可当作质量不稳定样品筛除,Ⅱ类样品为优质山楂叶。

图2 主成分得分图
2.4 聚类分析 利用面积归一化法将表1 山楂叶中金丝桃苷等15 种成分(色谱峰见图1)的峰面积比例输入SPSS19.0 软件,采用组内联接法,同时以欧式距离为区间进行聚类分析,结果见图3。当类间距在15~25 时,药材被分为两类。1、9、11、21 及15~18 为Ⅰ类,其余30 批为Ⅱ类。
2.5 判别分析 应用SPSS19.0 软件中分类判别,利用贝叶斯判别函数系数法对Ⅱ类药材建立矩阵,表达式为Y=-16.241+0.335X1+2.302X2+0.313X3+0.317X4+0.209X5+0.446X6+0.522X7+1.572X8+0.578X9+2.664X10+0.790X11-0.313X12-0.498X13+0.156X14-1.615X15,其中X1~X15分别代表图1 中色谱峰1~15 的峰面积比例。把Ⅱ类药材所有峰面积比例的平均值代入上述表达式,得Y值为14.611。当有未知质量样品的Y值范围在90%~110%(13.15~16.08)之间时,此样品质量稳定可靠,可作为供试品进行深入研究。
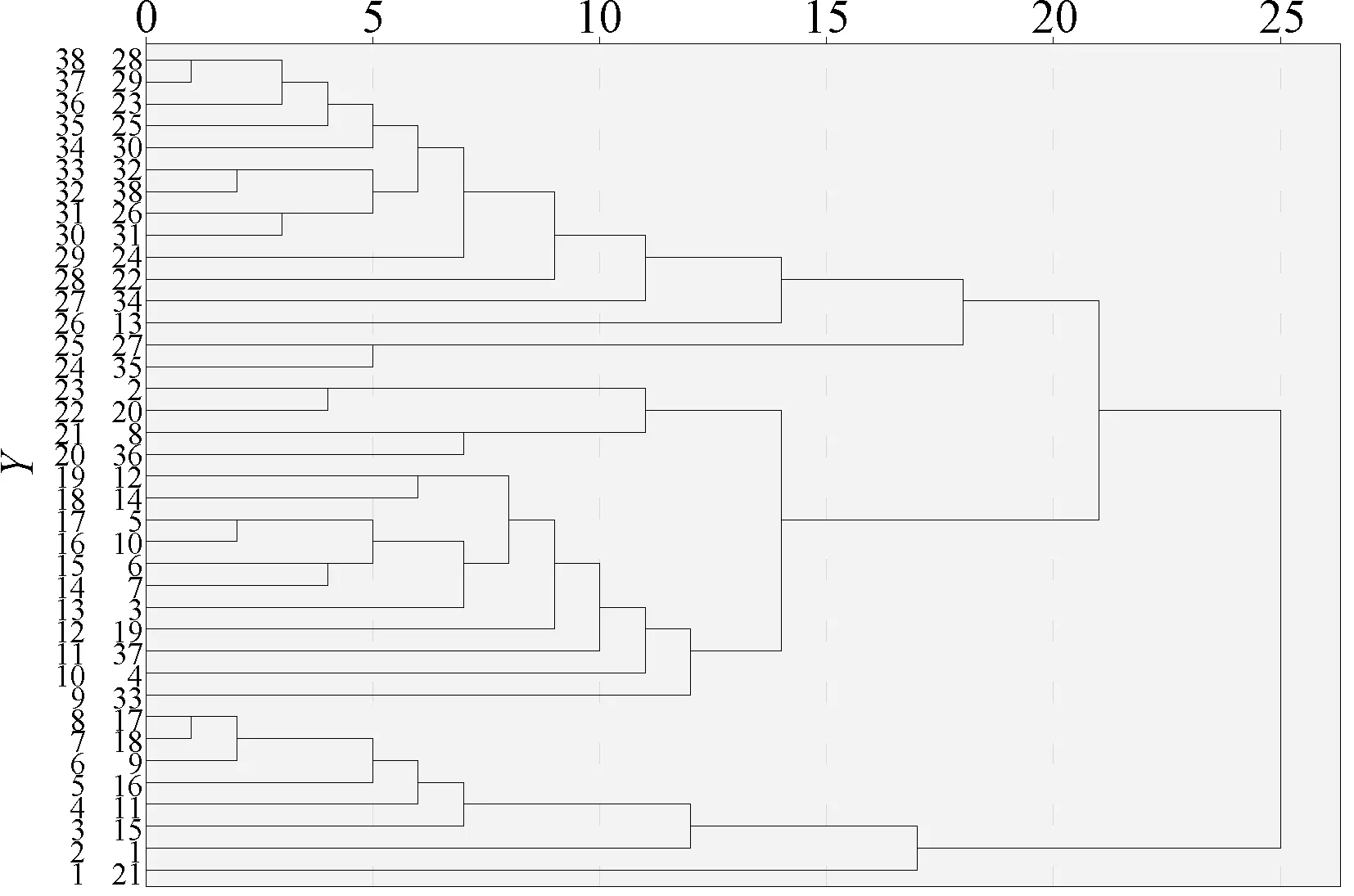
图3 38 批样品聚类树状图
2.6 各制备方法提取物对血瘀模型大鼠全血黏度的测定方法建立
2.6.1 实验动物分组及给药 Wistar 大鼠(雄性)随机分为15 组,每组8 只,分别为制备方法A、B、C、D 的高、中、低剂量组,模型组,空白组。各给药组灌胃给予相应剂量药物,均用同样体积的0.5% 羧甲基纤维素钠溶液溶解,空白组与模型组平行处理,每天给药1 次,连续8 d。
2.6.2 血瘀模型大鼠建立 大鼠第7 天给药后除空白组皮下注射给予生理盐水外,其余组均颈背部皮下注射盐酸肾上腺素,剂量为0.8 mg/kg,2 h 后除空白组外其余各组大鼠均浸入冰水中(4 ℃)5 min。冰浴结束2 h后,再次注射同剂量盐酸肾上腺素。
2.6.3 指标测定与数据处理 第8 天给药1 h 后取血,20%乌拉坦麻醉(5.0 mg/kg)后腹主动脉取血,取约4.0 mL加入有肝素钠抗凝剂的EP 管中,全血使用全自动血流变仪测定全血黏度。计量数据采用SPSS19.0 软件进行统计,对数据进行单因素方差分析。
2.6.4 不同制备方法的山楂叶对全血黏度的影响 与空白组比较,模型组高、中、低切变率全血黏度值均明显升高(P<0.01);与模型组比较,山楂叶A、B、C、D 高、中、低剂量组在不同切变率下对全血黏度值均有不同程度影响,其中D 在3 个切变率下各剂量全血黏度均显著降低(P<0.01)。见表2。
表2 不同制备方法山楂叶提取物对全血黏度的影响(mPa·s,±s)

表2 不同制备方法山楂叶提取物对全血黏度的影响(mPa·s,±s)
注:与空白组比较,∗P<0.05,∗∗P<0.01;与模型组比较,#P<0.05,##P<0.01
3 讨论
2015 年版《中国药典》一部中,山楂叶质量标准包括性状鉴定、薄层色谱鉴别以及山楂叶总黄酮和金丝桃苷的测定。目前的质量标准存在质控指标单一,与药效关联性不强等问题。本研究在课题组成果-山楂叶指纹图谱基础上,以中药多组分作用特点,尽可能多的选取色谱峰为研究目标,同时采用面积归一化法测定了指标成分的比例值,面积归一化法可体现每种成分所占总成分的含有量百分比,与中药多组分、多靶点的作用特点相呼应。本实验又利用化学计量学中聚类分析和主成分分析法,以指标成分比例值为分析目标,从不同采集地中排除安徽、广东乳源、广东南昆山、广西桂林、广西贺州、广西梧州、广西玉林及山东维安,最终剩余多个采集地的山楂叶质量可靠、稳定。筛选出的山楂叶样品采用判别分析,建立了质量数学表达式,如有未知质量的山楂叶样品,可把每个色谱峰面积比例值直接带入数学式中,当Y值范围在13.15~16.08 时,未知山楂叶质量符合要求,该药材质量评价的方法简便、可靠。
本实验在优选出山楂叶药材基础上,以活血化瘀药效实验对不同制备方法的山楂叶提取物进行评价。本研究所选取的4 种制备方法山楂叶提取物通过血瘀模型大鼠全血黏度值变化,最终确定4 种制备方法山楂叶提取物均对大鼠全血黏度有不同程度的作用。但是综合不同制法的高、中、低浓度作用于大鼠全血黏度,制备方法D 在低浓度就有显著性差异,而且在不同切变率下均具有显著性差异,最终制备方法D 在全血黏度这项指标上效果更加明显,与活血化瘀作用关联度更加紧密,更加具有实用意义,为最优制备方法提取物。
本研究既保证活血化瘀药效试验样本质量的可追溯性,又以药效试验评价山楂叶制备方法,即筛选优良药材-建立质量数学表达式-符合质量要求药材进行主要药效学试验-最优提取物制备方法选择。

