慢性踝关节不稳的病理机制和评估诊断研究进展
施晓剑 韩甲 刘宇 王雪强 陈佩杰
1上海市第一康复医院(上海 200082)
2上海体育学院(上海 200438)
踝关节扭伤是最常见的运动损伤[1],严重的踝关节扭伤如果没有得到及时有效的处理和治疗,就会逐渐发展成慢性踝关节不稳(chronic ankle instability,CAI)[2]。CAI是由于踝关节及其周围组织发生结构性或功能性的缺损,致使踝关节不稳,患者关节活动受限,平衡和姿势控制异常,并以反复踝关节扭伤为主要临床表现[3]。相较于急性踝关节扭伤,CAI对运动表现和日常活动的影响更大[4];CAI是继发引起下肢其他结构(如前交叉韧带、腓骨肌、腓上支持带等)损伤的重要原因之一。2016年国际踝关节联盟(International Ankle Consortium)共识声明指出,尽管踝关节扭伤的直接治疗成本相对低廉,但是其间接导致的医疗开支却十分高昂。除了考虑与损伤有关的时间消耗成本外,每年与踝关节损伤相关的医疗支出就高达十亿美元,因此,由踝关节扭伤和慢性踝关节不稳导致的负面影响非常值得关注[5]。慢性踝关节不稳对运动机能具有重要影响[6]。本文从疾病分类、病理机制、诊断评估等方面阐述了慢性踝关节不稳的研究进展,以期为后续研究、临床诊疗的发展提供参考。
1 慢性踝关节不稳模型的构建与发展
早期的研究文献显示,CAI传统的分类为机械性不稳(mechanical instability,MI)和功能性不稳(functional instability,FI),前者是指由于韧带损伤,关节软骨或关节囊病变及周围组织损伤导致的解剖结构不稳[7];后者又称感知性不稳(perceived instability,PI),多由神经肌肉协调控制障碍或功能紊乱导致,亦可由机械性不稳逐渐发展而来,即周围结构性的损害可逐渐引起神经肌肉控制的改变[8]。Heterl[7]在早期理论的基础上构建了以机械性不稳和功能性不稳为主要分类的慢性踝关节不稳的病理模型,并认为反复踝关节扭伤(recurrent sprain,RS)是机械性不稳与功能性不稳合并出现时的表现(图1a)。但Hiller[9]等考察了Heterl模型的实际应用后发现,反复踝关节扭伤可以独立于机械性不稳和功能性不稳之外,而非简单的被两者包含的关系,随即对模型进行了再次补充,提出了机械性不稳、功能性(感知性)不稳和反复踝关节扭伤的三元素7亚组模型(图1b)。
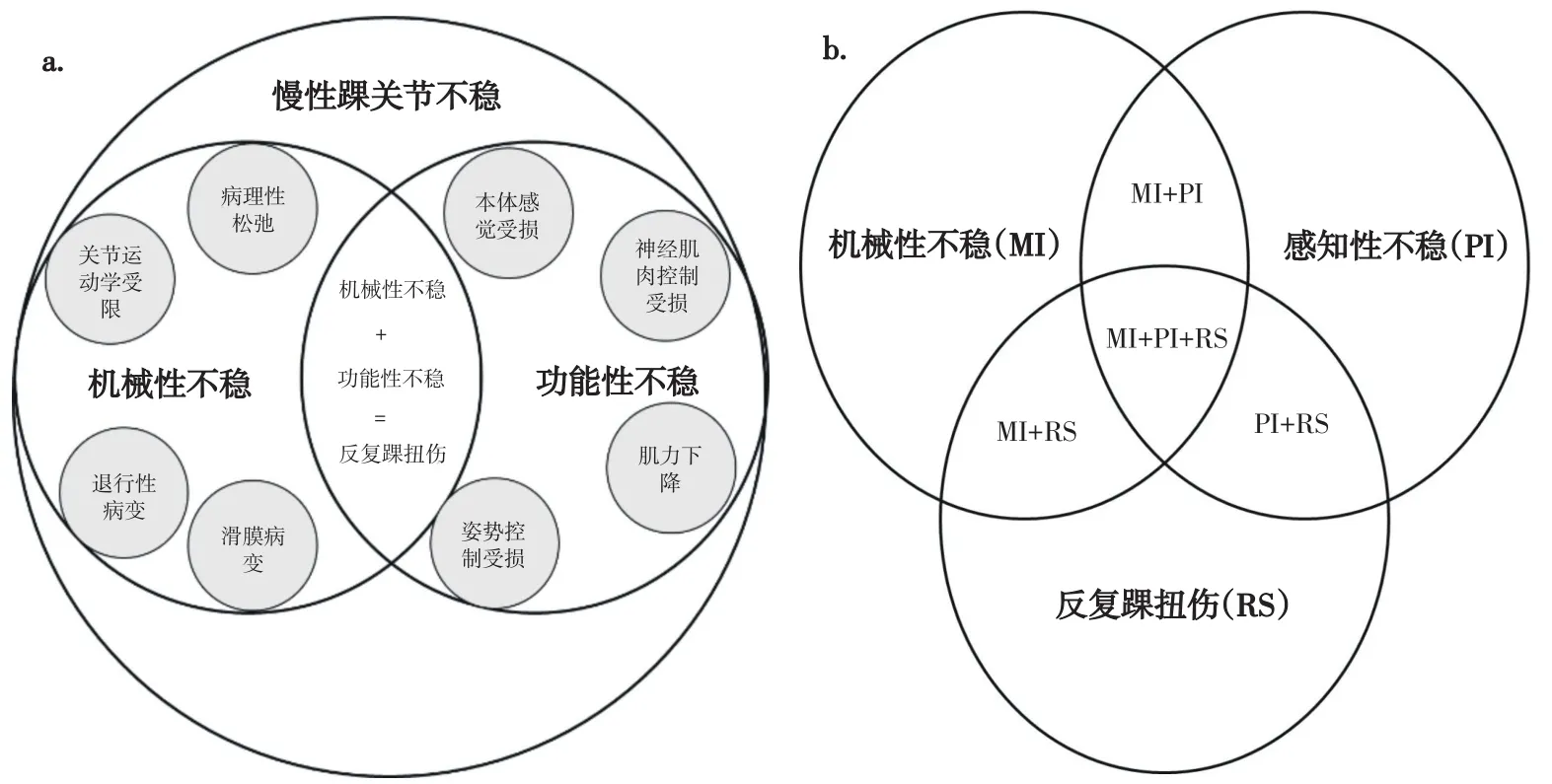
图1 慢性踝关节不稳分类模型[7,9]
Croy等[10]通过超声影像发现,与健康组相比,有踝关节扭伤史组(无主诉症状并且已经回归高强度的体力活动)和慢性踝关节不稳组的前距腓韧带(anterior talofibular ligament,ATFL)长度都显著增加;但有扭伤史组与慢性踝关节不稳组ATFL长度的差异无统计学意义。因此,研究者认为结构性的韧带松弛是导致慢性踝关节不稳的潜在因素而非固有病理特征,不应作为单独的亚组进行分析,并主张将机械性不稳从现有的模型中剔除[11]。可见,慢性踝关节不稳并非简单的踝关节结构松弛,而是一种神经动作控制机能失调综合征。
另外,由于当前的慢性踝关节不稳的模型是基于多因素和不同病理特征进行分类的,因此在不同的亚组间存在较强的异质性,很难对亚组间在运动学、生物力学和形态学等方面的特征进行统一的评价。Terada等[12]尝试采用运动觉、生物力学和心理学测量指标对Hiller模型中的三个亚组(感知性不稳、感知性不稳+反复踝扭伤、反复踝扭伤)进行体系构建,以评价不同亚组特征。虽然这项研究最终未能从生物力学和心理学角度区分三种类型的慢性踝关节不稳,但研究发现踝关节本体感觉信息在外周机械感受器的收集与中枢处理方面对于慢性踝关节不稳具有重要影响,提示踝关节本体感觉机能可能在将来的慢性踝关节不稳模型分类研究中扮演重要的角色,因此需要进一步对踝关节不稳的中枢神经机制进行深入研究。
2 慢性踝关节不稳的神经动作控制机能失调
神经动作协调、精确的控制需要本体感觉信息传入、中枢神经加工处理以及动作输出[13]。以往的研究比较关注慢性踝关节本体感觉的缺失,尤其是踝关节外周感受器的损伤,而近些年的研究表明,慢性踝关节不稳患者神经动作控制机能失调与信号传入、中枢处理、动作输出三个过程都有密切联系[14]。
首先,慢性踝关节不稳患者普遍存在踝关节本体感觉减弱现象,这种本体感觉的减弱可能是引起反复踝关节扭伤的重要原因之一[15]。早期研究的信号“关节传入神经阻滞”(articular deafferentation)理论认为,踝关节周围韧带的损伤导致了韧带内机械感受器的缺损,致使本体感觉信号在向上位中枢传输的过程中发生了“阻滞”[16]。有学者对踝关节周围韧带注射麻醉阻滞药物后发现,韧带内机械感受器的屏蔽会引起被动关节位置觉的下降,但不会影响主动关节位置觉[17],提示韧带和肌梭在编码不同运动形式的本体感觉信息时具有特征性差异。尽管这些研究对于我们理解不同机械感受器在本体感觉的作用方面具有重要意义,但这些研究都过于强调本体感觉的外周传输机制,即认为踝关节机械感受器受损是导致踝关节本体感觉下降的主要原因。然而越来越多的研究证据表明,CAI患者踝关节本体感觉的中枢处理进行了适应性改变。例如,有研究发现踝关节不稳患者的双侧踝关节本体感觉机能都显著低于健康对照组,且单侧踝关节不稳的患者的健侧的本体感觉与患侧无显著差异[18],提示高位中枢的神经可塑机制可能通过“串扰”(cross talk)或“通用运动程序”(common motor program)使踝关节健、患侧的本体感觉机能相对均衡,从而达到对患侧的保护[18]。因此,信号阻滞假说并不能完全解释慢性踝关节不稳患者本体感觉机能下降的机理。
第二,在本体感觉信号的中枢处理与调控方面,越来越多的证据表明,慢性踝关节不稳患者的中枢处理机制会发生变化。有研究表明,踝关节不稳患者在运动中更多地使用视觉信息,提示大脑可能受本体感觉信息缺损的影响,而对不同感觉信息进行再次权重(re-weighting),从而对本体感觉进行代偿,以优化传入信息整合[19]。另外Witchalls等[20]发现在本体感觉重复测量过程中,慢性踝关节不稳患者的学习效率显著低于健康人,提出慢性踝关节不稳可能会抑制中枢对于运动学习的效率。Kosik等[21]借助核磁成像技术发现慢性踝关节不稳患者的腓骨长肌在大脑功能区的支配面积减小,提出这可能是功能脑区聚焦式的提高与腓骨长肌的关联度以减少再次损伤风险的代偿机制,此外,减少的功能区会被其他的功能区支配,也可以用于解释在踝关节损伤后下肢运动学的改变。
第三,从动作输出方面来看,早期研究表明,CAI患者表现出较差的姿势和平衡控制能力,可能与踝关节活动受限和肌力不足有关[22]。肌力和关节活动度是下肢运动中足廓清功能的重要保障,在近期的研究中,Kim等[23]采用3D运动捕捉系统(VICON)记录了受试者在测力台上进行单腿落地后横向跳跃的动作测试结果,通过采集CAI患者在动作测试中的下肢生物力学参数,发现与健康同龄控制组相比,CAI患者的踝关节和膝关节处的力矩都显著下降。研究者认为踝关节处感觉运动缺失所致的神经驱动作用可能具有抑制膝关节处肌力的效应。此外,多数研究发现CAI患者在运动中下肢的运动策略会发生改变。如Son等[24]发现,CAI患者在跑跳运动中胫骨前肌、腓骨长肌等处的肌电信号均发生不同程度的衰减,且对髋和膝关节的屈曲运动控制要求显著增加。尽管很多学者认为CAI患者下肢运动力学的改变是一种保护性代偿,以避免踝关节损伤再次发生,然而目前还缺乏前瞻性研究论证动作模式改变与踝关节不稳的因果关系;同时也缺乏大样本的流行病学调查,说明踝关节不稳患者是否具有更高的下肢其他部位损伤风险。
以上研究表明,CAI患者踝关节本体感觉的下降不仅源于外周组织中本体感受器功能的受损,还在于神经传入-中枢处理-动作传出闭合环链系统的失调。随着大脑影像学技术的发展(如最近Nature报道了穿戴式可移动的脑成像设备[25]),未来的研究可能通过建立影像学和行为学之间的神经网络,从而更好地解释CAI形成和发展的机理,及其如何影响下肢动作控制与运动表现。同时,中枢神经可塑性机制为踝关节不稳的干预提供了新的思路,但所有的干预都必须建立在可靠、有效的评估之上。
3 慢性踝关节不稳的临床评估与诊断
CAI在临床上有多种评价与诊断方法,主要包括自陈量表、理学测试、影像学检查和功能性测试。
3.1 自陈量表
临床上,CAI的诊断仍缺乏“金标准”,研究者开发了不同版本的评价踝关节不稳的量表作为对疾病的主观判定办法(表1),但其诊断的信、效度和检验效能(灵敏度和特异度)并没有得到统一的考证。Eechaute等[26]对临床上采用的CAI患者自陈量表进行系统回顾,在对信度和效度进行考察后指出,足踝残疾指数(foot and ankle disability index,FDAI)和功能性踝关节稳定测试(functional ankle ability measure,FAAM),后者进一步分为运动亚问卷(FAAM-sport subscale,FAAM-S)和日常生活能力亚问卷(FAAM-ability of daily life subscale,FAAM-ADL),两者相比踝关节功能评估工具(ankle joint functional assessment tool,AJFAT)和功能性踝关节结局评分(functional ankle outcome score,FAOS)对评价因CAI导致的功能缺失具有更好的评估和诊断价值。Eechaute等[27]又开发了慢性踝关节不稳量表(chronic ankle instability scale,CAIS),发现该量表与运动能力测试表现之间具有较高的相关性,因而具有良好的外在效度。Donahue等[28]对涉及CAI的7个自陈量表采用回归分析后发现,踝关节不稳计(ankle instability instrument,AII)和坎伯兰踝关节不稳工具(Cumberland ankle instability tool,CAIT)能够预测Freeman[16]提出的功能性踝关节不稳的最小标准,并且都具备较高的诊断灵敏度和特异度。Simon[29]在前期研究的基础上,将CAIT与AII进行整合,开发了功能性踝关节不稳确认问卷(identification of functional ankle instability,IdFAI),并且证明了 Id-FAI在诊断CAI时具有良好的检验效能。
在自陈量表的应用方面,Freeman[16]最早对慢性踝关节的临床自述进行了描述,即踝关节扭伤后具有经常打软(giving away)的现象。Gribble等[34]通过系统综述推荐CAIT、AII、IdFAI均可作为是否具有踝关节不稳的筛查指标,而对于不稳导致的功能障碍程度的评估推荐采用FAAM和FADI。同时Wilstrom等[35]对2013年前发表的CAI研究的纳入标准进行系统回顾后指出,慢性踝关节不稳的最低纳入标准应该包括:(1)初次外侧踝关节扭伤较为严重,需要使用护具1周以上,或至少3天以上的制动或不能负重;(2)至少12个月未发生再次损伤,能够回归到中等强度以上的负重体力活动;(3)无或有最小程度的自我陈述功能障碍。这些慢性踝关节不稳受试者的主观纳入标准已经逐步被多数研究者采纳并使用到他们的研究中。
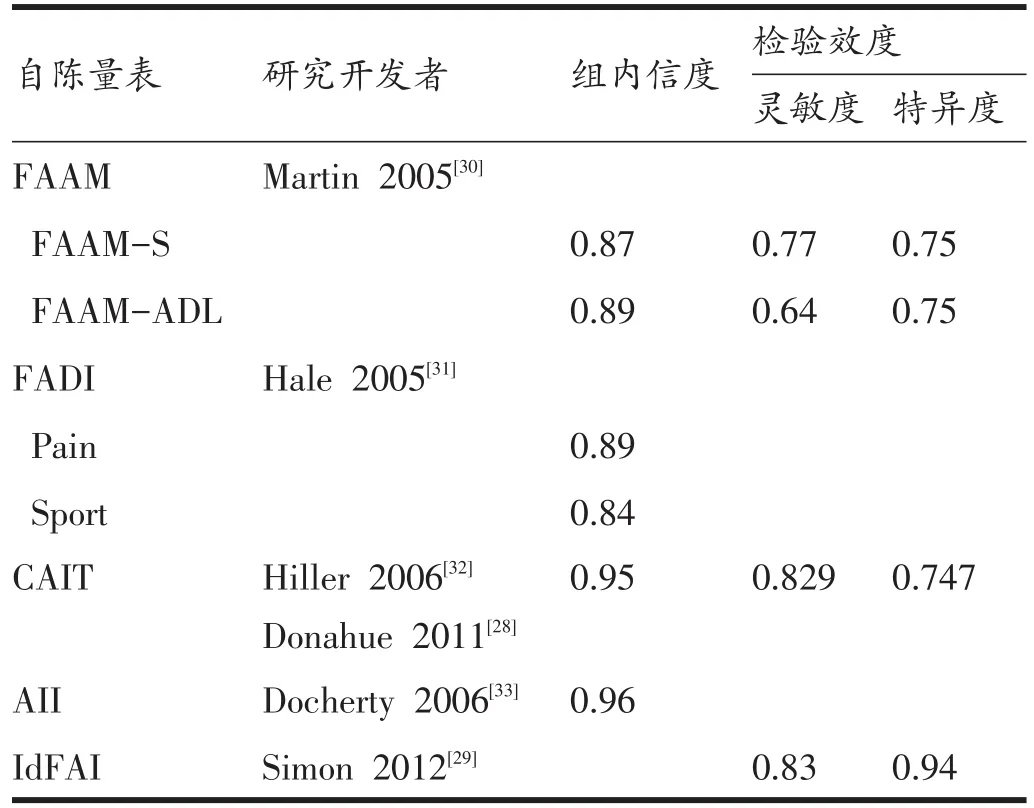
表1 常用慢性踝关节不稳自陈量表
目前,被开发用于CAI患者的自陈量表有10种,然而在实际使用中,多数自陈量表仍偏向于研究领域而非临床实践,导致自陈量表的临床应用不够完善的主要原因可能是开发者的开发意图不一致。尽管当前纳入的自陈量表对CAI患者功能评估均具有较高的敏感度,然而由于缺乏有效的诊断切点值或检验效能不足,多数自陈量表并不能够在临床上作为有效的筛查和诊断工具。因此,有学者指出在现阶段的临床和科研中鼓励多种量表结合的使用方法来弥补单个量表评估或检验效能不足的问题[36]。基于此,在后续研究中,进一步优化自评量表的内容结构以及寻找有效的诊断切点值将是后续临床应用型自陈量表开发者亟需解决的问题。
3.2 理学测试
在临床检查与评估中,康复治疗师经常会使用理学检查,判断结构是否有损伤,甚至可以大致评定损伤的程度,为后续治疗方案的制定提供依据。对于CAI的检查,大部分理学测试主要关注结构性的松弛,测试中通过施加应力牵拉韧带,根据检查者感知的松弛度(终末感)和患者所产生的症状(多数为疼痛)进行诊断及程度分级。见表2。
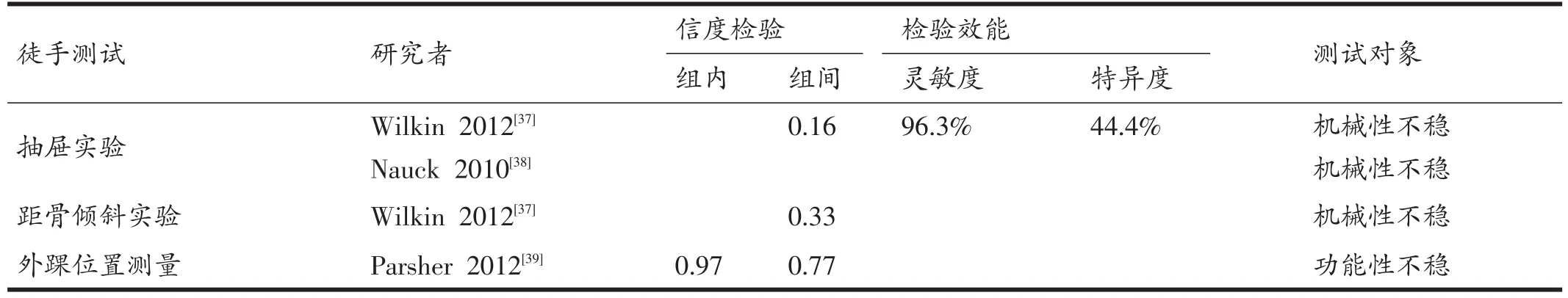
表2 常用慢性踝关节不稳徒手理学测试
3.2.1 前抽屉试验
前抽屉试验(anterior drawer test)是用于测试踝关节前距腓韧带(ATFL)松弛度的主要徒手测试之一,临床上主要用于诊断踝关节韧带松弛引起的机械性不稳[40]。在检查中距骨向前滑动超过4毫米被认为前抽屉实验检测阳性[41]。前抽屉测试的检验效能受检查者施力大小的影响,施力过小不足以产生有效的距骨滑动,施力过大容易引发踝关节周围肌肉收缩反应,此外暴力可能会引起假阳性结果的出现,甚至引发再次损伤。Tohyama等[42]通过人体标本测试施力大小对于前抽屉测试结果的影响,发现在测试时施加30 N的力能够更好地产生距骨的前移,即能够更好地检测韧带的完整性。
有学者[43]认为前抽屉试验在测试时只是单纯的距骨前后向滑动,而没有考虑到距骨生理性的前外侧旋转,并且这种生理性外旋会使内侧三角韧带紧张而限制测试的精度。Phinit等[44]主张改良前抽屉试验测试,通过放在后踝的食指和中指以及放在外踝前侧的拇指使踝关节产生轻微的内旋和前向的组合运动,即前外抽屉实验(anterior lateral drawer test)。Miller等[45]通过尸体标本研究发现,前外抽屉实验相比前抽屉实验能够产生近2倍的距骨前向滑动,表明前外抽屉实验可以有效解除周围组织的限制,并且这种滑动的增加可能会有利于测试者进行判断,从而增加测试结果的准确性。前外抽屉虽具有高的敏感度和特异度,但限于研究的结果是在人体标本上获取的,因此其信效度和检验效能仍需进一步临床验证。
3.2.2 距骨倾斜试验
距骨倾斜试验(talar tilt test)主要用于检测前距腓韧带和跟腓韧带的完整性,也是踝关节机械性不稳的徒手检查的主要手段之一[46]。1995年McCaskie等[47]就报道了全身麻醉下进行距骨倾斜试验可以确诊CAI的研究。然而,与前抽屉试验一样,受限于测试者施力因素的影响,两者的组内信度均比较低,但距骨倾斜实验的组内信度仍优于前抽屉实验[37],这可能与该测试受到其他韧带及周围结构的干扰较少有关。通过对踝关节测试仪与徒手距骨倾斜试验进行比较后发现,两者在CAI的诊断中虽然灵敏度均较低,但均具有较高的特异度,因此距骨倾斜试验可以作为CAI的排除诊断方法之一[46]。
由于徒手抽屉测试和距骨倾斜测试都受测试者本身主观用力因素的影响,因此在徒手测试时不同测试者间的组间一致性较低,很难定量化地评价不同踝关节韧带稳定性之间的差异。Docherty等[48]采用LigMaster关节活动计(ligmaster joint arthrometer)在150 N的力下进行前抽屉试验和距骨倾斜试验,得到较高的组内和组间信度。尽管借助这种仪器进行测试在临床中应用有一定困难,但良好的组内测试信度仍然保证了徒手应力测试可以作为检测踝关节稳定性较为可靠的手段。
3.2.3 外踝位置测量
外踝位置测量(distal fibular position)是一种间接测量CAI患者外踝位置偏移角度的方式。早期有学者对踝扭伤的患者进行回顾性研究发现,腓骨远端(外踝)位置都普遍靠后,提出这种位置错位可能与再次发生损伤有关[49]。Berkowitz等[50]对1998年至2001年间因CAI而手术的病人的术前影像学资料进行分析,通过测算轴向踝指数(axis malleolar index,AMI)发现,与正常踝关节相比AMI普遍增大,提出外踝位置靠后可能会容易导致踝关节不稳。Hubbard等[51]的发现却与之前研究相反,单侧CAI的患者的外踝会倾向于靠前而不是靠后。尽管对于外踝位置变化存在争议,但CAI的发生均与外踝位置的异常有关。这种位置的异常可能会限制和改变踝关节正常的关节运动,从而增加损伤的风险。Parasher等[39]对外踝位置测量进行信效度考察后发现,外踝位置测量具有较好的组内(0.97)和组间信度(0.77),然而该研究所纳入的受试者包含了部分健康群体,因此该信效度检验无法在测试CAI时具有良好的代表性。基于外踝位置测量无法特异性地区分个体变异与损伤所致外踝角度偏倚之间的差异,因此在实际临床工作中,外踝位置测量仅能作为参考辅助诊断而不具备真正的诊断效度。
3.3 影像学检查
3.3.1 应力XX线摄像技术
理学测试在临床上使用便利,但对损伤部位的定位不够明确,因此仍需借助其它辅助手段来提高诊断的精准度[52]。X线是用于诊断踝关节不稳结构因素的辅助手段之一,多用于检查胫腓下联合,踝关节内外侧副韧带的完整性。临床上在检查慢性踝关节机械性不稳时,采用X线结合徒手或应力装置,即应力X线技术(stress radiograph)对韧带和距骨位置进行拍摄。Lee等[53]对单侧CAI患者分别采用徒手前抽屉试验、距骨倾斜试验和X线下前抽屉试验对距骨倾斜角和旋转角进行测量后发现,X线下前抽屉试验相比其它两种测试具备更好的组内和组间信度。X线可用于拍摄矢状面下距骨的位置,通过测量胫骨下端前缘与距骨穹顶前缘的距离来定量计算距骨的位置变化,辅助诊断CAI[54]。Wikstorm等[55]通过测量发现在矢状面上CAI患者的患侧踝关节与健侧及健康人相比,距骨位置更加靠前,并且该测试具有较高的组内(0.90)和组间信度(0.78)。
计算机断层扫描(computed tomography,CT)与X线相比,在踝关节结构成像和形态学参数测量方面具有明显的优势[56]。临床上,CT可替代X线对踝关节的结构进行断层扫描,检查踝关节周围韧带完整性。Kobayashi等[57]借助CT检查发现CAI患者腓骨远端与健侧相比位置靠外,因此,CT结合三维成像技术可用于观察CAI患者胫腓骨的排列情况,对CAI做出辅助诊断。
3.3.2 磁共振成像技术
磁共振成像(magnetic resonance imaging,MRI)相比于X线技术,在韧带等软组织结构的成像上具有显著优势。T1加权像下正常的距腓前韧带在冠状面表现出从腓骨远端(外踝)至距骨的细长的低信号带,跟腓韧带在冠状面上则表现为从跟骨连至腓骨的圆形均质低信号结构[58]。当存在慢性踝关节机械性不稳时,MRI影像可表现为韧带结构的缺失、信号的中断或不连续,或表现出波浪或卷曲状的韧带轮廓[59]。Jolman等[60]回顾了临床187名主诉踝关节不稳的患者资料,发现MRI虽然对于CAI诊断的灵敏度较高,但特异度较低,因此提出MRI不应该作为踝关节不稳的常规诊断工具。然而,Kanamoto等[61]分别收集了慢性踝关节不稳患者术前MRI和应力X线影像资料,在与手术探查结果进行对照后发现MRI检查能够准确地区分CAI患者距腓前韧带的增厚及缺损的情况,而在应力X线下测量距骨倾斜角度不能判断韧带实际的损伤情况,因此提出在临床诊断中MRI仍可以作为应力性X线的补充检查手段。
Seebauer等[62]尝试将应力性测试(前抽屉试验、距骨倾斜试验)与MRI特点相结合,采用碳纤维合成材料开发了MRI兼容应力装置,该装置可以在MRI环境下安全使用,通过对15名CAI患者与健康受试者进行测试,所有的应力性测试中都存在显著性差异。相比于应力X线,MRI结合应力性测试装置时的成像更加清晰,并且还可以反映应力性测试中的性别差异以及各应力性测试间的相关性。该技术将有助于诊断的精准化,以及推动徒手测试方案在后续操作中的改良。
3.3.3 超声成像技术
超声(ultrasound,US)技术可用于观察CAI患者踝关节周围软组织及韧带结构的完整性,Guillodo等[63]分别采用CT和超声对无疼痛症状的CAI运动员的胫腓前韧带进行探查,以CT作为诊断的“金标准”时发现,US具有较高的灵敏度(84.6%)和特异度(100%),提出US可以在一定程度上替代CT,从而减少运动员X线暴露的累计时间。
Lee等[64]报道了超声结合前抽屉试验检查CAI患者距腓前韧带完整性的技术,即应力超声(stress-ultrasound)技术。检查时,检查者用超声探头在被检查者前抽屉试验的起始位和终止位分别记录距骨骨性标记点与外踝前外侧的直线距离作为距腓前韧带的长度,并计算距腓前韧带的伸长变化量,再与徒手前抽屉试验和应力X线结果相比,三者间具有良好的相关性,并且应力超声技术比应力X线操作更加简便。Cho等[65]随后为进一步评估该技术的诊断价值,采用应力X线、MRI和关节镜技术与应力超声技术进行对照,发现在显示踝关节不稳的灵敏度上应力超声甚至优于MRI和应力X线技术,因此提出应力超声技术可与徒手前抽屉试验和应力X线技术一样,作为CAI的主要检查手段之一。此外,超声成像技术还可以用于动态观察CAI的踝关节运动轨迹,这将为深入了解CAI患者踝关节生物力学和运动学改变提供便利[66]。
影像学技术的发展推进了CAI精准诊疗的进程。大量的动静态影像学信息丰富了探究CAI病理机制的研究路径,但同时也容易导致构建错误的表象因果关系以及干扰疾病的诊断。CAI是以功能损害为主导的慢性进展性运动损伤疾病,影像学技术的应用必须结合其它功能性检查资料,才能对疾病的机理做出较为准确的判断(表3)。
3.4 功能性测试
功能性测试是除自陈量表外,评价CAI患者下肢运动控制功能的主要手段。星状平衡偏移测试(star excursion balance test,SEBT)是临床常用的功能检查方法之一,具有较高的信效度[68]。SEBT能够对下肢的肌力、关节活动度、动态平衡和姿势控制能力,以及本体感觉进行评价[69]。
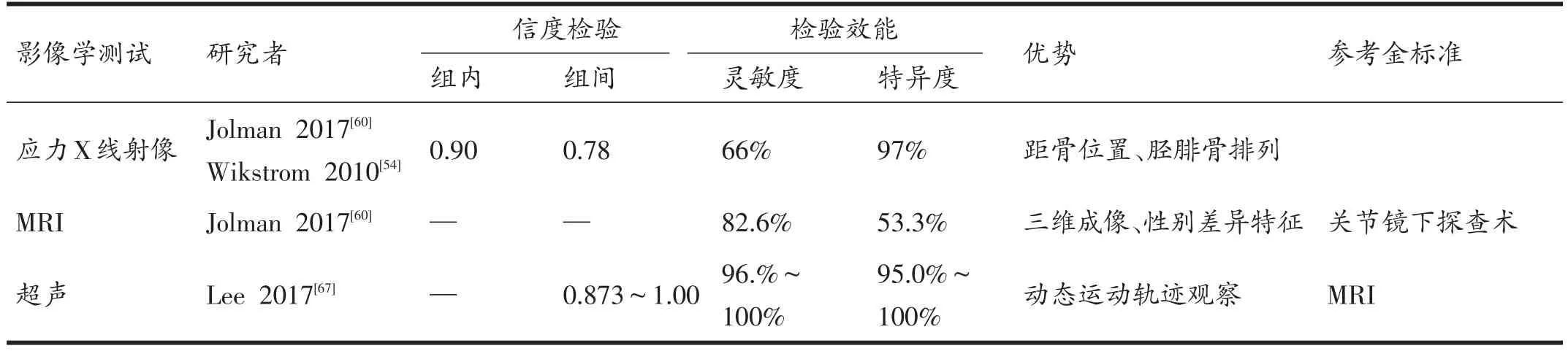
表3 常用慢性踝关节不稳影像学检查
早期的版本中,SEBT共有8个方向,后期的研究发现前向(SEBT-A)、后外向(SEBT-PL)和后内向(SEBT-PM)与下肢的姿势控制和平衡能力有显著的相关性[70],因此对SEBT进行了简化,以增加测试的效率,减轻被测者因为疲劳对检查结果的影响[71]。但Razeghi等[74]采用简化版的SEBT对CAI的女性运动员进行测试,发现在SEBT的任何方向上与健康组都没有显著差异,认为简化版的SEBT可能对CAI的鉴别敏感度不够,不主张在进行CAI的检查时对SEBT进行简化。简化版的SEBT测试与Y平衡测试(Y-balance test,YBT)相似,均由3个运动测试方向构成(前向、后内向、后外向)[72]。Fullam等[73]通过生物力学分析手段发现在前向测试中,与SEBT测试相比,YBT测试对受试者髋关节的屈曲运动程度要求更高,提示YBT测试与SEBT测试两者间仍然存在着一定的神经肌肉控制的差别。
除SEBT以外,单腿站立测试也是最常用的评价静态平衡能力的测试手段之一,并且在该测试动作为基础的多项指标中,到达支撑面边界时间(time to boundary,TTB)被认为是反映下肢静态平衡和姿势控制能力的较好指标[19]。TTB测试需要借助测力台,被测者单腿站在测力台的中心并保持10秒,计算机通过记录身体重心的位置和移动速度,估算出重心偏离足底支撑面所需的时间,时间越长代表下肢的静态平衡和姿势控制能力越好,反之则越弱[75]。Hertel等[76]采用测力台测量CAI患者与健康人,发现TTB相比传统重心移动参数(如压力中心晃动距离,压力中心移动速度矩),能够更敏锐地探测出CAI患者与健康人相比姿势控制的差异。因此,与传统的重心移动参数相比,TTB能够更好地反映被测者主动控制和调整的能力。但由于需要借助于测力台,因此较难在临床上应用与普及。
功能性测试对于评价CAI患者的功能状态具有较高的生态效度,然而,在实际应用中测试结果往往受到诸多外在或内在因素的限制。一方面测试难度过大或测试时间过长会引起被测试者的不适和疲劳,由此可能导致不同被测试者间及不同研究间的横向可比性不高[77];另一方面,被测试者自身的运动学习效应也可能导致测试者对被测试者运动能力产生评价偏差。因此,功能测试在开发的过程中,不仅要关注不同运动控制模式对测试结果的影响,还需对测试的流程和休息间歇进行合理标准化的设置,以期实现最优化功能测试的检验效能。
4 总结
在当前研究中,CAI的模型分类仍然不够清晰,机械性不稳与功能性不稳并非是两种可以独立分开的病理机制,由于韧带及周围组织损害导致的机械性不稳的病理机制仍需要进一步探讨。然而,越来越多的研究者已经意识到CAI的中枢神经控制异常可能是引起踝关节损伤后向CAI转变的核心机制,踝关节本体感觉中枢机制的研究将是未来研究热点。
在临床诊疗实践中,一方面,受限于现有诊断工具检验效能的局限性和自身特点,CAI的诊断必须在搭建最优化的诊疗逻辑框架基础之上,避免由错误表象关系的构建所导致的疾病误诊和漏诊;另一方面,随着对于CAI病理机制研究的不断深入,诊断工具的证据等级将会不断得到更新,利用前沿技术和最新证据不断更新现有的诊疗逻辑框架结构是推动精准化医疗以及循证医学发展的主流路径。在未来的研究中,研究者有望采用动态超声、近红外光谱技术,甚至可穿戴式的脑电成像等手段对CAI患者在运动中的变化进行进一步的观察,通过不断地优化神经及运动学参数有望建立以神经肌肉控制缺损为核心的CAI病理模型以及临床诊疗思路的新方向。

