以重度高钙血症为首发症状的一例B细胞性淋巴瘤PET/CT显像及文献复习
于艳霞,晁芳芳,韩星敏
郑州大学第一附属医院核医学科郑州450052
以高钙血症为首发症状的B细胞性淋巴瘤的相关报道较为少见,同时描述其PET/CT影像学表现的文献更为少见。现将郑州大学第一附属医院收治的以重度高钙血症为首发症状的一例B细胞性淋巴瘤患者报道如下,并结合相关文献就其可能的发病机制进行阐述。
1 临床资料
患者,男,67岁,于2017年10月因“食欲减退10 d,发现血钙高12 h”为主诉入院。10 d前患者无明显诱因出现食欲减退,伴夜间多汗、全身乏力,至当地医院就诊。查电解质:血钙5.00 mmol/L,血钠132 mmol/L,血钾4.5 mmol/L。予以补液、利尿、补钾等治疗,效差,遂来郑州大学第一附属医院,急诊以“高钙血症”为诊断收住,发病以来,体重下降10 kg。
入院后完善相关检查。甲状旁腺激素(PTH)3 210 pg/L(降低)。电解质:血钾4.66 mmol/L(正常),血钠 132 mmol/L(降低),血钙 4.54 mmol/L(升高);予以补液、利尿等对症支持治疗,并密切监测电解质变化。血同型半胱氨酸38.39μmol/L(升高),N 端脑钠肽前体(BNP)2.45 μg/L(升高),乳酸脱氢酶(LDH)2 458 U/L(升高);心电图、心肌酶正常。患者炎症指标白细胞计数、红细胞沉降速率、C-反应蛋白升高。肺部CT示双肺轻微炎症。予以补液、利尿、降钙(艾本、降钙素、双磷酸盐)、护胃、营养心脏等治疗,后多次复查血钙,持续降低至1.88 mmol/L。
患者饮食、睡眠质量较差,精神欠佳。头颅MRI示:双侧额顶叶、侧脑室旁脑白质脱髓鞘;右侧额叶、双侧侧脑室旁、基底节区、左侧丘脑脑梗死。
为寻找高钙血症原因,行尿本周蛋白电泳、血清免疫球蛋白固定电泳,均阴性。骨代谢指标:骨型碱性磷酸酶225 U/L(升高),降钙素原2.115μg/L(升高),N-MID 骨钙素6.93 μg/L(降低),25-羟基维生素D3、β胶原特殊序列测定均正常。肿瘤标志物:铁蛋白>1 000μg/L(升高),神经元特异性烯醇化酶 98.482 μg/L(升高),AFP、CEA、CA125、CA19-9、CA72-4、CA15-3、前列腺特异性抗原、游离前列腺特异性抗原、非小细胞肺癌抗原21-1均阴性。PET/CT示:脾脏不均匀性代谢活跃,SUVmax约14.2;肝脏弥漫性代谢活跃,SUVmax约7.0;双侧肾上腺增粗,代谢活跃,SUVmax约7.7;全身骨骼多发不均匀性代谢活跃灶,SUVmax约21.2;左侧髂窝软组织肿块代谢略活跃,SUVmax约1.7(图1)。综上,考虑血液系统疾病,诊为淋巴瘤。
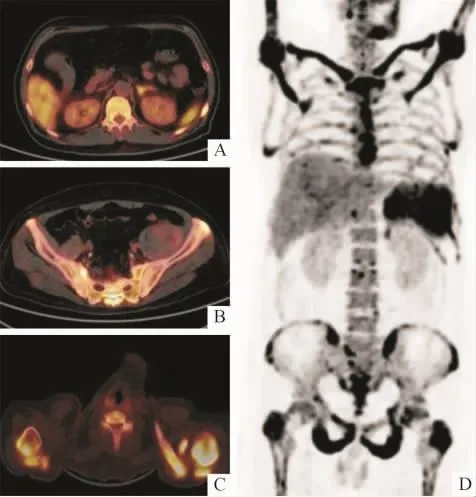
图1 B细胞性淋巴瘤患者PET/CT影像表现
随后行CT引导下坐骨穿刺活检术,病理提示高级别B细胞性淋巴瘤。穿刺后次日晚,患者突发意识不清、呼吸急促、阵发性全身抽搐,伴牙关紧闭,口角稍向右偏斜,急查血气分析示代谢性酸中毒。心电图示急性前间壁心尖部心肌梗死、下壁心肌呈梗死样改变。心肌酶谱和BNP均明显升高。头颅CT无异常。患者血乳酸明显升高,有癫痫发作症状,首先考虑代谢紊乱所致,给予纠正酸中毒等对症治疗。患者处于浅昏迷状态,家属强烈要求出院,于出院后不久死亡。
2 讨论
高钙血症是指血清游离钙﹥2.6 mmol/L,其主要病因是原发性甲状旁腺功能亢进症和肿瘤性高钙血症。本例患者PTH水平降低排除原发性甲状旁腺功能亢进症可能。肿瘤性高钙血症常伴有全身多脏器的转移,可迅速导致肾脏、神经系统受损,甚至心跳骤停。血液系统肿瘤伴发高钙血症常见于多发性骨髓瘤和淋巴瘤,本例尿本周蛋白电泳、血清免疫球蛋白固定电泳均阴性,结合影像学表现排除多发性骨髓瘤可能。B细胞性淋巴瘤仅约7.1%发生高钙血症[1],以高钙血症为首发症状的病例更为少见。
检索“中国知网”“万方医学网”两大数据库,复习近10 a国内文献,以“高钙血症”为首发症状的恶性淋巴瘤共7篇文献8例患者。检索近10 a PubMed文献,共20篇个案报道,只有4篇描述以“高钙血症”为首发症状的恶性淋巴瘤患者的PET/CT影像表现[2-5],其中3篇 PET/CT显示累及骨骼[3-5]。本例患者坐骨穿刺病理示高级别B细胞性淋巴瘤,且以高钙血症为首发症状,临床罕见。PET/CT示脾脏、肝脏、双侧肾上腺、全身骨骼代谢活跃,较为明确地显示出肿瘤累及范围,且考虑为血液系统疾病导致,诊断为淋巴瘤。全身骨骼代谢活跃,SUVmax约21.2,同机CT示双侧锁骨、肩胛骨可见轻度虫噬样骨质改变,余全身骨骼骨质改变不明显。由此可见PET/CT可在早期发现淋巴瘤的骨骼浸润。PET/CT还发现左侧髂窝软组织肿块代谢略活跃,SUVmax约1.7。由于患者病情危急,未能取得病理结果。但是该肿块的SUVmax较低,与肝、脾、双侧肾上腺、全身骨骼的代谢程度明显不同,所以作者认为左侧髂窝软组织肿块不考虑为淋巴瘤累及所致。
恶性肿瘤发生高钙血症的机制包括以下3种。①局部溶骨性因素:肿瘤细胞通过骨转移、骨质破坏,骨钙直接进入血液,以及分泌具有溶骨活性的破骨细胞激活因子,刺激骨吸收,导致骨质溶解和高钙血症。本例中PET/CT示全身骨骼不均匀性代谢活跃,考虑为淋巴瘤的骨骼浸润所致的高钙血症。②体液性因素:主要是甲状旁腺激素相关蛋白(PTHrP)分泌增加,有时亦可通过1,25-二羟维生素D3介导引起。PTHrP因其N末端氨基酸序列与PTH同源,故具有与PTH相似的作用,即通过破骨细胞的效应提高骨吸收,并作用于肾脏上的PTH受体,增强钙的吸收,从而引起高钙血症[6]。本例患者由于条件限制,没有检测PTHrP,25-羟基维生素D3水平正常。③肿瘤高负荷:晚期恶性肿瘤患者肿瘤细胞负荷高,与病情进展迅速及化疗药物引起肿瘤细胞裂解有关,常伴有肿瘤溶解综合征,血清LDH、β2微球蛋白、血尿酸明显升高。
高钙血症治疗的基本原则为促进钙排出、抑制破骨细胞性骨吸收及治疗原发病。唑来膦酸联合降钙素及水化、利尿等综合治疗措施对恶性肿瘤性高钙血症疗效肯定[7-8]。研究[1]表明淋巴瘤伴高钙血症者多数预后较差。本例患者经过有效的治疗,血钙水平降低,但是病情仍然持续恶化。
综上,以高钙血症为首发症状的高级别B细胞性淋巴瘤患者临床少见,PET/CT在其诊断及分期中起到了重要的作用。