重症医学科脓毒症和脓毒性休克患者影响预后相关因素分析
王宝权, 李 男, 付海燕, 胡占升
脓毒症是指明确或可疑感染引起的全身炎性反应综合征。严重脓毒症是指脓毒症伴由其导致的器官功能障碍和/或组织灌注不足。脓毒性休克是指脓毒症伴由其所致的低血压,虽经液体治疗后仍无法逆转。这是危重病和危重病医学面临的重要临床问题。全世界脓毒症患者人数每年超过1 900万,其中600万人死亡,死亡率超过1/4,约300万幸存患者有认知功能障碍[1-6]。在重症医学科(ICU),约10%~25%的患者住院期间发生过重症脓毒症,其中19%~47%的患者死亡。本研究旨在探讨脓毒症和脓毒性休克患者的死亡危险因素,以提高对脓毒症的认识,并指导临床治疗与预后评 估。
1 材料与方法
1.1 研究对象
选取2016年6月-2018年10月我院ICU严重感染患者,入院的患者符合预先确定的纳入和排除标准,最终共168例纳入研究。
1.2 诊断标准
1.2.1 入选标准 根据 2018年《中国脓毒症/脓毒性休克急诊治疗指南》中关于脓毒性休克的诊断标准[1]:对于感染或疑似感染的患者,当脓毒症相关序贯脏器衰竭评估(SOFA)评分较基线上升≥2分可诊断为脓毒症。严重脓毒症是指脓毒症伴由其导致的器官功能障碍和/或组织灌注不足。脓毒性休克为在脓毒症的基础上,出现持续性低血压,在充分容量复苏后仍需血管活性药物来维持平均动脉压(MAP)≥65 mmHg(1 mmHg=0.133 kPa)以及血乳酸浓度>2 mmol/ L。年龄≥18周岁。预期ICU住院时间≥72 h。
1.2.2 排除标准 年龄<18岁;妊娠;住院时间<72 h者;急性脑血管事件入院;急性冠脉综合征;严重心律失常;合并中心静脉置管禁忌;家属签署“拒绝积极抢救”的意见;数据缺失及失访者。
1.3 方法
1.3.1 一般资料 收集纳入病例的一般信息包括性别、年龄;住院时间;患者是否伴有冠状动脉粥样硬化性心脏病、慢性阻塞性肺疾病(COPD)、糖尿病、高血压等基础疾病;患者是否有癌症病史、脑卒中病史及慢性肾功能不全病史;感染部位及来源;记录入住ICU后12~24 h、25~36 h、37~48 h的基线中心静脉血氧饱和度、白细胞、血乳酸、C反应蛋白、血小板计数、凝血酶原时间、血肌酐以及动脉血氧分压与吸入氧浓度之比(PaO2/FIO2);患者入ICU时急性生理与慢性健康评分(APACHE Ⅱ评分)及基线;24 h、48 h的SOFA评分[1]对呼吸、凝血、肝脏、心血管、中枢神经系统、肾脏6个系统功能的总体评估。
1.3.2 统计学分析 采用 SPSS 20.0 软件进行数据整理、筛选与统计分析:正态分布数据以平均数±标准差(x±s)形式记录,非正态分布计量资料以中位数(四分位数)[M(P25,P75)]形式记录,计数资料数据以n(%)形式记录。正态计量资料采用独立样本t检验进行组间比较,非正态计量指标采用Mann-Whitney检验进行组间比较,计数指标采用卡方检验(必要时辅以精确概率法)进行比较;采用强制进入法将可能影响患者生存的相关因素进行多因素logistic回归分析,探究患者生存状态的相关影响因素。采用0.05检验水准,P<0.05则差异具有统计学意义。
2 结果
2.1 一般资料
共有168例符合入选标准的脓毒性休克患者,其中66例在出院后60 d内死亡,病死率为39.3%,102例存活。生存组和死亡组在性别、年龄与住院时间上差异无统计学意义。两组患者相比,死亡组入院时的APACHE Ⅱ评分更高(P<0.05),差异具有统计学意义。见表1。
2.2 感染部位
168例患者感染部位为:肺部50例,胃肠道69例,肝胆系统25例,泌尿系统12例,原发性败血症6例,盆腔感染3例,其他3例。生存组与死亡组患者感染部位差异无统计学意义(χ2=11.110,P=0.085)。见表2。
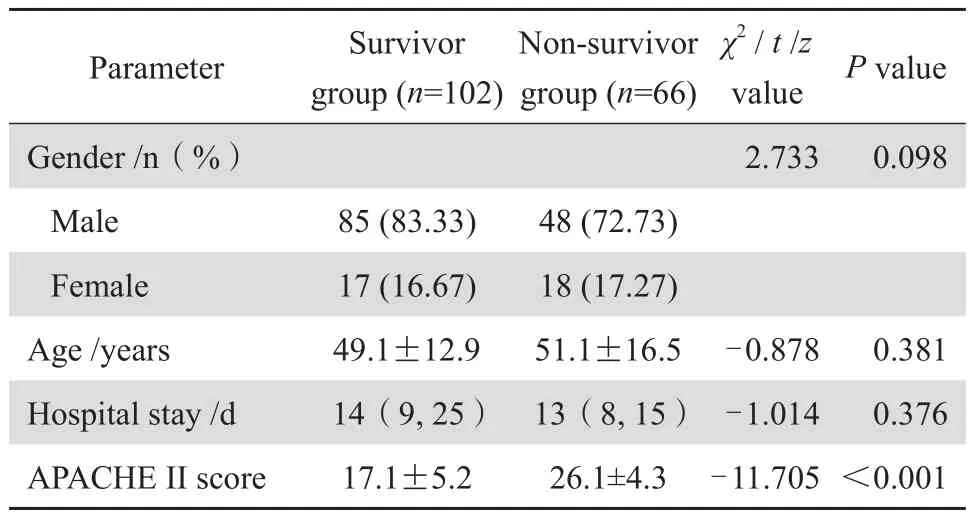
表1 患者一般情况Table 1 General situation of the patients
2.3 基础疾病
基础疾病中,死亡组患有COPD 44例,生存组56例,P<0.05;高血压疾病死亡组63例,生存组69例,P<0.05;慢性肝脏疾病死亡组34例,生存组30例,P<0.05;肿瘤死亡组21例,生存组18例,P<0.05,以上基础疾病生存组与死亡组相比差异均有统计学意义。冠状动脉粥样硬化性心脏病、慢性肾功能不全、糖尿病和脑中风,生存组与死亡组相比差异无统计学意义。见表3。将患者合并症进行分层分析,发现合并症个数两组间差异无统计学意义(χ2=4.655,P=0.199)。见表4。

表2 患者感染部位Table 2 Site of infection in patients with sepsis or septic shock in terms of survival[n (%) ]

表3 患者基础疾病情况Table 3 Basic information of the patients with sepsis or septic shock in terms of survival

表4 患者合并症分层情况Table 4 Complications in the patients with sepsis or septic shock in terms of survival[n (%) ]
2.4 实验室检查
生存组和死亡组患者刚入住ICU及治疗36 h内,C反应蛋白、白细胞计数、氧合指数、血乳酸、血肌酐、血小板计数,两组间差异无统计学意义。而治疗37~48 h后死亡组C反应蛋白水平显著高于生存组(P<0.05),其他化验指标两组间差异无统计学意义。见表5。
2.5 多因素logistic回归分析
进一步评估重度脓毒症和脓毒性休克患者最终结局的相关性,基础疾病中COPD(OR:18.75,95%CI:2.57~157.34,P=0.037)、肿瘤(OR:11.09,95%CI:1.79~66.24,P=0.007)、高血压(OR:5.54,95%CI:2.57~7.56,P=0.048)、慢性肝脏疾病(OR:14.32,95%CI:1.78~16.76,P=0.038),治疗37~48 h后高C反应蛋白水平(OR:1.37,95%CI:1.00~1.74,P=0.046),高APACHE Ⅱ评分(OR:1.27,95%CI:1.13~1.49,P<0.001),均为患者死亡的独立高危因素。见表6。
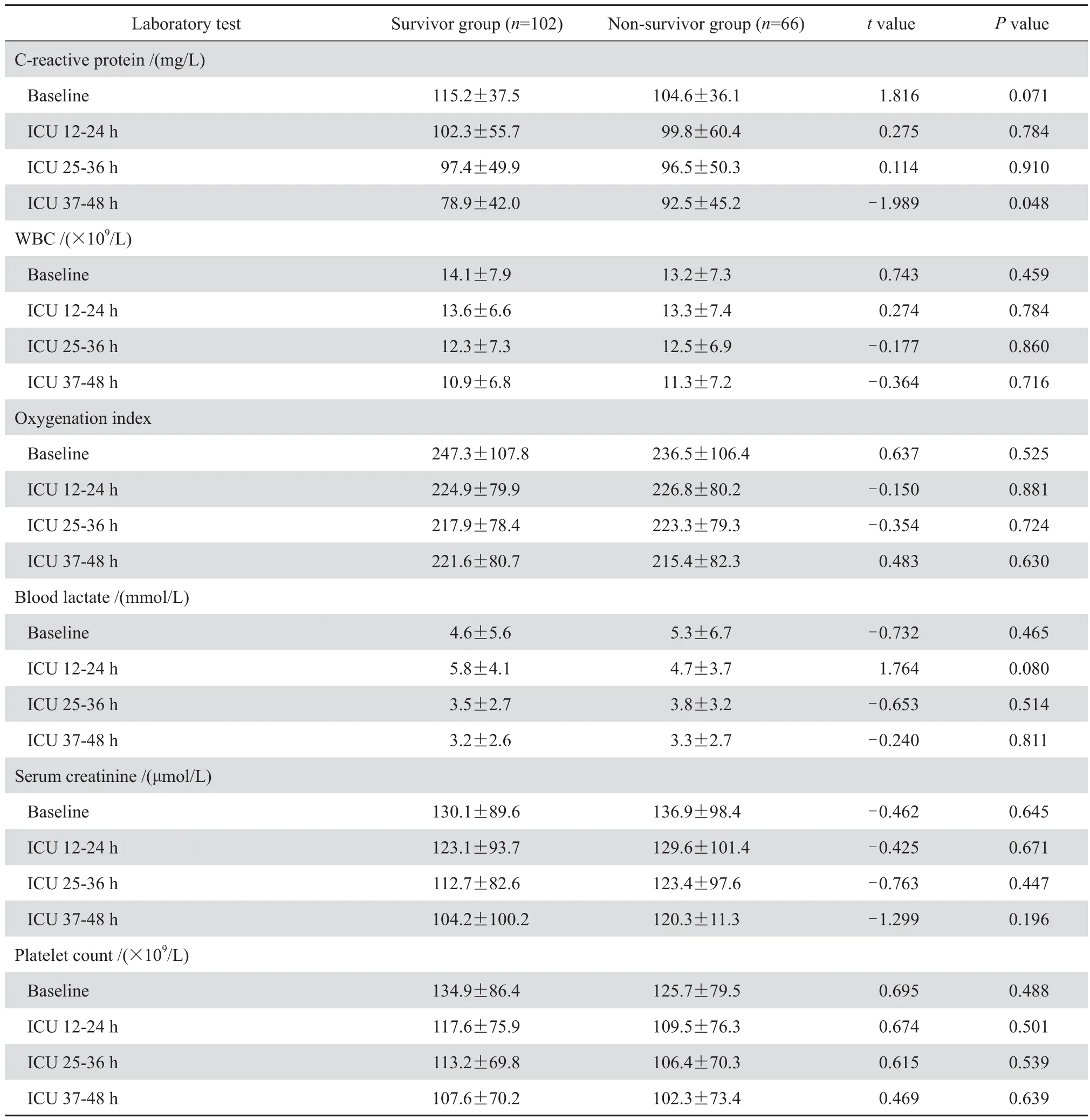
表5 患者实验室检查指标Table 5 Laboratory tests in the patients with sepsis or septic shock in terms of survival
3 讨论
脓毒症是由感染引起的全身炎性反应综合征,可发展为严重脓毒症和脓毒性休克。严重脓毒症和脓毒性休克是重症医学面临的重要临床问题,随着人口的老龄化、肿瘤发病率上升以及侵袭性医疗手段的增加,脓毒症的发病率在不断上升,全球每年新增数百万脓毒症患者,其中超过1/4 的患者死亡[7]。脓毒症不仅发病率和病死率高,其对患者出院后的生活质量亦有不同程度的影响。
本研究共收集168例脓毒性休克患者,对生存组与死亡组进行分析,在性别、年龄和住院时间上两组无明显差异。老年人免疫功能下降是老年严重脓毒症和感染性休克患者病死率增加的重要原因之一[8]。

表6 重度脓毒症/脓毒性休克患者死亡结局相关性多因素回归分析Table 6 Multivariate regression analysis of predictors for fatal outcomes in patients with severe sepsis or septic shock
APACHE Ⅱ评分系统是目前临床上ICU应用最广泛、最具权威的危重病病情评价系统。两组患者相比,死亡组入院时的APACHE Ⅱ评分更高,差异具有统计学意义(P<0.05)。在重症监护领域,APACHE Ⅱ评分、简化急性生理学评分(SAPS II )和SOFA三种评分均可对脓毒性休克患者的预后进行评估[9-12]。本研究说明APACHE Ⅱ评分在评估脓毒症和脓毒性休克患者的预后方面具有重要价值。 然而,每个评分系统都有不同程度的缺陷,影响其在临床工作中的应用。APACHE Ⅱ评分的缺点是评分系统有许多项目,临床数据的收集很麻烦。 SAPS Ⅱ评分预测病死率高于实际病死率,且准确率相对较差。 回顾性研究表明,护理人员在实际临床实践中计算的SAPS Ⅱ评分的准确性不高[13]。而 SOFA 评分的缺点在于无死亡危险度的预测。
COPD会对全身多器官系统造成损害,一旦发生感染性休克,预后通常很差[14];本研究基础疾病中,COPD死亡组44例(66.67%),生存组56例(54.90%),差异有统计学意义(P<0.05)。慢性肝病患者的免疫力低于正常人,易于继发感染,同时,这些患者的肝储备功能低下,休克期间肝功能容易恶化,肝功能衰竭、肝肾综合征、肝肺综合征、肾综合征、多脏器功能衰竭等肝脏并发症迅速出现[15-16];慢性肝脏疾病死亡组34例(51.52%),生存组30例(29.41%),差异有统计学意义(P<0.05)。广泛化疗、放疗、免疫抑制和其他治疗的肿瘤患者易患败血症甚至感染性休克;肿瘤患者的全身营养状况较差,易患恶病质,感染的机会显著高于无肿瘤患者,并且疾病的严重程度更重,死亡率高[17-20];肿瘤死亡组21例(31.82%),生存组18例(17.65%),差异有统计学意义(P<0.05)。高血压疾病死亡组63例(95.45%),生存组69例(67.65%),生存组与死亡组相比差异具有统计学意义(P<0.05)。其他疾病,如糖尿病、冠心病、慢性肾功能不全等,也可引起全身多器官损害,这可能增加脓毒症的发病率和病死率。本研究中冠状动脉粥样硬化性心脏病、慢性肾功能不全、糖尿病、脑中风,生存组与死亡组相比差异无统计学意义。将患者合并症进行分层分析,发现合并症数两组间无明显差异。
为进一步评估重度脓毒症、脓毒性休克研究对象最终结局的相关性,以患者死亡作为结局二分类多因素logistic回归分析,根据大量的文献报道及临床经验,研究患者人口学资料、患者来源、有无手术史、脓毒症分型、入住ICU时有无机械通气、基础疾病、感染部位等可能混杂因素[20]。多因素回归分析显示,基础疾病中COPD、肿瘤、高血压、慢性肝脏疾病,以及治疗37~48 h后高C反应蛋白水平,高APACHE Ⅱ评分是患者死亡的独立高危因素。
本研究针对脓毒症、脓毒性休克患者出院后的长期预后进行回顾性调查,为临床医师提供更多客观的评估依据,同时改善脓毒性休克患者的预后,提升患者院外生活质量。

