电解制备焦磷酸锰(Ⅲ)盐工艺条件及动力学研究
刘思浩,陈金芳,王 岩
(武汉工程大学化工与制药学院,绿色化工过程教育部重点实验室,湖北武汉430073)
可溶性三价锰盐属于较新的化合物,其应用比较广泛。三价锰盐可以在化学发光中应用,与四价锰盐和七价锰盐相比更具有潜力,已用于有机物和无机物的检测[1-2]。三价锰还可以应用于有机合成,作为自由基反应的引发剂效果很好[3-7]。三价锰盐应用于电化学,Mn3+/Mn2+和Mn4+/Mn3+电对具有较高的电位。此前已有把Mn3+/Mn2+作为电对的研究,多是与其他元素的电对,会形成膜的交叉污染。如果研究全锰的液流电池可以改善这个问题[8-12]。
三价锰离子的水溶液在弱酸性条件下不稳定,容易发生歧化反应[13],反应式为2Mn3++3H2O=Mn2++MnO(OH)2+4H+。因此,提出了提高酸度以及配合物等方法来改善其稳定性[14-15]。制备可溶性三价锰盐的方法有以下几种[16]:1)通过高锰酸钾来氧化二价锰盐获取可溶性三价锰盐,此方法获取三价锰的浓度不高,而且引入了其他阳离子[17];2)利用二氧化锰与硫酸锰来制备可溶性三价锰盐,此方法反应速度慢[18];3)利用加热硫酸锰和硫酸的溶液来制备三价锰溶液,此方法危害性较大,会产生发烟硫酸[19];4)电解二价锰的酸式盐溶液制备可溶性三价锰盐,此方法制备速率快,也不会引入其他阳离子[17,20]。 文献中提到电解制备三价锰的浓度仍不够高,但可以通过修改工艺条件及改变介质等来获取浓度更高而且更加稳定的可溶性三价锰。
Mn(Ⅱ)/Mn(Ⅲ)电极电位在硫酸介质(1.5 V左右)中明显高于焦磷酸介质(1.2 V左右)中,因此Mn(Ⅱ)在焦磷酸介质下较易被氧化[21]。在此前大多数文献中,电解制备可溶性三价锰均采用硫酸作为介质。笔者首次采取焦磷酸作为介质,焦磷酸作为络合剂的络合性能更强,对电极的腐蚀性更小。可溶性三价锰水溶液研究较多,但是没有提及如何从溶液中获得可溶性三价锰盐的固体产物,因此获取可溶性三价锰盐固体产品的方法有待提出。
1 实验部分
1.1 原料和仪器
原料:磷酸二氢锰(纯度为99.5%)、磷酸(纯度为85%)、N-苯基邻氨基苯甲酸(纯度为99.5%)、硫酸亚铁铵、重铬酸钾(纯度为99.8%)、乙醇、丙酮,均为分析纯。
仪器:AL204电子天平,78-1型磁力搅拌器,HH-1恒温水浴锅,KQ-100VDB型双频数控超声波清洗器,UV1900紫外可见分光光度计(UV-Vis),DDS-307A型电导率仪,1502AD直流电源,CHI600A电化学工作站,X′Pert PRO MPD型X射线衍射仪(XRD),TM3030 型扫描电子显微镜(SEM)。
1.2 实验方法
1.2.1 电解槽及电极板的制作
可溶性三价锰盐电解装置包括电解槽、阴极、阳极、离子交换膜和直流电源。自制电解槽(13.5cm×10.2 cm×11.8 cm)和石墨板(100 mm×50 mm×5 mm)。每次电解前将石墨板用丙酮浸泡超声10 min,再用乙醇浸泡超声10 min,最后在浓磷酸中浸泡6 h。电极反应如下:

1.2.2 考察焦磷酸浓度对可溶性三价锰浓度的影响
采取有离子交换膜的电解槽电解,恒定电流为0.3 A、电解时间为6 h、温度为0℃。在不同焦磷酸浓度(2~4 mol/L)、相同磷酸二氢锰浓度(0.3 mol/L)下电解,每间隔1 h记录可溶性三价锰的浓度。电解现象大致为阳极板冒出紫红色物质。三价锰浓度由硫酸亚铁铵溶液(每次滴定之前用重铬酸钾标定)滴定得出,以N-苯基邻氨基苯甲酸作为指示剂。
1.2.3 考察磷酸二氢锰浓度对可溶性三价锰浓度和电流效率的影响
采取有离子交换膜的电解槽电解,恒定电流为0.5A、电解时间为6h、温度为10℃。在不同磷酸二氢锰浓度(0.1~0.4 mol/L)、相同焦磷酸浓度(3 mol/L)下电解,每间隔1 h记录可溶性三价锰的浓度及电流效率。 电流效率可用式(1)计算[22]:

式中:n为转移电子数;F为法拉第常数;V为阳极室有效体积;c为电解制备的可溶性三价锰浓度;J为电流密度;A为电极有效面积;t为电解时间。
1.2.4 考察电流密度及时间对可溶性三价锰浓度和电流效率的影响
在相同的石墨电极板、电源型号以及相同的电解液浓度(0.3 mol/L磷酸二氢锰+3 mol/L焦磷酸)下,以不同的电流密度电解8 h,观察在不同的电流密度下电解液的浓度和电流效率。利用相同的直流电源,分别设定电流为 0.1、0.2、0.3、0.4、0.5、0.6、0.7 A,对应的电流密度分别为 2.174、4.348、6.522、8.696、10.87、13.04、15.22 mA/cm2,在 10 ℃水浴下开始电解,每间隔1 h测试电解液的浓度直至反应结束,记录电解1~8 h电解液的浓度和电流效率。
1.2.5 考察电解温度对可溶性三价锰浓度的影响
在其他条件均保持不变的情况下,改变电解池的水浴温度(0~40℃),观察电解现象及可溶性三价锰的浓度变化。
1.2.6 电解过程的动力学研究
采用三电极体系,6 mm直径石墨棒作为工作电极,Hg/Hg2SO4作为参比电极,铂丝作为对电极。在扫速为10 mV/s、扫描电压范围为0.2~1.0 V条件下,对2~4 mol/L的焦磷酸电解液(磷酸二氢锰浓度为0.3mol/L)进行循环伏安(CV)特性曲线测试;在扫描电压范围为0.2~1.0 V、电解液为0.3 mol/L磷酸二氢锰+3 mol/L 焦磷酸条件下,改变扫速(5~25 mV/s)进行CV特性曲线测试。
2 结果与讨论
2.1 XRD和UV-Vis分析
在磷酸介质中电解制备可溶性三价锰时,Mn3+易与磷酸根形成MnPO4,此物质溶解度很低,容易导致阳极电解液形成浑浊液。图1为灰绿色沉淀物质XRD谱图,与磷酸锰标准物质XRD谱图吻合。让磷酸脱水变为焦磷酸后其配合能力会大大增加,实验也证明在焦磷酸介质下电解,阳极液超过5 h也不会变浑浊。在强酸介质中,可溶性三价锰以[Mn(P2O7)3]9-的形式存在。 在焦磷酸介质中电解制备可溶性三价锰所得阳极电解液稀释20倍,用紫外可见分光光度计进行检测,吸收峰出现在500 nm附近,Mn2+在扫描波长范围内不能被观察到,所以溶液含有三价锰离子。
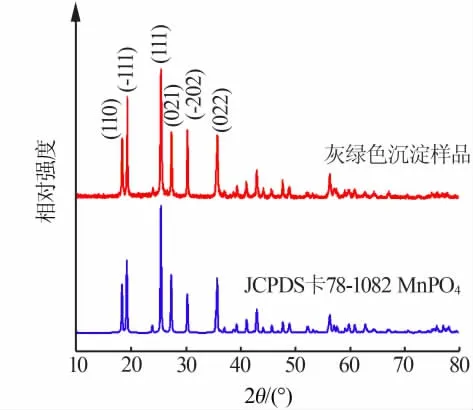
图1 在磷酸介质中电解制备可溶性三价锰所得灰绿色沉淀XRD谱图
2.2 焦磷酸浓度对可溶性三价锰浓度的影响
图2为不同焦磷酸浓度下制备可溶性三价锰的浓度。从图2看出,焦磷酸浓度小于3 mol/L时,三价锰浓度随着焦磷酸浓度的增加而增加。石墨电极的钝化层会降低三价锰的产率,但是在一定的酸度条件下也会导致电极的有效溶解。图3为石墨电极在不同酸度条件下的SEM照片。由图3b看出,在3 mol/L焦磷酸介质电解后的石墨电极表面钝化层被腐蚀,而且凸起部分增加了比表面积,说明此过程产生了有效溶解。但是,焦磷酸浓度超过3 mol/L以后,电解制备的三价锰浓度出现明显下降。主要是因为焦磷酸浓度过高后,溶液黏度增加以及电极的恶性溶解,影响了离子在溶液中的扩散,导致电流效率下降。由图3c观察到,在4 mol/L焦磷酸介质电解后的石墨电极出现了过量腐蚀,表面粗糙且孔径大(可能由腐蚀产生的CO2等气体导致),与原始电极相比发生了巨大变化,附着点明显下降,说明此过程为恶性腐蚀。在3 mol/L焦磷酸介质制备的可溶性三价锰比较稳定,冷藏1 d后三价锰浓度仍保持在97%,常温保存1 d后三价锰浓度也保持在95%。

图2 不同焦磷酸浓度下制备可溶性三价锰的浓度

图3 石墨电极在不同酸度下的SEM照片
2.3 磷酸二氢锰浓度对可溶性三价锰浓度和电流效率的影响
在固定焦磷酸浓度3 mol/L条件下,改变磷酸二氢锰的浓度(0.1~0.4 mol/L),考察其对三价锰浓度及电解过程电流效率的影响。实验结果表明,随着磷酸二氢锰浓度增加,三价锰浓度以及电解过程的电流效率都在增加而且增幅较大。这归因于增加了锰源,同时Mn2+浓度的增加抑制了Mn3+的歧化反应。通过多次实验发现,当磷酸二氢锰浓度超过0.4 mol/L时,电解时间不到1 h,阳极就开始产生四价锰,溶液开始变浑浊。
2.4 电流密度及时间对可溶性三价锰浓度和电流效率的影响
改变电解过程中的电流(0.1~0.7 A),考察电流密度对三价锰浓度和电流效率的影响,结果见图4。由图4a看出,三价锰浓度随着电流密度的增加而增加,而且增加的幅度较大。但是,当电流高于0.5 A后,三价锰的浓度出现了波动。这可能是由于电流密度过高导致了三价锰的过氧化,较高的电流密度会使得电解池的温度升高及辐射热增加,从而加剧了Mn3+的歧化分解。实验观察到电流密度较大时,阳极电解液会出现大量黑色粉末。图5为黑色粉末XRD谱图,可以确认此黑色粉末就是α-MnO2[23]。 因此认为,大量的过氧化导致溶液出现较多四价锰(电流在0.7 A下电解7 h后就会出现类似现象,在0.8 A下不到0.5 h就会出现类似现象),也会附着在电极和离子交换膜上影响效率。
由图4b看出,在电流为0.1~0.2 A时电流效率最高。但是随着电流继续增加,并没有出现电流效率一直下降。在电解电流为0.5 A时出现了新的电流效率峰值,这归因于过高的电流并没有带来较高的三价锰产率,而且低的电流相应的三价锰的产率又过低。综合三价锰的产量和电流效率,最佳的电流应为 0.4~0.6 A。

图4 不同电流密度下制备可溶性三价锰的浓度(a)和电流效率(b)

图5 电流密度较大时阳极电解液出现的黑色粉末XRD谱图
2.5 电解温度对可溶性三价锰浓度的影响
固定焦磷酸浓度为3 mol/L(由相应的6 mol/L磷酸所需的浓磷酸制备)、磷酸二氢锰浓度为0.3 mol/L,考察不同温度下制备可溶性三价锰的浓度,结果见表1。由表1看出,随着电解温度的升高,三价锰的浓度大幅度降低。高温有利于Mn3+的歧化反应(歧化反应多为吸热反应),一定程度上抑制了三价锰的产生。当温度过高时,电解液在不到0.5 h就开始变浑浊。所以磷酸介质下的三价锰最好冷冻保存,主要是因为歧化反应为吸热反应,温度升高促进歧化分解。
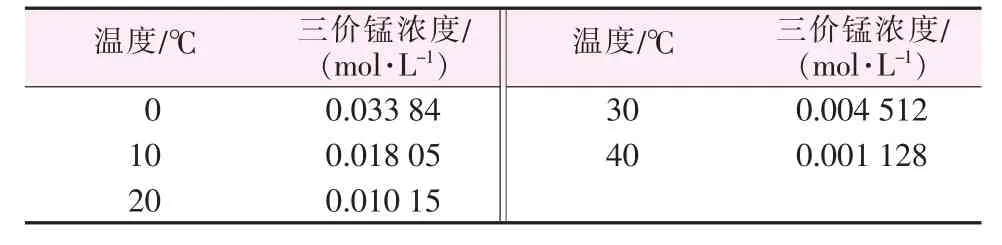
表1 不同温度下电解4 h制备可溶性三价锰的浓度
2.6 电解过程的动力学研究
图6为不同焦磷酸浓度下和不同扫描速率下的CV曲线。由图6a看出,每个CV图都有一个氧化峰和两个还原峰,在氧化峰之前,主要的电极反应为Mn2+氧化为Mn3+(测试中这段过程电极附近溶液变为紫色,正是三价锰的状态),越过氧化峰后面的电流又开始进一步增加,归因于Mn3+被进一步氧化为更高价态的四价锰(在这段电压过程中明显观察到电极附近液体由紫色逐渐变为浑浊灰白色)。负向扫描出现很明显的两个还原峰,说明焦磷酸介质下电解极易产生大量四价锰,也说明四价锰较易被还原。第一个还原峰(Mn3+还原为Mn2+)往负向移动,第二个还原峰(高价态还原为Mn3+)往正向移动。因此可归结为:在低焦磷酸浓度范围内,适度提高焦磷酸浓度更有利于抑制歧化反应,改善电解三价锰过程中氧化还原反应的可逆性;而过高的焦磷酸浓度作用则并不显著。

图6 不同焦磷酸浓度下的CV曲线(a)、不同扫描速率下的CV曲线(b)
通过图6b不同扫速下共轭的氧化还原峰电压,确定Mn(Ⅲ)/Mn(Ⅱ)在3 mol/L焦磷酸介质下的条件电极电位E0,公式如下:
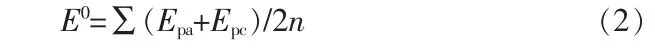
式中:Epa、Epc分别为不同扫速下氧化和还原的峰电压;n为扫描速率的种类。计算得到0.3 mol/L磷酸二氢锰+3 mol/L焦磷酸在静置的石墨棒上的条件电极电位为0.657 V,即1.315 V vs.NHE。
把图6b中的重要参数归入表2。由CV图中可以看出明显的氧化峰和还原峰,可以认为这个过程为可逆,过程肯定不是完全不可逆过程;但是氧化峰和还原峰之间电压差远大于59 mV,而且电压差随着扫描速率的增加而增加,这个过程又为不可逆,故认为此过程为准可逆体系。可以认为不同扫速下的峰电流和扫描速率的1/2次方存在下面的关系,根据拟合的曲线斜率可求出二价锰离子在本体系中的扩散系数D,拟合的直线方程如下式,根据斜率求出Mn2+在焦磷酸介质中的扩散系数为8.347×10-6cm2/s。

式中:n为电子转移数;F为法拉第常数;A为电极面积;R为常数,8.314 J/(mol·K);T为温度;D为扩散系数;c0为Mn2+初始浓度;v为扫描速率;α为电子转移系数;Ep/2为半峰电压。
通过ΔEp与ψ的关系可得出准可逆过程的参数ψ,再通过公式大致估算准可逆区电子转移标准速率常数к0,公式如下:
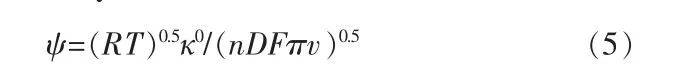
通常准可逆反应的电子转移标准速率常数均在0.3v0.5≥к0≥2×10-5v0.5范围, 计算得到的数值也均在此范围,进一步说明此过程为准可逆过程。
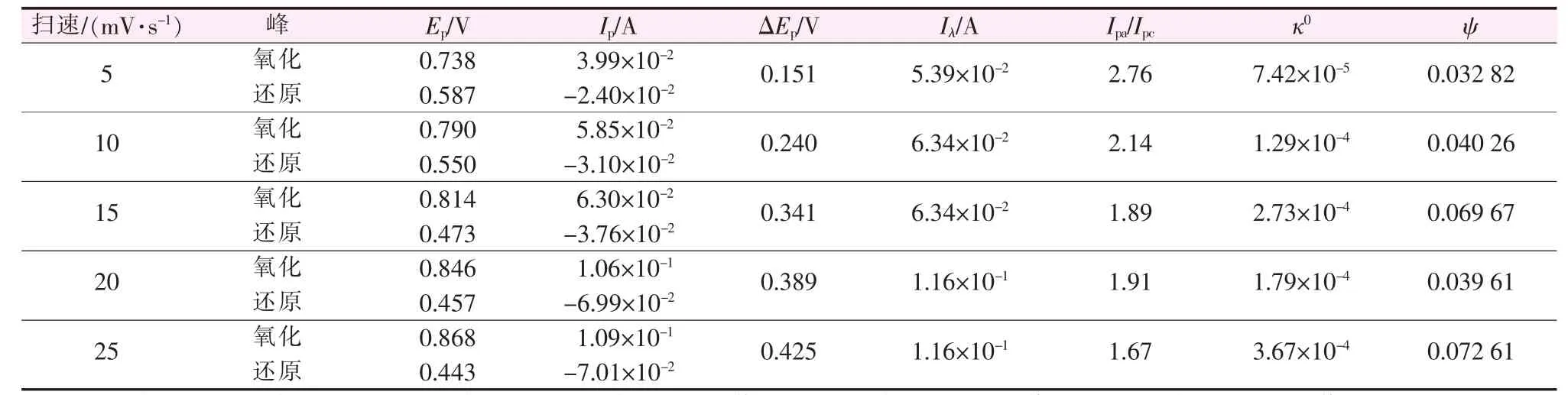
表2 不同扫描速率下CV图中的重要参数
3 结论
在焦磷酸介质中制备可溶性三价锰,主要利用焦磷酸的络合能力来稳定Mn3+。对电解制备Mn3+的工艺条件进行了优化,通过一系列单因素条件实验选择出最佳的电解反应条件。在不同酸度下,电解液对电极的腐蚀以及可溶性三价锰在液体中的浓度和稳定性均不同,综合考虑选取了最佳的焦磷酸浓度。在不同电流密度下,分析了可溶性三价锰的浓度、电流密度及副产物,较大的电流密度会导致过度氧化,应选取最佳的电流密度。在电流密度为10.87 mA/cm2、温度为0℃、电解液为0.3 mol/L磷酸二氢锰+3 mol/L焦磷酸条件下,得到三价锰离子产量最大,电解过程的电流效率也极高。
通过对电解液进行电化学测试及计算,得出0.3 mol/L磷酸二氢锰+3 mol/L焦磷酸在静置的石墨棒上的条件电极电位为1.315 V,且判断出此过程为准可逆过程。同时也计算出电解过程中阳极电子转移系数为0.2950,Mn2+在此过程的扩散系数为8.347×10-6cm2/s。

