水热离子交换时间对铯离子改型白榴石的影响
周振君,张 皓,罗伟华,许培俊,丛培良
(长安大学材料科学与工程学院,陕西西安710064)
利用烤瓷附熔技术制备用于牙齿修复的复合材料,由于结合了金属材料的高韧性和无机非金属材料优良的美学特点,一经问世就在临床上被广泛应用[1]。为避免在冷却过程中瓷体与金属材料之间的界面产生大的应力而降低界面的结合强度,最好把两种材料热膨胀系数差控制在(0.5~1.5)×10-6K-1[2]。然而,通常烤瓷材料的热膨胀系数比金属材料小很多,人们把高膨胀系数的白榴石引入烤瓷材料中,有效地提高了整个瓷体的热膨胀系数[3-4]。由于金属材料的品种和成分的多样性,要求用不同膨胀系数的白榴石来调控瓷体的膨胀系数与之匹配。因此,通过恰当的技术路线和工艺参数来调控白榴石的组成,进而调控其膨胀性能成为急需探究的课题。
鉴于铯榴石(CsAlSi2O6)与白榴石(KAlSi2O6)在化学组成和晶体结构上的相似性和两者膨胀系数的巨大差别[5-6],笔者利用水热离子交换法用铯离子对白榴石粉体进行改型,同时探讨了离子交换过程中铯榴石的生长动力学。
1 实验部分
1.1 样品制备
将熔盐法合成的白榴石粉体[7]按照1∶10的固液质量体积比(g/mL)倒入0.3 mol/L的硫酸铯(Cs2SO4)溶液中,机械搅拌20 min得到悬浮液。将悬浮液装入内衬聚四氟乙烯的高压反应釜中,填充率为70%。将密封的反应釜在180℃下保温不同的时间进行水热离子交换处理。待反应完成并冷却至室温后,取出悬浮液,经过离心分离和反复洗涤得到样品。
1.2 样品测试与表征
采用D8 ADVANCE型X射线衍射仪对样品的物相进行分析。采用S-4800场发射扫描电子显微镜对样品的形貌进行观察。
2 结果与讨论
2.1 XRD分析
图1为不同水热离子交换时间得到样品的XRD谱图。 由图 1 看出,在 180 ℃下保温 2、4、6、8、10、20h的样品均出现铯榴石衍射峰,但是铯榴石衍射峰随着保温时间的增加变得更加尖锐,说明在保温过程中除了有铯榴石不断生成,还存在铯榴石结晶度趋于完整的过程。

图1 不同离子交换时间所得样品XRD谱图
2.2 SEM表征
白榴石和铯榴石均为架状硅铝酸盐类矿物。然而,室温下白榴石为四方晶系而铯榴石为立方晶系[8-9]。由于熔盐法制备的白榴石具有优良的结晶度并且晶粒呈柱状[10],而铯榴石晶粒形貌为立方体,因此可以从晶体形貌变化上判断从白榴石向铯榴石的变化过程。
图2为不同离子交换时间所得样品SEM照片。对于2 h离子交换的试样,虽然从XRD谱图上可以看到铯榴石的衍射峰,但是衍射峰宽化,说明铯榴石晶体还没有充分发育,因此观察到的晶粒形状仍为柱状(见图2a)。随着离子交换时间的增加,柱状晶体的长径比逐渐减小(见图2b和图2c),至8 h时表面已经被立方形状的晶体完全覆盖。再进一步增加离子交换时间,由于铯榴石充分发育导致内应力增大,一旦超过晶相间结合强度,就会发生表面剥离现象。从图2 d看到,经过20 h离子交换的试样表面已经有表面剥离,露出柱状晶体的次表面。因此离子交换时间应该控制在10 h以内。

图2 不同离子交换时间所得样品SEM照片
2.3 离子交换时间对表面离子交换量的影响
图3为水热离子交换反应6 h所得样品表面能谱图(EDS)。借助元素特征能量分析结果,可以发现能谱图存在明显的Cs元素特征峰,说明水热介质溶液中的Cs+与白榴石中的K+进行了有效置换。
通过 EDS 分析得到n(Cs+)/n(K+)。不同水热离子交换时间所得样品表面n(Cs+)/n(K+)见图 4。 由图 4看出,随着反应时间延长,Cs+-K+交换量呈现整体上升趋势。单位时间内交换量曲线的斜率变化,可以反映不同阶段Cs+-K+交换率的大小。

图3 离子交换6 h所得样品EDS图

图4 离子交换时间与Cs+-K+交换量的关系
在本次实验离子交换时间范围内,Cs+-K+交换率的变化可分为两个阶段:当离子交换时间<8 h时,离子交换反应速率很快;当离子交换时间≥8 h后,离子交换速率明显变缓。结合前述对反应产物微观形貌的分析来看,离子交换首先发生在溶液与白榴石晶体接触的表面,在离子交换前期(<8 h),表面K+含量较高,Cs+-K+交换速率受离子扩散速率控制,离子交换速率保持在较高水平。交换时间进一步延长(≥8 h),白榴石表面生成的铯榴石增多,表面K+浓度大幅下降,Cs+-K+交换需要Cs+以扩散作用通过表面包裹层才能实现,因而反应后期离子交换率明显较前期要低。
2.4 铯榴石生长动力学分析
为准确把握铯榴石相在水热交换过程中的生长特性,需要对整个体系进行生长动力学分析。人们已经对不同种类和结构的晶体构建了动力学模型并进行了大量的计算和研究,不同晶体在水热反应过程中的生长规律已被部分掌握[11-12]。由于水热法制备晶体的结晶过程受不同机制的影响,因此采用的生长动力学理论模型也不尽相同。基于本次研究采用水热离子交换法,其整体反应过程更接近于水热法原位结晶机制,故预借助此机制下的生长动力学模型,开展对铯榴石动力学的分析[13]。模型核心基础由Johnson-Mehl-Avrami方程给出,其表达式:

对上式两边作对数运算,将其转变成线性形式,则相应的Sharp-Hancock表达式:

式中:αt为样品的晶化率;k为反应速率常数;t为反应时间;n为Avrami指数,不同的n值大小反映了晶体在反应中受不同反应机制控制的情况(一般情况下,n<0.5, 反应受体系扩散过程控制;0.5<n<1.0,产物和反应物界面控制体系反应过程;n>1.0,反应受成核控制);t0为晶化诱导时间。
首先,需要得到目标产物的晶化速率αt,对应的计算公式:

式中:At为反应时间为t时产物衍射峰的峰面积;AMax为产物衍射峰最大峰面积。
根据实验样品的物相测试分析结果 (见图1),在XRD谱图中铯榴石的最强峰为(400),因此选择不同反应时间下铯榴石产物(400)晶面的最大峰面面积作为AMax。通过Jade软件计算出不同离子交换时间样品的晶化速率(见图5)。由图5看出,反应初期(2~6 h)晶化进行得很快,表现在关系图中晶化率曲线的斜率较大;随着反应时间的延长(6~8 h),晶化率曲线的斜率逐渐减小,表明晶化速率正在逐渐减缓;当反应时间超过一定范围时(>8 h),晶化速率减慢至最低并逐渐趋于稳定。
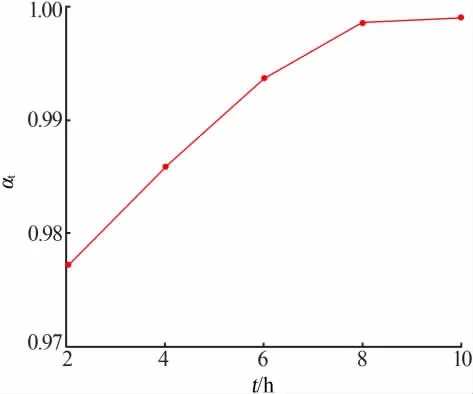
图5 不同离子交换时间所得样品的晶化率
将实验数据代入JMA方程,由于实验中晶化诱导时间极短,故取t0=0,则式(2)表示为:
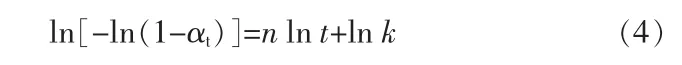
根据上式,以 ln[-ln(1-αt)]为纵坐标,lnt为横坐标作图,图6给出了铯榴石合成的拟合结果。根据拟合分析得到的铯榴石晶化率表达式:

通过对拟合曲线的斜率计算得到Avrami指数n=0.354 0,表明整个水热离子交换反应主要受扩散过程控制;利用拟合曲线的截距得到本次反应速率常数k=2.819 3。
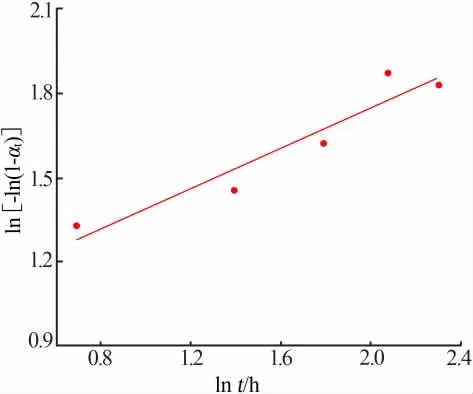
图 6 ln[-ln(1-αt)]与 ln t关系曲线
3 结论
1)利用水热离子交换法在白榴石粉体晶格中引入铯离子,从而实现了对白榴石粉体的改型。2)铯离子交换量随着交换时间的增加而增加,但是在交换时间超过8 h后,离子交换速率却随着交换时间的增加而下降。3)通过控制离子交换时间,在白榴石表面可以得到稳定的立方型铯榴石。4)铯榴石生长动力学分析表明水热离子交换受扩散过程控制。

