不同形貌纳米氧化铁的制备及性能研究
王冬华,付 新
(渭南师范学院化学与材料学院,陕西渭南714099)
氧化铁为应用较为广泛的无机材料,其物理和化学性质不仅与其化学组成有关,还与其尺寸、形貌及分散性有关。纳米氧化铁相比于常规氧化铁又表现出很多独有的特性,如:能大幅度吸收紫外线辐射、具有纳米材料的随角变色效应、对电磁波有强烈的吸引力、对红外线有特殊的反射和吸收性能,以及具有较强的催化功能、透明着色、无毒等特点。由于纳米氧化铁的优异性能,使其在多个领域得到广泛的应用。纳米氧化铁在涂料领域可制得纳米抗老化涂料、金属闪光涂料、电泳涂料和罐头涂料等[1],也被用于制作光吸收材料、磁性材料、催化和吸附材料、生物医学材料等[2]。
采用不同方法可控制备尺寸和形貌不同的纳米氧化铁已成为该领域的一个研究热点。伍媛婷等[3]用硫酸亚铁和柠檬酸为原料,通过溶胶-凝胶法制得粒径为30 nm的氧化铁颗粒;徐锁平等[4]以硝酸铁和尿素为原料,通过超声波辅助的均匀沉淀法,制得纳米纺锤形氧化铁颗粒;Xiao等[5]利用水热法制得粒径约为9 nm的氧化铁纳米颗粒;翟明明等[6]分别用九水合硝酸铁、四水合氯化亚铁、六水合氯化铁以及氢氧化钠为原料,分别通过固相研磨法、化学沉淀法以及均匀沉淀法制备出磁性氧化铁纳米粒子。同时也发现纳米氧化铁有很多不同的形态,比如李杰等[7]用三氯化铁和尿素为原料,以蒸馏水和甘油为反应溶剂,采用水热法制备出粒径分布均匀的α-Fe2O3球形纳米粒子;杜庆波[8]以 FeCl3为铁源,用CTAB和聚乙烯吡咯烷酮(PVP)为表面活性剂,分别制备出棒状和准立方体纳米氧化铁;陆希峰等[9]用水热法制得拥有花状结构的α-Fe2O3。笔者采用水热法,探究了不同溶剂(水和DMF)、不同表面活性剂(SDBS和CTAB)对α-Fe2O3尺寸和形貌的影响,讨论了不同α-Fe2O3的光致发光特性。
1 实验部分
1.1 试剂和仪器
试剂:硝酸铁(分析纯,质量分数≥98.5%),十二烷基苯磺酸钠(分析纯,质量分数≥90.0%),十六烷基三甲基溴化铵(分析纯,质量分数≥90.0%),N,N-二甲基甲酰胺(分析纯,质量分数≥99.5%),无水乙醇(分析纯,质量分数≥99.7%)。
仪器:AL204电子天平;RCT basic磁力搅拌器;DZF-6021真空干燥箱;80-2高速离心机;XRD-6100 X射线衍射仪;SIGMA 500扫描电子显微镜;F-7000荧光光谱仪。
1.2 实验步骤
准确量取30 mL DMF置于烧杯中,用电子天平称取1.212 g(3 mmol)九水合硝酸铁和0.6 g CTAB溶于DMF中。将上述溶液置于磁力搅拌器上持续搅拌,直到硝酸铁和CTAB全部溶解。将烧杯中的溶液倒入50 mL内衬聚四氟乙烯的高压反应釜中,将反应釜密封后放入真空干燥箱中,在160℃加热15 h。反应完毕后关闭真空干燥箱,待反应釜冷却至室温时从干燥箱中取出。把反应后的溶液转移到离心管中,用高速离心机离心分离,离心机转速为1 500 r/min、时间为10 min。原液离心分离后将上层清液倒掉,加入去离子水至离心管刻度,将溶液摇匀,离心机参数保持不变,进行离心洗涤。将离心洗涤后的上层清液倒掉,加入无水乙醇,将溶液摇匀,离心机参数保持不变,再次离心洗涤。将离心洗涤后的上层清液倒掉,将沉淀取出,置于真空干燥箱中,在60℃干燥2 h,得到红棕色粉末,收集存储。保持实验步骤不变,第二组实验试剂变为1.212 g九水合硝酸铁和0.6 g CTAB溶于30 mL水;第三组实验试剂变为1.212 g九水合硝酸铁和0.6 g SDBS溶于30 mL水;第四组实验试剂变为1.212 g九水合硝酸铁和0.6 g SDBS溶于30 mL DMF。制备的样品分别记为1、2、3、4。 4 组实验原料、表面活性剂和溶剂,见表 1。

表1 4组实验原料、表面活性剂和溶剂
2 结果与讨论
2.1 XRD分析
图1为4组样品XRD谱图。由图1看出,样品衍射峰位置与α-Fe2O3的JCPDS标准卡片相对应,8个主要衍射峰对应α-Fe2O3的(012)(104)(110)(113)(204)(116)(214)(300)晶面特征峰,表明制得的样品均为α-Fe2O3。图1中除了α-Fe2O3衍射峰外,无其他杂质相关的衍射峰,表明4个样品中都无明显杂质,纯度较高,结晶性良好。从图1也可以看出,4组样品的X射线衍射峰强度不完全相同,表明不同条件下制得的α-Fe2O3晶粒尺寸有差异。

图1 4组样品XRD谱图
2.2 SEM分析
图2为4组样品SEM照片。比较样品1和样品2,两组实验所用表面活性剂均为CTAB,但样品1所用溶剂为DMF,样品2所用溶剂为水。由图2看出,样品1由颗粒组成,尺寸为40~60 nm,但是颗粒与颗粒紧密结合在一起,界限不分明。这是由于粒子尺寸小,颗粒间的毛细管力、静电引力、范德华力等相互作用力增强,造成团聚现象[10]。样品2也由颗粒组成,尺寸为30~50 nm,分布范围较小,而且分散程度较好。通过分析两组样品SEM照片可知,当表面活性剂为CTAB时,所得样品均为α-Fe2O3纳米颗粒,溶剂采用水比用DMF所得样品的分散性好。
对比样品3和样品4,两组实验都以SDBS为表面活性剂,溶剂分别使用水和DMF。由图2看出,样品3呈颗粒状,尺寸为20~40 nm;样品4形貌比较规则,为清晰的圆饼状,直径为80~120 nm,厚度为3~10 nm,表面不规整。对比两组样品SEM照片发现,以SDBS为表面活性剂时,用水和DMF为溶剂制成的纳米氧化铁的尺寸与形貌大不相同。造成两组样品形貌较大差别的主要原因是采用的溶剂不同。在DMF溶液中,许多离子型反应相对于一般的质子溶剂更容易发生[11]。DMF分子中带正电荷的一端被甲基包围,出现空间阻碍,造成负离子无法靠近,而只缔合正离子,因此更容易形成圆饼状产物。
对比4组样品SEM照片发现,不同的表面活性剂对制备α-Fe2O3有较大的影响。比较样品1与样品4,两组实验所用溶剂都为DMF,表面活性剂分别为CTAB、SDBS。通过对比SEM照片发现,两组样品的形貌和大小大不相同,样品4主要是分散性较好的圆饼状,而样品1为团聚严重的颗粒状。比较样品2和样品3,两组实验所用溶剂都为水,表面活性剂分别为CTAB、SDBS。通过对比SEM照片发现,两组样品的形貌均为颗粒状,而样品3颗粒更小。实验结果表明,表面活性剂对样品的形貌和尺寸产生了一定的影响。CTAB是阳离子表面活性剂,不但能够在合成前期作为模板剂吸附到微晶表面从而在固体表面形成一层保护膜,约束产物一维方向的生长,还能增加产物的分散性,减少团聚现象[12]。而SDBS作为表面活性剂时,疏水烷基链伸向溶剂中,亲水基的磺酸基附着在粉体表面,所以它可以包裹单个的纳米粒子,同样也可以裹住多个粒子[13]。因此,采用CTAB作为表面活性剂制得的样品主要为颗粒状,而采用SDBS作为表面活性剂时,与不同的溶剂作用就可以制得纳米颗粒和纳米圆饼。

图2 4组样品SEM照片
2.3 PL分析
图3为4组纳米氧化铁样品光致发光光谱图。从图3看出,样品1和样品2光致发光光谱图基本相似,均在430 nm处出现强发射峰,造成该现象的主要原因是样品1和样品2均由纳米颗粒组成且粒径相当。样品3在445 nm处出现一个较强的发射峰,相比于样品1和样品2发射峰的中心位置,样品3发射峰的中心位置发生了明显的红移,且发射峰强度远大于样品1和样品2,这可能是由于样品3的颗粒粒径较小导致的。纳米α-Fe2O3吸收光能会产生电子-空穴对,电子-空穴对能够在晶体中不断运动,如果被束缚在发射中心上,电子-空穴复合就引起了发光。样品3纳米颗粒较小,由于纳米颗粒的限域效应,电子-空穴对只能在小体积中运动,引起颗粒内部内应力增加,导致电子波函数重叠加大,使得带隙、能级间距变窄,从而形成了强发射峰并引起了红移。样品4在364 nm处出现强发射峰,相比于样品1、样品2、样品3,该发射峰的中心位置发生了明显的蓝移。一些材料科学家认为纳米材料出现发射峰蓝移的现象主要是由于纳米材料的量子尺寸效应、表面结构的影响等[14-15]。样品4出现明显蓝移主要是因为特殊的圆饼状结构,其厚度只有几纳米,当厚度小于常规材料的激子波尔半径时,就会产生明显的蓝移。除此之外,表面的堆积缺陷也是造成蓝移的一部分原因。
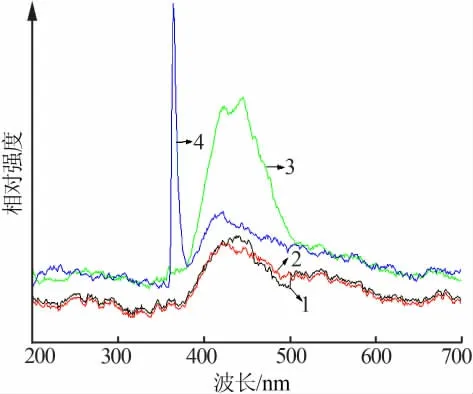
图3 4组样品光致发光光谱图
3 结论
1)利用不同的表面活性剂和溶剂,通过水热法制得了圆饼状和颗粒状纳米α-Fe2O3。2)表面活性剂和溶剂的不同作用是形成不同形貌和不同尺寸纳米α-Fe2O3的主要原因。3)不同形貌和尺寸的纳米α-Fe2O3具有不同的光致发光性能,纳米限域效应导致样品3的强发射峰发生了红移;量子尺寸效应和表面堆积缺陷导致样品4的强发射峰出现了明显蓝移。

