仔猪副伤寒活菌计数参考疫苗保存期试验
王秀丽,张 媛,李红霞,袁 露,李爱玲,曹翠萍,刘 博,辛凌翔,彭国瑞,李 建,蒋玉文
(1.中国兽医药品监察所,北京 海淀100081;2.齐鲁动物保健品有限公司,山东 济南250100;3.辽宁益康生物股份有限公司,辽宁 辽阳111000)
1 材料与方法
1.1 参考疫苗
1.1.1 参考疫苗的制备 按照《中华人民共和国兽用生物制品规程》[5]的方法,制备一批(500 瓶)仔猪副伤寒参考疫苗(20 头份/瓶),置于-70 ℃以下保存,批号:201602,对新制备的参考疫苗候选物进行活菌计数,作为保存期0 个月时每头份参考疫苗的活菌数。
1.1.2 参考疫苗的分发 从500 瓶参考疫苗中随机抽取100 瓶,置于隔热泡沫塑料盒内,并放入生物冰袋,最外层包装为纸箱,由EMS 快递至A 单位、B单位和C 单位,收到样品后立即置于-70 ℃以下冰箱中保存[6]。
1.2 培养基及耗材 普通琼脂培养基,批号:160412,普通肉汤培养基,批号:160412,均购自北京中海生物科技有限公司;1 mL、10 mL 一次性吸管,购自Costar 公司;一次性平皿(直径90 mm),购自青岛金典生化器材公司。A、B、C 三家单位所用的试验耗材完全一致。
1.3 试验方法
1.3.1 运输稳定性试验 B 单位和C 单位分别从100 瓶参考疫苗中随机抽取5 瓶用1.1.2 相同的方式寄到A 单位,A 单位检验员收到样品后马上进行活菌计数,运输过程均需要2 d,分析运输过程对样品稳定性的影响。
1.3.2 均一性试验 随机抽取500 瓶疫苗中的10瓶,由A 单位2 名检验员,按照《中国兽药典》2015年版进行活菌计数,每瓶疫苗加入10 mL 普通肉汤溶解,混匀后取1.0 mL 加入9.0 mL 普通肉汤中稀释,依次稀释至10-7,取0.1 mL 10-7稀释度的菌液滴3 付平板,0.1 mL/付,在普通琼脂上铺均,37 ℃培养24 h,记录每瓶疫苗活菌计数的结果,计算10瓶疫苗计数结果的变异系数。
1.3.3 协作标定 分别随机抽取100 瓶参考疫苗、100 瓶普通琼脂(100 mL/瓶)、100 瓶普通肉汤培养基(200 mL/瓶)以及相关耗材寄给B 单位和C 单位,A、B、C 3 家单位分别随机抽取2 名检验员,每位检验员对3 瓶参考疫苗按照1.3.1 的方法进行活菌计数,每瓶疫苗进行2 次活菌计数的重复性试验,统计不同检验员在不同时间、不同实验室活菌计数的结果[7]。
外高桥保税区一经设立,就是开放度最高、自由贸易的功能性最强的保税区。当时,国务院确定外交桥保税区内:一是实行免关税、免许可证;二是允许外商贸易机构从事转口贸易;三是可为区内外商投资企业代理本企业生产用原材料、零配件进口和产品出口业务;四是区内企业外汇全额留成;五是各国货币流通;六是设立生产资料交易中心;七是对保税区内的主要经营管理人员可办理多次出入境护照,提供出入境方便。
1.3.4 保存期试验 按照协作标定的方法对保存5~18 个月的仔猪副伤寒活菌计数参考疫苗进行活菌计数,剔除每次试验不满意的数值,统计试验结果的中位数、平均数、变异系数,判定参考疫苗在18 个月内菌数的差异。
1.4 结果处理
1.4.1 均一性试验 10 瓶参考疫苗活菌计数结果的变异系数小于10%,说明疫苗瓶间差异不显著,均一性良好。
1.4.2 根据CNAS-GL02:2006 《能力验证结果的统计处理和能力评价指南》[8]中稳健统计方法,测定Z 比分值,用于分析每个计数结果检测结果中所处的位置。 Z 比分值采用X、XM、Norm IQR 来确定[9]。
Z 比分值计算公式:Z=(X-XM)/Norm IQR
式中:Z 为稳健比分值;X 为检验数据;XM 为中位值;Norm IQR 为标准化四分位距,Norm IQR=0.741 3×四分位间距(IQR)。
判定标准为:︱Z︱≤2 为满意结果;2<︱Z︱<3 时,表示结果可疑;︱Z︱≥3 为不满意结果。
1.4.3 出现以下情况之一者,检验结果判为“不满意”,并将检验数据剔除,不参与数据统计:(1)任一平板上菌落数小于40 或大于200;(2)平板上有片状菌落生长;(3)3 付平板间菌落数相差50%以上[10]。
2 结果与分析
2.1 运输稳定性试验 由A 单位2 名检验员对B单位和C 单位分别寄回的5 瓶参考疫苗候选物进行活菌计数,结果显示,2 名检验员对10 瓶参考疫苗计数结果的最大差异为5%,差异不明显,10 瓶参考疫苗计数结果的最小值为3.6×109CFU/头份,本参考疫苗保存期为0 个月的计数结果为3.5×109CFU/头份,结果一致,说明该参考疫苗在2 ℃~10 ℃运输,48 h 内的稳定性良好,具体结果见表1。
2.2 样品的均一性分析 检验员1 计数结果的中位数为4.0×109.0CFU/头份,上四分位数为4.2×109.0CFU/头份,下四分位数为3.6×109.0CFU/头份,标准化四分位居为0.518 9,变异系数8.4%;检验员2 计数结果的中位数为4.05×109.0CFU/头份,上四分位数为4.3×109.0CFU/头份,下四分位数为3.6×109.0CFU/头份,标准化四分位居为0.518 9,变异系数8.2%。检验员1 和检验员2 计数的结果差异在5.3%以内,在活菌计数的误差范围内,︱Z︱均小于2,结果满意,见表2。
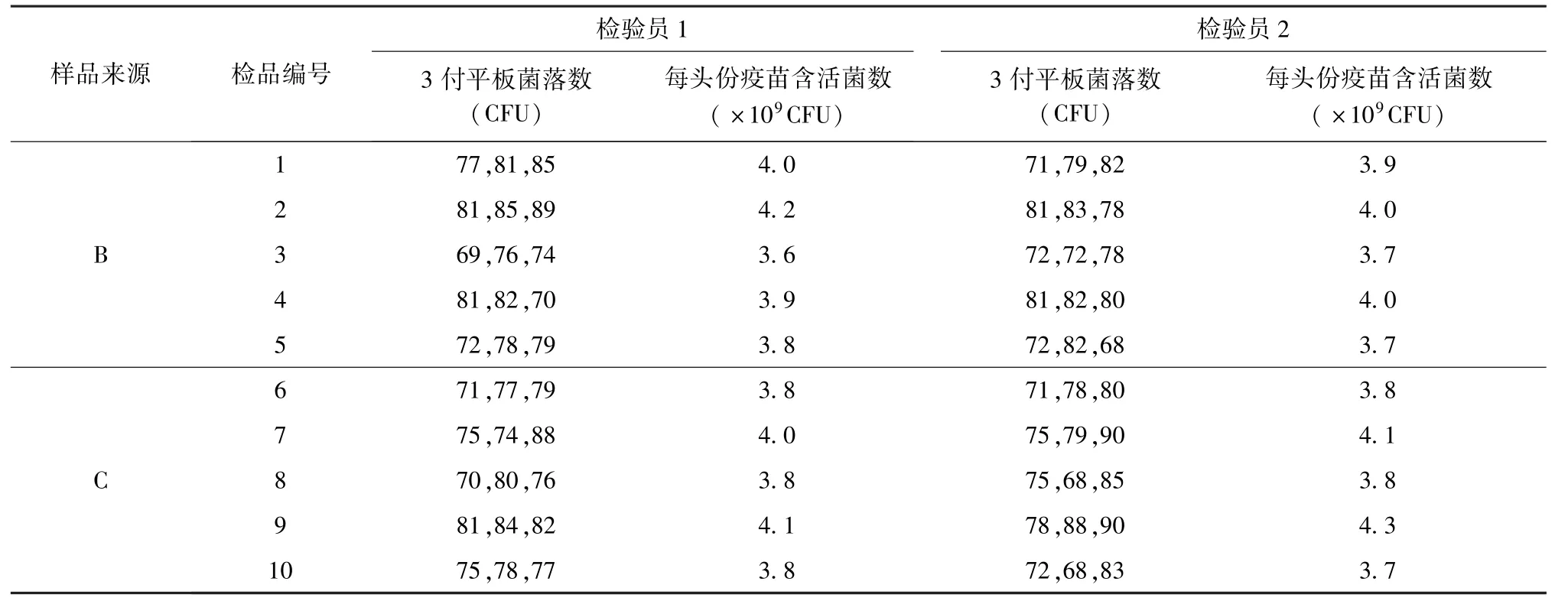
表1 运输稳定性试验结果
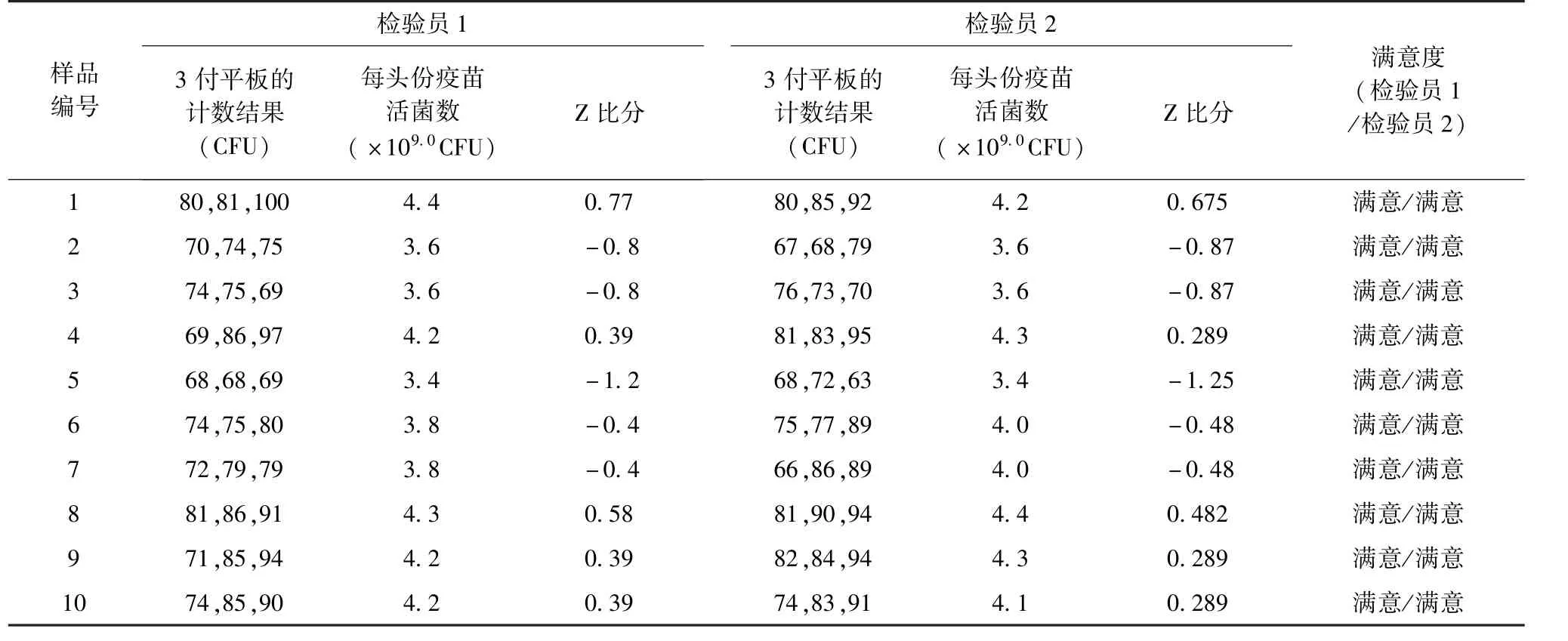
表2 均一性试验结果
2.3 协作标定 A、B、C 3 家单位6 名检验员对18 瓶参考疫苗计数的结果为(×109.0CFU):3.0、3.2、3.2、3.3、3.7、3.8、3.4、3.6、3.6、3.4、3.7、3.8、3.4、3.4、3.8、3.6、3.7、3.5、3.2、3.3、3.4、3.6、3.7、3.6、3.4、3.2、3.6、3.5、4.2、3.9、4.2、4.0、3.5、3.2、3.3、3.3,剔除不满意结果(︱Z︱>2 的数据),对剩余的34 个计数结果进行统计分析,计数结果的平均值为3.5,中位数为3.5,变异系数为6.7%,结果满意,且计数结果的平均数与保存期为0 个月计数结果一致(保存期为0 个月时的计数结果为3.5×109CFU/头份)。
2.4 保存期试验 按照协作标定的方法对-70 ℃以下保存5 ~18 个月的仔猪副伤寒参考疫苗候选物进行活菌计数,剔除结果不满意的偏离数据,变异系数为6.7%~8.9%,均小于10%,平均数为3.4×109~3.7×109CFU/头份,中位数为3.4×109~3.75×109CFU/头份,均在活菌计数可接受的误差范围内,且活菌计数结果在18 月内未随保存时间的延长而降低,结果见表3。
3 讨论与小结
活菌数是直接关系到兽用细菌类活疫苗安全性和免疫效力的重要参数,是疫苗质量的关键之一,在细菌学实验室工作中,可靠的计数结果是准确判断细菌毒力及免疫原性的前提。
运输稳定性试验结果显示,参考疫苗候选物在2 ℃~10 ℃冷藏条件下运输48 h,活菌数未因温度不恒定或者运输过程的条件差异而下降,说明运输稳定性良好。基于此,均一性试验和协作标定及保存期试验才有意义。这也为将来参考疫苗应用过程中样品的发放不会受到运输过程的影响提供数据支撑。
均一性试验结果显示,随机抽取的10 瓶样品计数结果的变异系数小于10%,证明本批次样品的均一性良好。

表3 保存期5~18 个月活菌计数结果统计 (×109CFU/头份)
因活菌计数结果受诸多因素影响,如培养基质量、操作方法、培养条件、稀释液、操作温度、菌液冲击程度、平板湿度等。 在本研究中,仔猪副伤寒(C500 株)参考疫苗候选物为同一批次的样品,培养基和稀释液均由同一单位发放,导致计数结果差异的样品、培养基、稀释液的影响因素不存在,影响因素可能有两方面,一是稀释过程中菌液冲击的程度不一致;二是所使用普通琼脂平板表面的湿度不一致。尽管按照统一的操作规程进行操作,活菌数也有差异,同一检验员对同一份样品进行计数,结果相差10%均在可接受的范围内。在协作标定中,3 家单位的计数结果也有差异,C 单位计数结果相对偏高,这与每家单位的计数操作习惯及实验室环境有关系。这也是参考品和国家/国际标准品需要协作标定的原因,本次协作标定结果满意,且平均数与保存期为0 个月时计数结果一致。
作为活菌计数的参考疫苗,在一定的保存期内活菌数稳定是前提条件,本研究对保存18 个月内的参考疫苗候选物每月均用协作标定的方法计数,结果表明,在18 个月的保存期内,计数结果未随时间的推移而降低,说明参考疫苗在18 个月内活菌数稳定,本研究可以为仔猪副伤寒活菌计数参考疫苗质量标准的制定提供可靠依据。

