经食管超声心动图引导FustarTM可调弯鞘封堵主动脉瓣瓣周漏手术经验总结
王石雄,王小峰,高秉仁,王 炜,王玮璠,马 麒,贺逢孝,薛 羽,柳德斌
瓣周漏是心脏瓣膜置换术后较常见的并发症之一,其发生率约2%~17%[1-2]。因血流动力学的改变,如不及时治疗,常引起心力衰竭、溶血、感染性心内膜炎等并发症。目前瓣周漏常规外科治疗须二次开胸,风险大,出血多,并发症多,且易复发瓣周漏[3-4]。而X线下导管封堵瓣周漏建立路径和操作也存在一定难度。我科在先天性心脏病(先心病)、主动脉瘤破裂外科封堵[5-6]的经验基础上,于2017年1月开展了采用经食管超声心动图(TEE)引导下,FustarTM可调弯鞘建立输送路径,在非X线照射下采用先心病封堵器先后成功封堵主动脉瓣瓣周漏 2例,临床效果满意。
1 资料与方法
1.1 临床基本资料(表1)
2017年1月至12月,我院收住瓣膜置换术后并发瓣周漏、反复心力衰竭患者2例,NYHA心功能分级Ⅲ级,均经彩色多普勒超声心动图确认无误。2例患者均排除急性感染性心内膜炎、结缔组织病等,术前均给予药物调整心功能至NYHA心功能分级II级,术前停用华法林,改用低分子肝素钙,国际标准化比值(INR)<1.5。所有患者及家属术前被告知采用新技术及可能出现的潜在并发症,均签署知情同意书。

表1 2例患者临床基本资料
1.2 手术方法
手术入路(图1):患者取仰卧位,采用静吸复合麻醉,常规穿刺左桡动脉、右颈内静脉测压管,置入TEE探头。取胸骨右缘第2肋间横行切4 cm微创切口,逐层分离进胸,并置入一次性切口保护固定牵开器(AKYQKB-70/70-35/40,见图1),呈 “打孔”入路,显露升主动脉,带垫片2-0 Prolene线于升主动脉处行双荷包缝合,静脉注射肝素1 mg/kg,控制血压,在荷包中央处穿刺置入FustarTM可调弯鞘(图2)入升主动脉。
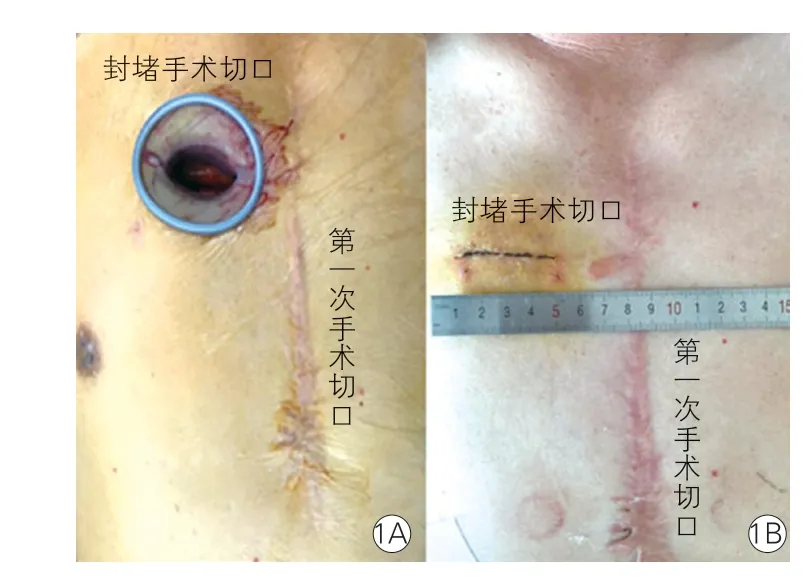
图1 A、B示手术切口入路

图2 FustarTM可调弯鞘
经食管超声心动图检测(图3):在TEE引导下,接近左心室流出道长轴,同时显露左心室流出道、人造主动脉瓣膜及瓣周漏漏口、升主动脉,调整FustarTM可调弯鞘头端对准瓣周漏口,经漏口置入导丝进入左心室,同时跟进FustarTM鞘管进入左心室建立输送路径,TEE再次检查人造瓣膜闭合正常(图3B)。
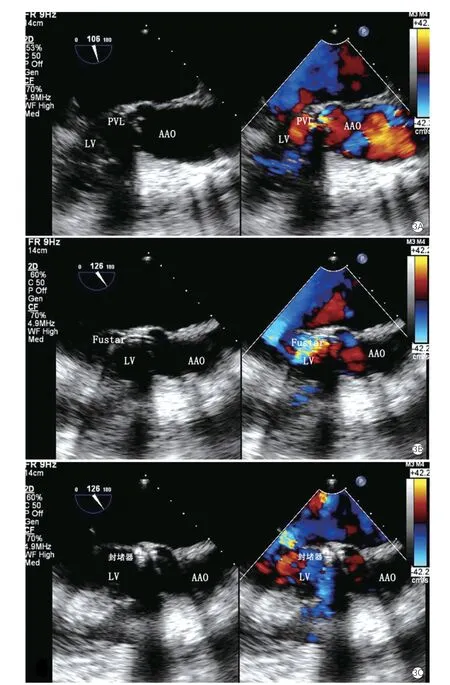
图3 经食管超声心动图检测
选择合适封堵器,装载封堵器,经弯鞘置入封堵器封堵瓣周漏,TEE再次检查人造瓣膜闭合正常,彩色多普勒检测证实瓣周漏反流束完全消失,心电图较术前无变化。反复推拉输送钢缆,判断封堵器镶嵌稳定无移位或脱落,旋转钢缆,释放封堵器,完成操作(图3C)。
2 结果
2例患者均顺利完成手术。封堵完成后即刻舒张压升高约10 mmHg(1 mmHg=0.133 kPa),无残余反流、无卡瓣或瓣膜损伤、无新增心律失常、无封堵器脱落及影响冠状动脉血流等并发症。切-缝皮时间55~70 min,心内操作15~25 min,术中出血量小于100 ml,无输血,未使用体外循环及造影剂,无X线照射。
术后2~6 h拔除气管插管,术后第1天从监护室转至普通病房。术后第3天复查超声心动图,人工瓣膜开闭正常,无残余漏,无封堵器移位,NYHA心功能分级均为Ⅰ级,左心室内径较前明显缩小[(58.5±3.5)mm vs (65.0±4.2)mm,P<0.05]。术后5~7天出院,术后常规口服华法林抗凝。
随访6~16个月,2例患者NYHA心功能分级均为Ⅰ级,均未发生封堵器脱落、无残余漏、无新增心律不齐、无卡瓣以及封堵器相关瓣膜关闭不全。
3 讨论
瓣周漏是心脏瓣膜术后常见的严重并发症之一,据长期随访观察,其在主动脉瓣和二尖瓣瓣位发生率约2%~17%[1-2],环状钙化、感染、既往开胸手术与瓣周漏病史,以及手术缝合技术和人工瓣膜类型是发生瓣周漏的风险因素[7],而赵星等[8]报道的大样本研究表明主动脉瓣瓣周漏发生的主要因素是术前感染性心内膜炎(36.6%)与非特异性血管炎(22.0%)。其中3%的瓣周漏患者因溶血、心力衰竭需要行手术治疗[9]。在有症状的患者中,与保守治疗相比,手术闭合瓣周漏或再次瓣膜置换明显改善患者的生存期[3]。但是再次外科常规手术,都需要二次开胸,难度增大,组织分离困难,易致大血管、心肌损伤,出血量明显增加,视野显露亦困难。另外,体外循环和总手术时间延长,术后炎症反应及其他并发症增多。有学者报道[10],二次手术的死亡率高达10%~22% ,赵星等[8]研究报道了第一次主动脉瓣置换手术合并感染性心内膜炎患者再次出现瓣周漏的死亡率高达20.0%,治疗后随访仍有瓣周漏达38.5%[8],而有研究发现12年生存率小于40%,而其瓣周漏再发率很高[11]。
如何避免采取高风险的常规外科手术治疗方法,1992年,Hourihan等[12]首次报道经导管动脉导管未闭封堵器成功封堵主动脉瓣瓣周漏,随着介入技术的发展,内科介入导管封堵逐渐成为治疗瓣周漏的另一种治疗方法,尤其是瓣周漏高危患者[13-15]。国内一组单纯主动脉瓣瓣周漏治疗数据显示再次行主动脉瓣置换或Bentall术的死亡率约6%~11.8%,而行封堵术死亡率为零[8]。近年,国内外关于微创封堵瓣周漏报道成功率约60%~90%[4,16-17]。因此目前微创封堵瓣周漏是首选推荐治疗方法,外科常规手术治疗瓣周漏适应证包括以下4种:(1)接受冠状动脉旁路移植或其他瓣膜手术的患者;(2)活动性心内膜炎;(3)瓣周漏长度> 1/3人工假体环形周长;或(4) 微创封堵治疗失败者[17]。内科介入封堵需要经双侧股动脉,路径长而略显曲折,全程需要X线照射及造影剂的注射,仍须TEE判断封堵效果,若一旦封堵器脱落及其他因素导致操作失败仍需要心脏外科紧急治疗,如果术前合并肾功能不全[18],介入导管封堵瓣周漏术后引起造影剂肾病,肾功能衰竭进一步加重心力衰竭。
瓣周漏的封堵治疗首选是明确诊断,精准判断其位置、形状、大小,据有研究显示主动脉瓣位的瓣周漏以无冠瓣、右冠瓣多发[19],目前瓣周漏的诊断主要依靠经胸超声心动图,但是对于瓣周漏的形状、大小的判断仍有一定的困难,增强CT血管造影、磁共振成像虽然有助于诊断,但在临床中的应用仍存在一定的局限[20]。随着超声影像技术发展,3维超声心动图对瓣周漏的大小、形状、出入口及血流方向的显示非常清晰,已成为瓣周漏详细评估和更准确评估的必不可少的成像技术[21-22]。3D-TEE在封堵瓣周漏过程中具有重要指导价值[23],如果在经胸封堵瓣周漏中应用3D-TEE,将进一步提高手术操作的可靠性、缩短手术时间。
本组病例采取经胸肋间“打孔”微创入路,于升主动脉处穿刺,操作路径大大缩短,对导管的控制能力明显增加。全程在TEE监视下进行,判断的准确性和安全性显著增加。TEE可准确判断瓣周漏的位置、大小、形态,不仅利于选择合适大小的封堵器,而且能精确定位,指导鞘管顺利通过瓣周漏口。因为无需X线,所以避免了长时间X线照射和造影剂相关并发症。
FustarTM可调鞘管是本研究另一亮点。鞘管远端有显影环,有助于在TEE下精准定位,该鞘管头端的25 mm可调弯曲度为0°~180°。在TEE引导下,通过FustarTM可调鞘管调整到合适弯度和角度,使得鞘管的头端恰好指向瓣周漏口,协助导丝先行通过漏口,随之鞘管亦顺利跟进。因此,FustarTM可调鞘管是协助建立路径的利器,一步到位,节约手术时间,降低对血管的损伤。
本研究2例患者术后进行了6~16个月随访,NYHA心功能分级均为Ⅰ级,均未发生封堵器脱落、无残余漏、无新增心律不齐、无卡瓣以及封堵器相关瓣膜关闭不全。初步经验:显示在TEE引导下,采用FustarTM可调弯鞘协助建立路径,经胸微创“打孔”封堵主动脉瓣瓣周漏安全、有效。FustarTM可调弯鞘在TEE下显影清晰,经胸骨旁途经操作路径短、更加可控,较X线下介入导管更易通过漏口,可降低介入封堵瓣周漏的难度,减少手术操作时间,减少并发症,避免X线照射及造影剂的使用,为治疗主动脉瓣瓣周漏提供了一种可靠的方案,但仍需更大样本量的研究证实其安全性及临床效果。
利益冲突:所有作者均声明不存在利益冲突
——一种安全简便的房间隔穿刺新方法

