绿原酸、异绿原酸A抑制亚硝化反应研究
胡昭君 李冬梅 杜华英 ,2 杜 娟 ,2 熊建华 ,2*
(1江西农业大学食品科学与工程学院 南昌 330045
2南昌市农产品加工与质量控制重点实验室 南昌 330045)
亚硝酸盐广泛存在于人们的日常生活中,蔬菜、千滚水、火锅等都含有亚硝酸盐[1]。在肉制品加工过程中,亚硝酸盐不仅会自然富集,而且常作为发色剂和防腐剂添加到肉制品中[2]。过量的亚硝酸盐可使人体中毒[3],亚硝酸盐可与人体中的胺类物质反应生成强致癌物亚硝胺,导致人类罹患胃癌、肝癌等癌症[4]。我国对食品中亚硝酸盐含量提出了明确的限量标准[5]。研究可清除食品中亚硝酸盐,抑制亚硝胺合成的亚硝化反应因素具有重要意义。
研究发现含有VC、黄酮类、酚类等植物提取物具有一定的清除亚硝酸盐能力[6]。绿原酸类物质属酚类化合物,分为3-O-咖啡酰奎宁酸 (绿原酸)、4-O-咖啡酰奎宁酸、5-O-咖啡酰奎宁酸、3,4-二咖啡酰奎宁酸、3,5-二咖啡酰奎宁酸(异绿原酸 A )、4,5-二咖啡酰奎宁酸、3-,4-,5-阿魏酰奎宁酸等,不仅存在于忍冬科、杜仲科、菊科等药食两用植物中,在水果、蔬菜及茶叶等食品中也有一定含量[7-8],具有抗癌、抗氧化、降糖降脂、抗菌抗病毒等多种药理功能[9-11],常添加到食品、药品、化妆品中以增加食品的保质期、利用率和更好地治疗疾病、护理皮肤[12-13]。本文以抗坏血酸和芦丁作为参照品,研究绿原酸、异绿原酸A清除亚硝酸盐和阻断亚硝胺合成的抑制亚硝化反应能力及条件,为清除亚硝酸盐,阻断亚硝胺合成提供天然安全途径。
1 材料与方法
1.1 试剂与仪器
主要试剂:异绿原酸A(≥99%)、亚硝酸钠标准品、1-萘胺,Aladdin Chemistry Co.Ltd;绿原酸、芦丁标准品,中国药品生物制品鉴定所;二甲胺40%水溶液,天津市大茂化学试剂厂;无水对氨基苯磺酸,上海三爱思试剂有限公司;N-1-萘乙二胺盐酸盐,天津市福晨化学试剂厂。
主要仪器:SpectraMax M2酶标仪,Molecular Devices公司;UV-9100紫外-可见分光光度计,上海元析仪器有限公司;移液器,Thermos;PHS-3C pH计,上海仪电科学仪器股份有限公司。
1.2 方法
1.2.1 最佳检测波长的确定 准确吸取已配制的5 μg/mL亚硝酸钠标准液2 mL于25 mL容量瓶中,加入pH 3.4的柠檬酸(0.1 mol/L)-磷酸氢二钠(0.2 mol/L)缓冲溶液18.75 mL,37℃水浴30 min后取出,加入0.4%对氨基苯磺酸溶液2 mL,混匀静置3 min,加入1 mL 0.2%盐酸萘乙二胺溶液,用蒸馏水稀释至25 mL,混匀放置15 min,用重蒸馏水代替亚硝酸钠溶液,以相同配制方法处理的溶液作参比,用紫外-可见分光光度计在波长400~800 nm范围进行扫描,确定最大吸收波长λmax。
1.2.2 亚硝酸钠标准曲线的测定 参照谢文仙等[14]方法并稍作改动。 分别吸取 0.5,1.0,2.0,3.0,4.0,5.0,6.0 μg/mL 亚硝酸钠标准应用液 16 μL 于酶标板的微孔中,加入pH 3.4的柠檬酸(0.1 mol/L)-磷酸氢二钠(0.2 mol/L)缓冲溶液 150 μL,37 ℃水浴12 min后取出,立即加入0.4%对氨基苯磺酸16 μL,混匀后静置 5 min,加入 8 μL 0.2%盐酸萘乙二胺溶液,用重蒸馏水稀释至200 μL,混匀后静置15 min。在确定的最大吸收波长处测定吸光度(AX),同时做空白试验(A0)。 每个处理重复 3次,计算平均值,绘制标准曲线。
1.2.3 绿原酸清除亚硝酸盐的研究
1.2.3.1 不同浓度时清除亚硝酸盐的效果 配制质量浓度为 0.5,1,2,3,4,5,6,7,8 μg/μL 的绿原酸、异绿原酸A、VC、芦丁等溶液,分别吸取上述溶液 10 μL 于酶标板的微孔中,加入 16 μL 5 μg/mL亚硝酸钠溶液,再加入pH 3.4的柠檬酸-磷酸氢二钠缓冲溶液150 μL,在37℃水浴30 min后取出,立即加入0.4%对氨基苯磺酸16 μL,混匀后静置5 min,加入8 μL 0.2%盐酸萘乙二胺溶液,混匀后静置15 min,在确定的最大吸收波长处测定吸光度(AXX),同时用蒸馏水代替样品做空白试验(AX0),计算清除率并绘制变化图。
1.2.3.2 不同pH值时清除亚硝酸盐的效果 分别吸取上述试验得到的最佳浓度的绿原酸、异绿原酸A、VC、芦丁溶液各10 μL于酶标板的微孔中,分别加入16 μL 5 μg/mL亚硝酸钠溶液和pH值分别为 2.8,3.4,4.0,4.6,5.2,5.8 的柠檬酸-磷酸氢二钠缓冲溶液150 μL,然后于37℃水浴锅中反应30 min,按照同上操作加入试剂,测定吸光度,计算清除率并绘制亚硝酸盐清除率变化图。
1.2.3.3 不同反应时间时清除亚硝酸盐的效果 依据上述试验结果,准确吸取10 μL最佳浓度的绿原酸溶液、异绿原酸A溶液、VC溶液、芦丁溶液于酶标板的微孔中,再加16 μL 5 μg/mL亚硝酸钠溶液和150 μL最佳pH的柠檬酸-磷酸氢二钠缓冲溶液于酶标的微孔中,分别置于温度37℃的水浴锅中,反应 5,10,20,30,40,50 min 后取出,加入0.4%对氨基苯磺酸16 μL,反应5 min,加入8 μL 0.2% 盐酸萘乙二胺溶液,混匀后静置15 min。在确定的最大吸收波长处测定吸光度,计算亚硝酸盐清除率并绘制变化图。
1.2.3.4 不同温度时清除亚硝酸盐的效果 添加10 μL最佳浓度绿原酸等溶液于酶标板的微孔中,加入16 μL 5 μg/mL亚硝酸钠溶液和最佳pH值的柠檬酸-磷酸氢二钠缓冲溶液150 μL,置于温度分别为 4,17,27,37,47,57 ℃的水浴锅中,反应一定时间后取出,加入试剂进行显示反应并测定吸光度,计算亚硝酸盐清除率并绘制变化图。
1.2.4 绿原酸阻断亚硝胺合成的研究
1.2.4.1 不同浓度对阻断亚硝胺合成的影响 准确配制 0.5,1,2,3,4,5 μg/μL 等不同浓度的绿原酸、异绿原酸A、VC、芦丁溶液,分别吸取上述溶液10 μL于洗净的离心管中,10 mmol/L亚硝酸钠溶液、10 mmol/L二甲胺溶液各8 μL,加入pH 3.4的柠檬酸-磷酸氢二钠缓冲溶液至200 μL,在37℃下水浴30 min。准确吸取反应液8 μL于酶标板的微孔中,加入0.5%碳酸钠溶液4 μL,在紫外-可见分光光度仪(选定波长254 nm)上照1 h。取出后加入1%对氨基苯磺酸12 μL,混匀静置3 min,再加入 0.1% α-萘胺 12 μL、蒸馏水 4 μL,混匀静置30 min。在确定的最大吸收波长510 nm处测定吸光度(AYX),平行试验3次,求平均值。同时做空白对照试验(AY0),计算亚硝酸胺合成阻断率并绘制变化图。
1.2.4.2 不同pH值对阻断亚硝胺合成的影响配制 pH 值分别为 2.2,2.8,3.4,4.0,4.6,5.2,5.8 的柠檬酸-磷酸氢二钠缓冲溶液,根据1.2.4.1节的试验结果,分别吸取最佳浓度的4种溶液10 μL、8 μL 10 mmol/L亚硝酸钠和10 mmol/L二甲胺溶液于洗净的0.5 mL离心管中,加入不同pH缓冲液至200 μL,于37℃水浴锅中水浴30 min,按照同1.2.4.1节步骤,加入试剂进行反应,并测定吸光度,计算亚硝酸胺合成阻断率并绘制变化图。
1.2.4.3 不同反应时间阻断亚硝胺合成的效果根据以上试验的结果,准确吸取10 μL最佳浓度的4种物质,10 mmol/L亚硝酸钠溶液和10 mmol/L二甲胺溶液各8 μL于离心管中,加最佳pH值缓冲液至200 μL,于温度37℃的水浴锅中分别反应 1,3,5,10,20,30 min 后取出,按照同上操作测定吸光度值,计算亚硝酸胺合成阻断率并绘制变化图。
1.2.4.4 不同温度时阻断亚硝胺合成的效果 在以上试验基础上,取最佳浓度绿原酸、异绿原酸A、VC、芦丁溶液 10 μL,8 μL 10 mmol/L 亚硝酸钠溶液和10 mmol/L二甲胺溶液于离心管中,加最佳pH缓冲液至200 μL,置于温度分别为4,17,27,37,47,57℃的水浴锅中反应最适时间后,按同上步骤测定吸光度值,计算亚硝酸胺合成阻断率并绘制变化图。
1.2.5 抑制亚硝化条件优选 根据绿原酸类物质清除亚硝酸盐及阻断亚硝胺合成的最适条件与变化规律优选抑制亚硝化条件并做验证试验。
1.2.6 亚硝酸盐清除率和亚硝胺合成阻断率的统计 以上每个试验重复3次,同时做空白对照试验,按照公式1和公式2进行亚硝酸盐清除率和亚硝酸胺合成阻断率的计算,并根据结果绘制各变化图。
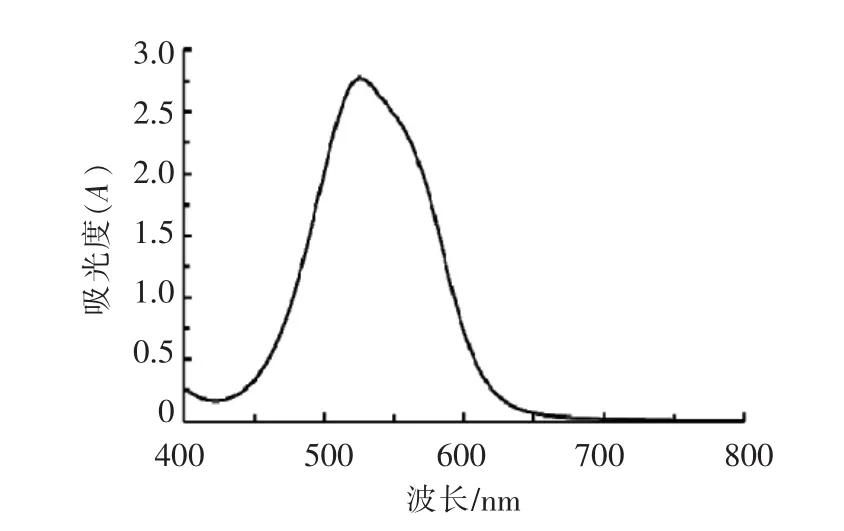
图1 吸收波长曲线Fig.1 The curve of absorption wavelength
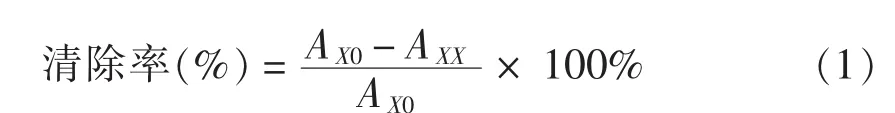
式中,AX0——未加样液时的吸光度值;AXX——加样液时的吸光度值。
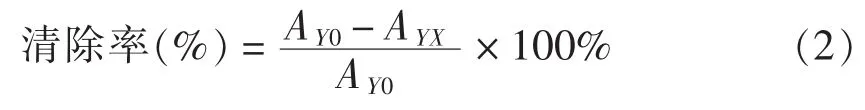
式中,AY0——未加样液时的吸光度值;AYX——加样液时的吸光度值。
2 结果与讨论
2.1 最大测定波长
由图1可知,亚硝酸钠反应液的最大吸收波长为526 nm。
2.2 标准曲线的绘制
以亚硝酸钠浓度为横坐标,以测定的吸光度值为纵坐标,绘制标准曲线图2,并对数据进行线性回归处理,得到回归方程y=0.125x+0.016,R2=0.998,说明在本试验条件下,亚硝酸钠溶液在0.5~6.0 μg/μL质量浓度范围线性关系良好。可以通过吸光度来计算样品中亚硝酸盐的浓度。
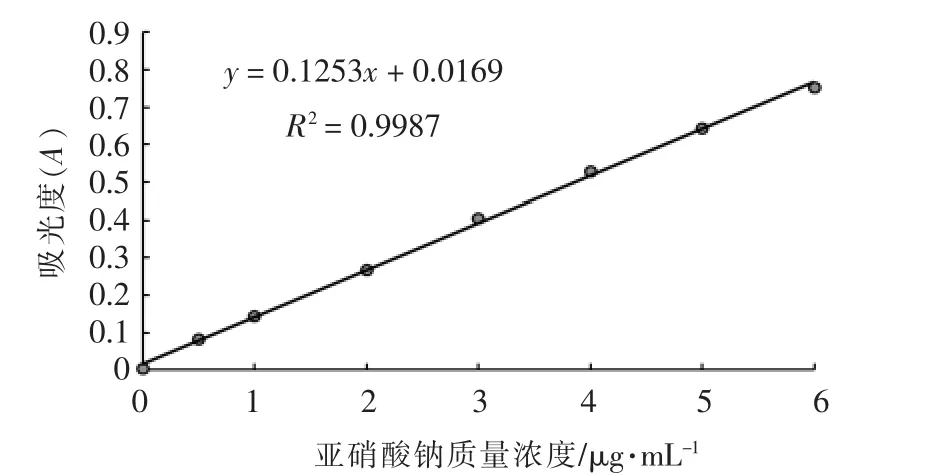
图2 亚硝酸钠标准曲线图Fig.2 Standard curve of sodium nitrite
2.3 清除亚硝酸盐的研究
2.3.1 各物质浓度对亚硝酸盐清除率的影响 绿原酸等物质浓度对亚硝酸盐的清除作用如图3所示。绿原酸对亚硝酸盐的清除率随浓度的增加而升高,当质量浓度为5 μg/μL时对亚硝酸盐的清除率逐渐稳定,此时的清除率为57.34%;异绿原酸A清除亚硝酸盐的作用较绿原酸好,当质量浓度为4 μg/μL时清除率达59.83%,浓度继续增大清除效果增加渐缓;芦丁和VC在低浓度时效果介于异绿原酸A与绿原酸之间,质量浓度大于5 μg/μL时清除效果好于异绿原酸A,当质量浓度为7 μg/μL时清除率增加变缓,此时芦丁和VC清除率分别为 69.03%,72.41%。5 μg/μL 时样品和对照品清除效果相差较小,选择5 μg/μL质量浓度做下一步试验。
2.3.2 pH值对亚硝酸盐清除率的影响 绿原酸类物质随pH值变化对亚硝酸盐的清除率的试验结果如图4所示。pH值对各物质清除亚硝酸盐的影响较大,4种物质随pH值的增大其清除率降低,其中绿原酸、VC随pH值升高降低较缓慢,可在较大的范围内保持较好的活性。绿原酸pH 3.4时对亚硝酸盐的清除率为57.44%,pH 4.0时清除率保持在53.97%。VC在pH 3.4时对亚硝酸盐的清除率为60.49%,pH 4.0时清除率保持在58.00%。异绿原酸A随pH值的升高快速降低,芦丁随pH值的增大先缓慢下降后快速降低。pH值通过影响绿原酸等物质中羟基的解离形式,进而影响绿原酸等物质与亚硝酸盐反应,尤其异绿原酸A分子中含有更多的羟基,对pH值的变化更敏感。在所选pH范围,芦丁和VC的清除效果好于绿原酸和异绿原酸A,而在pH 2.8和3.4时4种物质的清除效果相差不大,都比较好;pH 2.8~3.4时与人体胃液酸度比较接近,绿原酸能在其中保持较好的活性,可清除胃中的亚硝酸盐,减少人体因亚硝酸盐过量引起的中毒等不良反应的发生。pH 3.4的酸性较缓和,选择pH 3.4作为下一步试验的pH。
2.3.3 反应时间对亚硝酸盐清除率的影响 反应时间对绿原酸类物质清除亚硝酸盐的影响见图5。4种物质都随时间的增加对亚硝酸盐的清除作用增强。其中绿原酸、异绿原酸A和芦丁变化规律较为一致,都先快速增加后缓慢增加,40 min时的清除率分别为61.43%,67.44%,70.73%;当反应时间小于20 min时VC的作用效果小于绿原酸,随着作用时间的增长,其作用效果稍强于绿原酸,40 min时的清除率为64.25%。40 min后4种物质的清除率都增加缓慢,再延长反应时间意义不大。最终选择40 min做下一步试验。
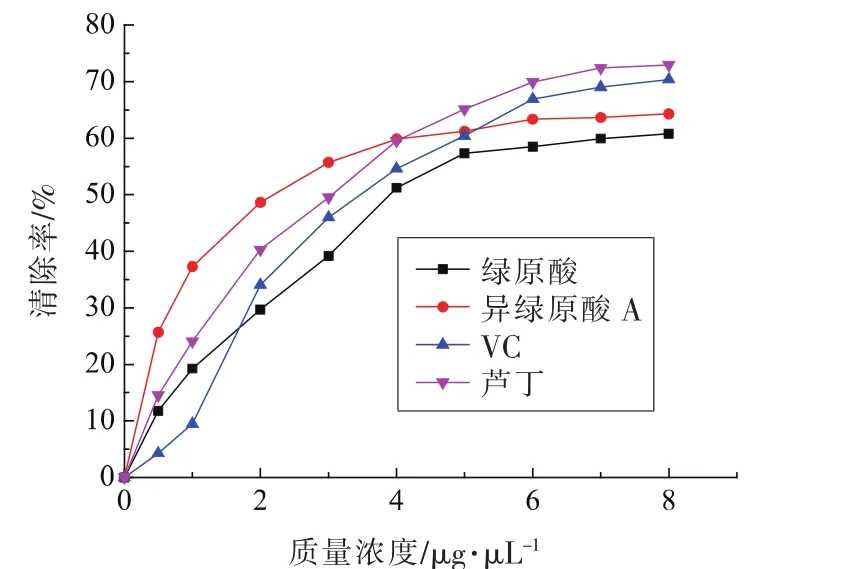
图3 各物质浓度对亚硝酸盐清除率的影响Fig.3 Effect of different concentrations on the rate of cavenging nitrite
2.3.4 温度对亚硝酸盐清除率的影响 绿原酸等物质随温度的变化对亚硝酸盐的清除率的试验结果见图6。4种物质随温度的增大对亚硝酸盐的清除作用增大;在低温时4种物质的清除作用相差较大,随着温度的升高,物质间的清除率差距减小;47℃时4种物质间的差距最小,此时绿原酸和异绿原酸A的清除率分别为79.69%和78.15%;57℃时各物质的清除率增加较小。相对于高温,47℃更易保存食品的理化品质。最终选择47℃作为反应温度。
绿原酸、异绿原酸A清除亚硝酸盐的效果较好,总体而言,异绿原酸A好于VC,绿原酸与VC相近,两者清除效果略低于芦丁。清除作用与体系温度、pH值、反应时间等各种因素有关。5 μg/μL绿原酸和异绿原酸A在pH 3.4,温度47℃的条件下作用40 min,可清除79.69%和78.15%的亚硝酸盐。
2.4 阻断亚硝胺合成的研究
2.4.1 不同浓度绿原酸类物质对亚硝胺合成阻断率的影响 胃中的胺类物质可与亚硝酸盐反应生成强致癌物亚硝胺,消除亚硝酸盐可在一定程度上阻断亚硝胺的生成,然而亚硝胺的形成受温度、pH等因素的影响。本试验以VC和芦丁为参照,研究绿原酸类物质在不同条件下对亚硝胺合成的阻断效果。添加不同浓度的绿原酸类物质影响亚硝胺合成阻断率的试验结果。如图7所示,各物质对亚硝胺合成的阻断率随浓度的增大先快速升高后缓慢升高,绿原酸和VC的阻断效果较为接近,当质量浓度为3 μg/μL时阻断率分别为48.49%,50.86%;异绿原酸A阻断效果好于VC,当质量浓度为3 μg/μL时阻断率达60.96%;芦丁阻断效果最好,质量浓度为1 μg/μL时阻断率就达68.75%;4种物质在质量浓度大于3 μg/μL后虽有上升,但上升程度小,故选择3 μg/μL进行下一步试验。
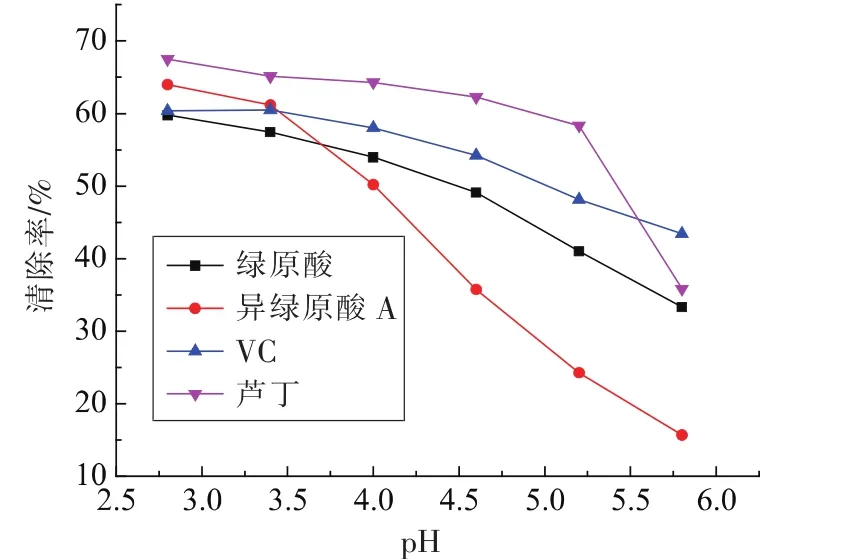
图4 不同pH值对亚硝酸盐清除率的影响Fig.4 Effect of different pH on the rate of cavenging nitrite
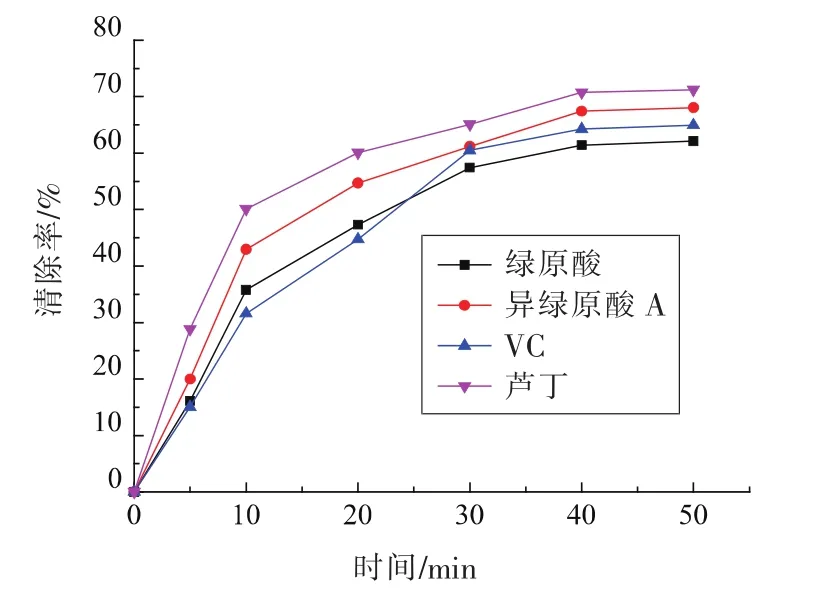
图5 不同反应时间对亚硝酸盐清除率的影响Fig.5 Effect of different action time on the rate of cavenging nitrite
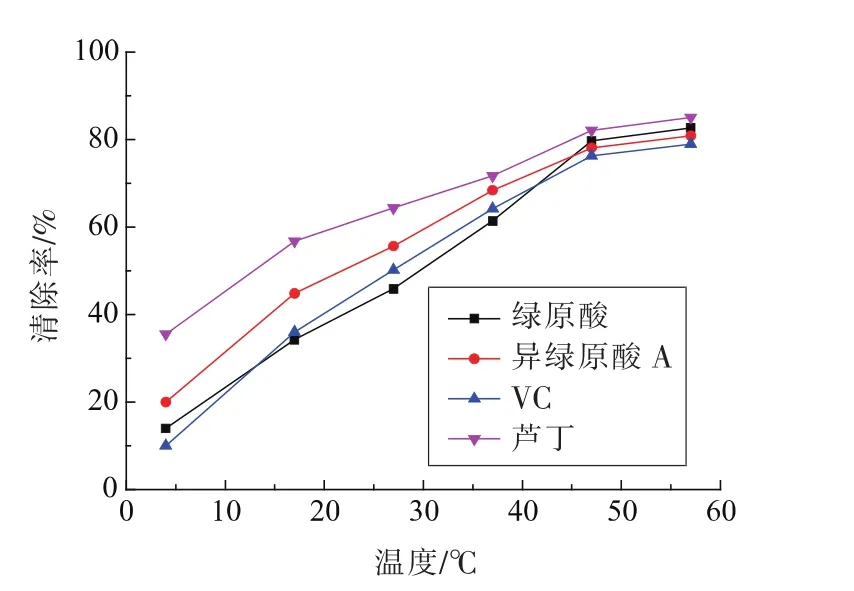
图6 不同温度对亚硝酸盐清除率的影响Fig.6 Effect of different temperature on the rate of cavenging nitrite
2.4.2 pH值对亚硝胺合成阻断率的影响 绿原酸等物质在不同pH值条件下对亚硝胺合成的阻断效果见图8。随着pH值的增大,4种物质的阻断率降低。在试验的pH范围内4种物质中芦丁的阻断率高,其次为异绿原酸A,绿原酸和VC的阻断效果不及异绿原酸A。当pH值为2.8时绿原酸、异绿原酸A、VC、芦丁4种物质相较于pH 3.4具有较好的阻断亚硝胺合成的作用,阻断率分别为 60.89%,68.46%,63.28%,76.57%。 最终选择pH 2.8做下步试验。
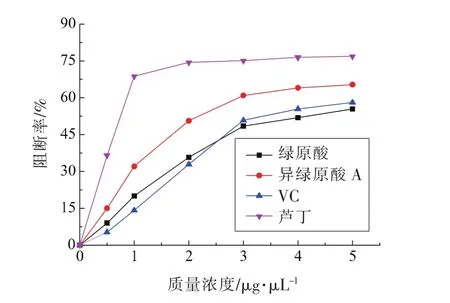
图7 不同浓度绿原酸类物质对亚硝胺合成阻断率的影响Fig.7 Effect of different concentration chlorogenic acids on the rate of blocking synthesis of nitrosamine
2.4.3 反应时间对亚硝胺合成阻断率的影响 图9显示不同时间4物质阻断亚硝胺合成的效果。随着时间的增加,各物质对亚硝胺合成的阻断率先快速增加,尤其在5 min前,20 min后增加趋势不明显,最终选择20 min为最佳的反应时间。阻断效果排序为芦丁、异绿原酸A、VC、绿原酸,这4种物质在5 min的阻断率分别为72.79%,58.39%,49.91%,44.72%,20min时的阻断率分别为76.29%,64.99%,60.53%,58.04%。
2.4.4 温度对亚硝胺合成阻断率的影响 不同温度下各种物质阻断亚硝胺合成的效果见图10。芦丁、异绿原酸A、VC、绿原酸的阻断率都随温度的升高而逐渐增加,各物质在47℃时阻断率较为接近,分别为 77.43%,68.31%,67.09%,70.93%,此时绿原酸的阻断率强于异绿原酸A和VC。可见温度对绿原酸阻断亚硝胺合成有较为显著的促进作用。57℃时绿原酸等物质的阻断率上升不显著,47℃为合适的反应温度。
总体而言,对亚硝胺合成合成反应阻断效果:芦丁最好,异绿原酸其次,绿原酸与VC相近。
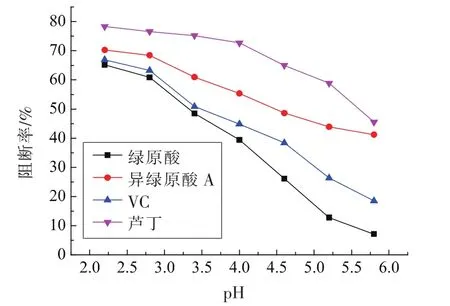
图8 不同pH对亚硝胺合成阻断率的影响Fig.8 Effect of different pH on the rate of blocking synthesis of nitrosamine
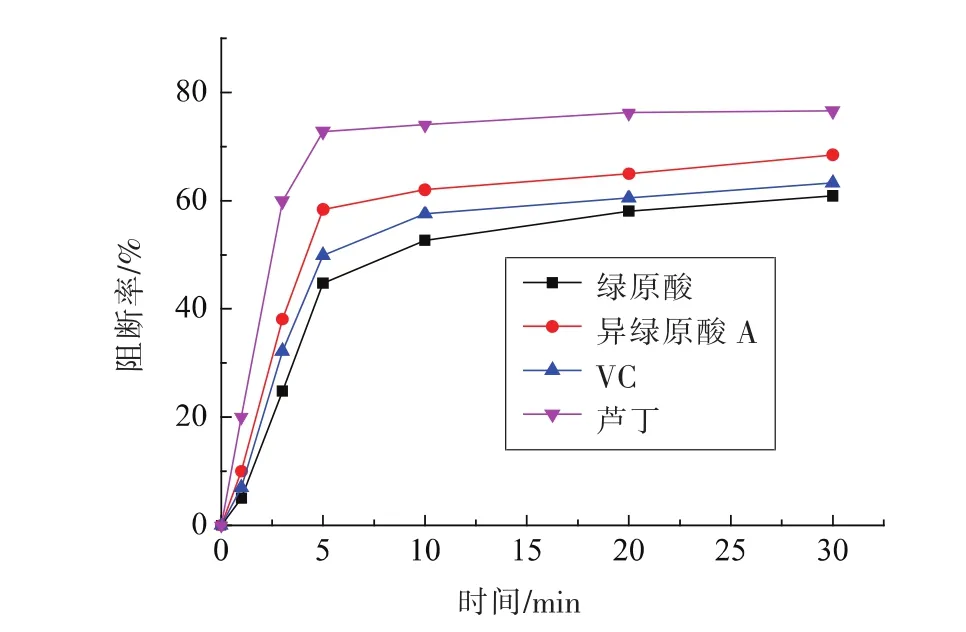
图9 不同反应时间对亚硝胺合成阻断率的影响Fig.9 Effect of different action time on the rate of blocking synthesis of nitrosamine
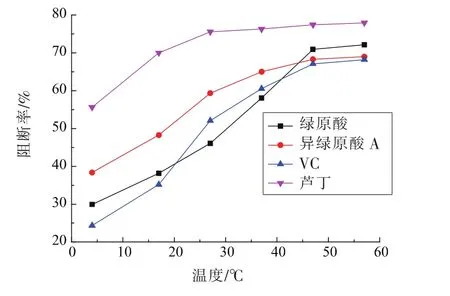
图10 不同温度对亚硝胺合成阻断率的影响Fig.10 Effect of different temperature on the rate of blocking synthesis of nitrosamine
2.5 抑制亚硝化反应的研究
绿原酸、异绿原酸A清除亚硝酸盐的最适浓度、pH、反应时间、 温度分别为 5 μg/μL,3.4,40 min和47℃,阻断亚硝胺合成合成的最适浓度、pH、 反应时间和温度分别为 3 μg/μL,2.8,20 min及47℃,且抑制亚硝化反应效果变化趋势一致,均随浓度、反应时间和温度的升高逐渐增强,随pH的升高而降低。最终选择抑制亚硝化反应条件样品浓度 5 μg/μL、pH 2.8、反应时间 40 min、温度47℃并进行验证试验(表1)。
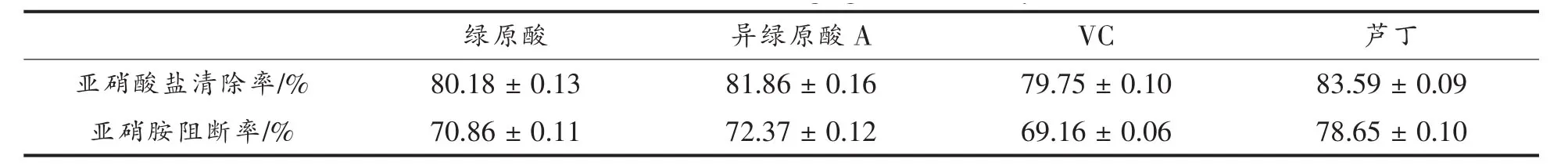
表1 4种物质对清除亚硝酸盐和阻断亚硝胺合成的效果Table1 Effect of four substances on cavenging nitrite and synthesis of nitrosamine
所选反应条件下绿原酸和异绿原酸A的亚硝酸盐的清除率在80%以上,亚硝胺合成阻断率在70%以上,均有较好的抑制亚硝化效果。
绿原酸和异绿原酸A都有较好的抑制亚硝化反应的能力,随反应体系环境的变化而存在差异。
3 结论
绿原酸类物质清除亚硝酸盐及阻断亚硝胺合成的抑制亚硝化效果随浓度、反应时间和温度的升高逐渐增强,随pH值的升高而降低。清除亚硝酸盐的最适质量浓度 5 μg/μL,pH 3.4,反应时间40 min,温度47℃;阻断亚硝胺合成的最适质量浓度 3 μg/μL,pH 2.8,反应时间 20 min 和温度 47℃;抑制亚硝化反应最适条件为质量浓度5 μg/μL、pH 2.8、反应时间 40 min、温度 47℃。 在抑制亚硝化反应方面,绿原酸与VC效果相当,稍弱于异绿原酸A,三者效果弱于芦丁。

