老年冠心病合并高血压患者血清NO、Lp-PLA2、Hcy水平与颈动脉粥样硬化程度的关系
李 凤,陈静丹,薛桂君
(四川大学华西医院健康管理中心,四川 成都610041)
数据统计,2010年心血管疾病在全世界死亡人群中占29.60%(1560万死亡),比癌症患者死亡高2倍[1]。且近年来受老龄化、饮食结构变化影响,冠心病发病率仍较高,对冠心病的研究一直是临床重点。冠心病主要由冠脉粥样硬化引起,高血脂、高血压、吸烟等是其发生危险因素。目前临床上冠心病合并高血压比较常见,且颈动脉粥样硬化程度被认为是冠心病合并高血压的直观指标[2]。颈动脉粥样硬化机制复杂,血管内皮功能损伤、炎症、氧化应激等均可能引发之。一氧化氮(NO)为内皮功能损伤反映指标之一,脂蛋白相关磷脂酶A2(Lp-PLA2)为炎性标志物,同型半胱氨酸(Hcy)为蛋氨酸代谢中间产物,其异常表达被认为是冠脉粥样硬化发生的独立危险因子[3-5]。本研究主要分析老年冠心病合并高血压患者血清NO、Lp-PLA2、Hcy水平表达及其与颈动脉粥样硬化程度的关系,以为疾病防治提供参考。
材料和方法
1 对象
选择本院2016年1月至2018年1月收治的老年冠心病患者260例,其中男160例,女100例,年龄47~79岁,平均63.1±7.0岁。其中合并高血压153例(合并组),不合并高血压107例(冠心病组)。选择同期体检健康人员70例(对照组),其中男40例,女30例,年龄40~76岁,平均62.6±8.0岁。
2 诊断标准
冠心病诊断依据美国心脏病学会提出的标准[6];高血压诊断依据中国高血压防治指南修订委员会提出的标准[7]。
3 纳入及排除标准
3.1 纳入标准 符合相关诊断标准;年龄<80岁;均配合完成相关检查;资料完整;知情并签署同意书。
3.2 排除标准 恶性肿瘤;血液疾病;肝肾功能异常;感染性疾病;近期有使用过影响血清NO、Lp-PLA2、Hcy水平的药物;近期有重大手术史;瓣膜性心脏病;资料不全。
4 方法
4.1 血清指标测定 统一上午8点空腹抽血4mL,静置半个小时后以3000r/min离心15min,血清提取后放入EP管内,保存于-80℃冰箱内。血清NO、Lp-PLA2、HCY水平均经由酶联免疫吸附法(ELISA)测定,试剂盒均购自上海一研生物科技有限公司,依据试剂盒说明书操作。
4.2 颈动脉粥样硬化程度 对患者行多普勒超声(迈瑞DC-6)检查,探测两侧颈动脉厚度,取均值,即颈动脉内膜-中膜厚度(IMT),依据Grous积分法[8]判定。IMT 1mm以下,内膜不增厚计0分;IMT 1mm~<1.2mm,内膜局部增厚计1分;IMT 1.2mm~<1.5mm,斑块形成计2分;IMT 1.5mm~<2mm,轻度狭窄计3分;IMT 2.0mm及以上,动脉狭窄明显计4分。
5 统计学处理
SPSS20.0软件分析数据。计数资料以例表示,行χ2检验;计量资料以表示,多组间行单因素方差分析,两组间行独立样本t检验;相关性行Pearson分析。检验标准α=0.05。
结 果
1 基线资料
各组性别、年龄、体重指数比较差异无统计学意义(P>0.05)。见表1。
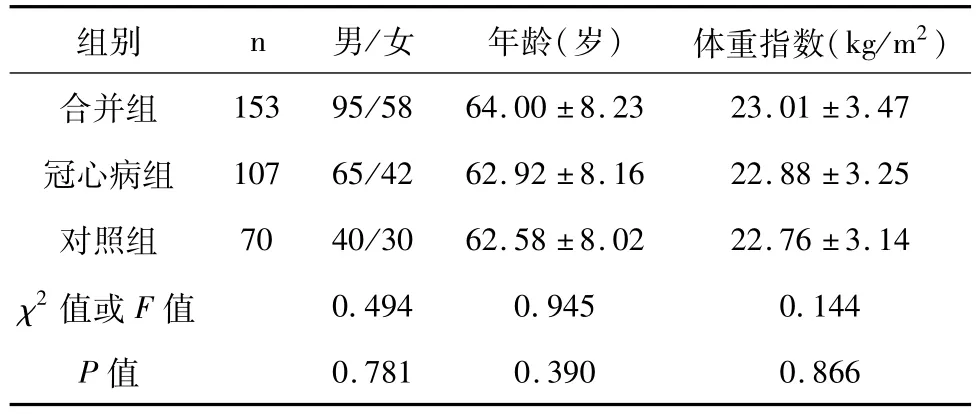
表1 各组对象基线资料比较
2 血清NO、Lp-PLA2、Hcy水平
各组血清NO、Lp-PLA2、Hcy水平比较差异有统计学意义(P<0.05);合并组血清NO水平明显低于、Lp-PLA2、Hcy水平明显高于冠心病组、对照组,差异有统计学意义(P<0.05)。见表2。
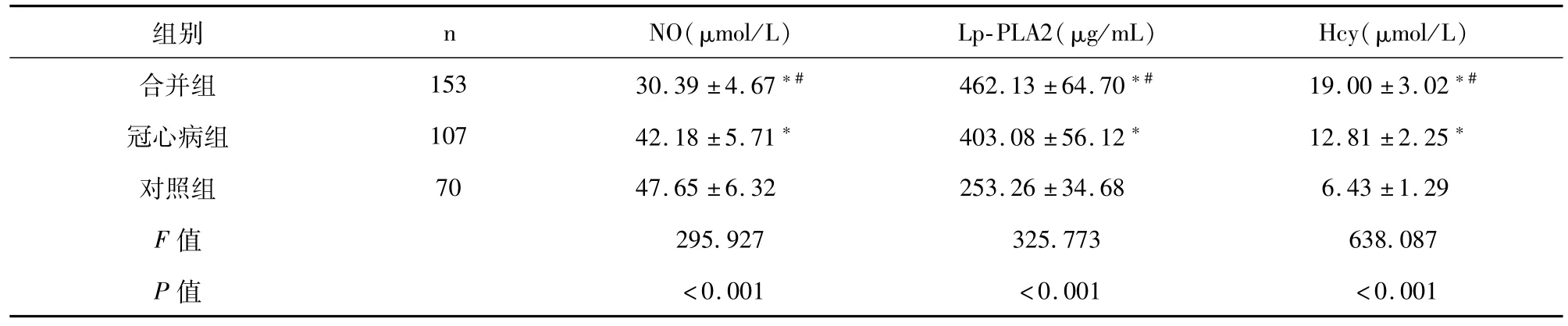
表2 各组对象血清NO、Lp-PLA2、Hcy水平比较
3 Grous积分
合并组患者Grous积分平均2.82±0.42分,冠心病组Grous积分平均2.00±0.24分,两组比较差异有统计学意义(t=18.216,P<0.05)。260例患者中Grous积分 <2分者110例(42.31%),≥2分者150例(57.69%)。
4 不同Grous积分患者血清NO、Lp-PLA2、Hcy水平
Grous积分<2分患者血清NO水平明显高于、Lp-PLA2、Hcy水平明显低于Grous积分≥2分者,差异有统计学意义(P<0.05)。见表3。
表3 不同Grous积分患者血清NO、Lp-PLA2、Hcy水平比较()
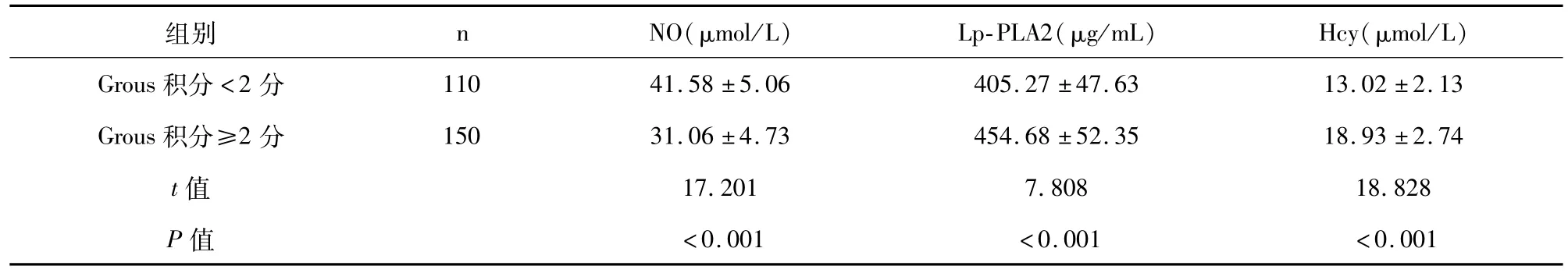
表3 不同Grous积分患者血清NO、Lp-PLA2、Hcy水平比较()
组别 n NO(μmol/L) Lp-PLA2(μg/mL) Hcy(μmol/L)Grous积分 <2分110 41.58±5.06 405.27±47.63 13.02±2.13 Grous积分≥2分 150 31.06±4.73 454.68±52.35 18.93±2.74 t值 17.201 7.808 18.828 P值 <0.001 <0.001 <0.001
5 相关性分析
Pearson相关性分析发现血清NO水平与Grous积分负相关(P<0.05),血清Lp-PLA2、Hcy水平与Grous积分正相关(P<0.05)。见表4。
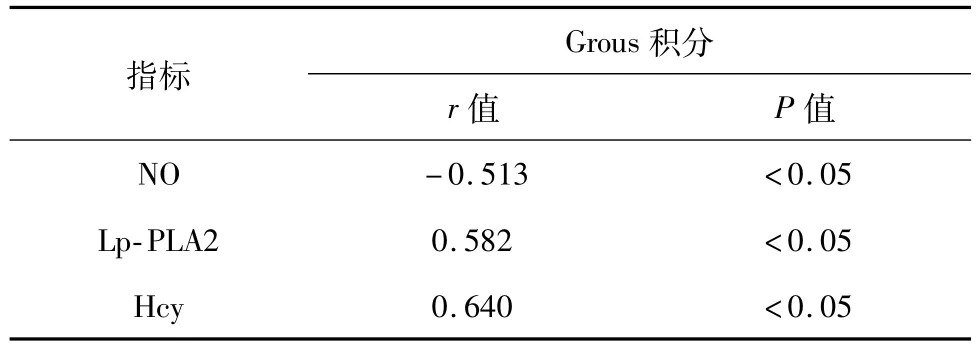
表4 血清NO、Lp-PLA2、Hcy水平与Grous积分的相关性
讨 论
动脉粥样硬化是高血压、冠心病等多种疾病发生的危险因素,其发生时多伴血管内皮功能损伤。临床上用于血管内皮功能评价指标之一为NO,血管内皮功能损伤时NO生成变少,血清NO水平下降。NO不仅对平滑肌细胞增殖有一定的抑制作用,促内皮细胞增殖,而且还对血小板聚集抑制,避免白细胞等黏附至内皮[9]。NO在血管扩张、免疫调节等中发挥重要作用,被认为是心血管系统保护因子。杨雪松等[10]研究表明NO诊断冠心病曲线下面积为0.723,Hcy曲线下面积为0.718,但Hcy与冠心病的关联强度比NO高。
Hcy被证实与冠脉粥样硬化密切相关,它除了经由自身氧化作用阻断蛋白质合成外,还对内皮有依赖性血管影响,致使其损伤,促进动脉粥样硬化发生,增加硬化斑块形成风险。血清Hcy水平上升会促平滑肌细胞增殖,加重颈动脉粥样硬化程度。同时高血清Hcy水平还会影响糖脂代谢,致使脂质沉积,增加动脉狭窄发生几率。另外它还能加快低密度脂蛋白氧化速度,间接对血管影响。李晓妹等[11]研究表明血清Hcy水平可作为冠心病诊断、病情变化评估的有效指标。许金鹏等[12]研究也发现血清Hcy水平在H型高血压合并颈动脉粥样硬化患者中高表达,且Hcy水平与炎症因子、斑块稳定性密切相关。
炎症是高血压、冠心病发生的共同机制之一,血压长时间控制不当,机体持续存在炎症,相关致炎因子异常上升,进行性造成心血管功能异常,可能导致心脏等其他器官损害,引发不良心血管事件。Lp-PLA2主要由巨噬细胞、T淋巴细胞等多种细胞分泌而成,不仅可对血小板活化因子等炎症介质水解以发挥抗动脉硬化作用,而且还能对氧化低密度脂蛋白内氧化磷脂水解,促动脉粥样硬化,具有双重特性。相关系统分析发现Lp-PLA2水平是引发不良心血管事件的独立因子[13]。杜文涛等[14]通过Logistic回归分析发现Lp-PLA2水平是高血压、冠心病发生的独立危险因子,且其对冠心病合并高血压风险有较大的预测价值。燕蒲娟等[15]研究发现Lp-PLA2水平在高血压合并冠心病患者中高表达,且其水平随高血压炎症反应增强而上升。
本研究结果显示相比健康人员,单纯冠心病、冠心病合并高血压患者血清NO水平显著降低,Lp-PLA2、HCY水平均显著升高,且冠心病合并高血压相比单纯冠心病更明显。提示血清NO、Lp-PLA2、HCY水平可能参与冠心病、高血压发生过程,增加冠心病合并高血压发生风险。Grous积分能客观反映颈动脉粥样硬化程度,以IMT为依据(IMT 1.2mm及以上判断为斑块形成),2分及以上提示颈动脉粥样硬化斑块形成。本研究结果显示冠心病合并高血压患者Grous积分相比单纯冠心病显著升高。提示颈动脉粥样硬化可能是冠心病合并高血压的有效评估指标。另外本研究发现Grous积分≥2分患者血清NO水平比Grous积分<2分显著降低,Lp-PLA2、HCY水平显著升高,且相关性分析发现血清NO与Grous积分负相关,Lp-PLA2、HCY与Grous积分正相关。提示血清NO、Lp-PLA2、HCY能作为冠心病合并高血压患者出现动脉粥样硬化的预警因子。但本研究也存在不足:未对NO、p-PLA2、HCY之间的关系分析;未将高血压分类(如H型高血压)。对此有待日后通过相关资料深入查阅,扩大样本例数进一步分析。

