带鱼蛋白水解肽-金属配合物制备工艺
王晓玲*,张玉清,贺延茏,韦素贞,付砚渤,张雨晴
威海海洋职业学院食品工程系(荣成 264300)
带鱼(Hairtail)是我国盛产的四大经济鱼种之一,在中国的黄海、东海、渤海一直到南海都有分布。在带鱼加工过程中产生的下脚料占带鱼质量的1/2以上[1-2],这些下脚料中含有丰富的优质蛋白资源,若随意丢弃不仅浪费资源,还会污染环境,故有效利用带鱼下脚料便成为研究热点。
蛋白肽金属螯合物是多肽、小肽或氨基酸与金属离子以配位键结合而成,具有营养高、吸收快及多种生物活性等优点。目前关于金属螯合物的文献,主要集中于金属螯合物抑菌、抗氧化、降血脂、降血糖及免疫调节等活性研究。Sarah等[3]研究发现GHTD氨基化合物及其类似物ISF402与锌配合后与胰岛素并用,与单独使用胰岛素相比,可显著降低患糖尿病小鼠体内血糖。Ambar等[4]研究发现Humanin肽对β-淀粉样蛋白产生的神经毒素有抑制作用,是因为该肽分子中螯合有锌离子,形成八面体的配合物。
试验以带鱼下角料为原料,经木瓜蛋白酶酶解得带鱼蛋白水解肽,并与氯化亚铁、氯化镁、氯化锌、氯化钙螯合,制得4种对应带鱼蛋白水解肽-金属配合物,即铁肽、镁肽、锌肽、钙肽。研究水解条件及螯合条件对配合物的影响,为优化带鱼蛋白水解肽-金属配合物的制备条件,并为后期研究带鱼蛋白水解肽-金属配合物脱除重金属活性研究准备,以期发明一种高效、经济、环保脱出重金属的方法。
1 材料与方法
1.1 材料与试剂
带鱼下脚料,市售,将带鱼经碎肉粉碎机粉碎后,分装成100 g/袋,于-18 ℃冰箱冷冻保存,使用前于4 ℃冰箱解冻24 h。
1 000 mg/L铁标准溶液,上海西格玛奥德里奇贸易有限公司;1 000 U/mg木瓜蛋白酶,上海金穗生物科技有限公司;盐酸羟胺,分析纯,北京陆桥技术有限责任公司;溴酚蓝,分析纯,天津市福晨化学试剂厂;氯化亚铁(FeCl2·4H2O)、氯化镁(MgCl2· 6H2O)、氯化锌(ZnCl2)、氯化钙(CaCl2)、盐酸(HCl)、氢氧化钠(NaOH)、抗坏血酸、乙酸钠及三氯甲烷(CHCl3),分析纯(AR),国药集团化学试剂有限公司;试验过程中所使用的水皆为去离子水。
1.2 仪器与设备
CR 21 G型冷冻离心机,日本日立公司;WTM-1812 G型卷式膜分离设备,杭州沃腾膜工程有限公司;冷冻干燥机,美国LABCONCO公司;EYEL 4型旋转蒸发仪,上海爱朗仪器有限公司;UV-2600型紫外可见分光光度计,尤尼柯(上海)仪器有限公司。
1.3 带鱼蛋白水解肽的制备
取20 g解冻好的带鱼下脚料,加入200 mL去离子水,匀浆后调节pH为6.5,在45 ℃下保温10 min。按带鱼下脚料质量加入适量的木瓜蛋白酶,在一定温度下进行酶解,酶解过程中不断搅拌,并且每隔2 h调节pH。酶解结束后,于90 ℃水浴灭酶10 min,混合液在4 ℃下以5 000 r/min离心20 min,除去上层油膜和下层沉淀即为带鱼蛋白水解肽。酶解条件由试验探究优化得出,料液比1:10 g/mL、加酶量20 000 U/g带鱼、45℃、pH 6.5、酶解6 h,带鱼蛋白水解度高达71.3%。
1.4 蛋白水解肽-金属元素配合物的制备
将上述带鱼蛋白水解肽调pH为7.0,按体积的2%加入1 mol/L氯化亚铁(加入少量VC作保护剂)、氯化镁、氯化锌、氯化钙,于30 ℃水浴振荡合成30 min,以10 000 r/min离心20 min,除去上层油膜和下层沉淀,所得上清液即为蛋白水解肽-金属元素配合物,简称铁肽、镁肽、锌肽、钙肽(PH-Fe2+、PH-Mg2+、PH-Zn2+、PH-Ca2+)。螯合条件由试验探究优化得出。
1.5 蛋白水解肽-金属元素配合物的膜分级
在0.35 MPa压力下,用透过分子量为3 kDa的超滤膜超滤,得到4种分子量小于3 kDa的带鱼蛋白-金属配合物滤出液,将未螯合带鱼蛋白酶解液、4种金属元素螯合的酶解液原液及分级的螯合肽段透过液经旋转蒸发浓缩、冷冻、干燥后备用。
1.6 金属元素螯合率的测定
亚铁螯合率=(亚铁离子总量-游离亚铁离子含量)/亚铁离子总量×100%,式中游离亚铁离子含量测定采用邻二氮菲法[5-6]测定。
钙螯合率=螯合钙含量/钙离子总量×100%,式中螯合钙含量的测定采用EDTA法[7-8]测定。
锌螯合率=螯合锌含量/锌离子总量×100%,式中螯合锌含量的测定采用EDTA法[9-10]测定。
镁螯合率=螯合镁含量/锌离子总量×100%,式中螯合镁含量的测定采用EDTA法[11]测定。
2 结果与分析
2.1 螯合温度对蛋白水解肽-金属配合物制备的影响
鳌合反应为吸热反应,因而螯合温度对水解肽-金属元素配合物螯合率有一定的影响,温度越高对反应越有利。若温度太低,则鳌合速度慢且收率低;若温度太高,容易破坏氨基酸及其鳌合物结构[12]。酶解液分别添加2%的1 mol/L氯化亚铁(加入少量VC作保护剂)、氯化锌、氯化钙、氯化镁,在pH 7.0条件下水浴恒温振荡60 min后,测定不同温度对螯合率的影响情况。如图1所示,4种金属螯合率随温度的升高先增加后降低,在30 ℃左右达到最大值;在此条件下,铁肽、锌肽、钙肽和镁肽的螯合率分别为67.7%,64.6%,55.4%和46.8%(p<0.05)。
2.2 螯合pH对蛋白水解肽-金属配合物制备的影响
溶液体系pH不同,鳌合反应完成的速度和效果也不同。在酸性条件下,溶液中的H+将与金属离子(亚铁离子、镁离子、锌离子、钙离子)竞争氨基酸提供的供电子基团而使螯合率降低;而在碱性条件下,金属离子(亚铁离子、镁离子、锌离子、钙离子)则会发生水解,以沉淀析出而使螯合率降低。酶解液分别添加2%的1 mol/L的氯化亚铁(加入少量VC作保护剂)、氯化锌、氯化钙、氯化镁,于30 ℃水浴恒温振荡60 min,测定不同pH对螯合率的影响。如图2所示,4种金属螯合率随pH的升高先增加后降低,在pH 7.0时达到最大值,此时铁肽、锌肽、钙肽和镁肽的螯合率分别为66.9%,62.5%,58.7%和41.2%(p<0.05)。
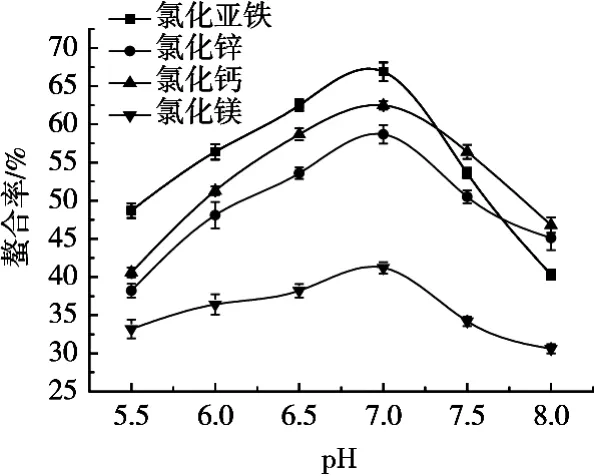
图2 pH对螯合率的影响
2.3 螯合时间对蛋白水解肽-金属配合物制备的影响
螯合时间对水解肽-金属元素配合物螯合率也有一定的影响,将酶解液调节pH 7.0,分别添加2%的1 mol/L的氯化亚铁(加入少量VC作保护剂)、氯化锌、氯化钙、氯化镁,于30 ℃水浴恒温振荡10,20,30,40和50 min,测定不同螯合时间对螯合率的影响。螯合时间对水解肽-金属元素配合物螯合率的影响,如图3所示。螯合率随螯合时间延长不断增大,当螯合时间为30 min左右时,4种金属配合物螯合率达到最大,最大螯合率分别为铁肽66.1%,锌肽64.6%,钙肽50.4%和镁肽43.2%;螯合时间继续增加,4种金属螯合率均不再增大(p>0.05)。
2.4 蛋白水解肽-金属元素配合物制备条件优化
为了进一步验证上述单因素试验的准确性,探究温度、pH及时间对4种水解肽-金属元素配合物螯合率影响程度大小,以螯合温度、螯合pH、螯合时间为影响因素,正交试验见表1和表2,其试验结果见表3。由表2可知,4种水解肽-金属元素配合物在相同试验条件下的螯合率各不相同,但它们的变化趋势是相同的。螯合率随温度和pH升高先增大后减小,均在30 ℃、pH 7.0达到最大螯合率;螯合率随螯合时间延长,开始时逐渐增大,然后在30 min左右达到平衡。4种水解肽-金属元素配合物均是在组合为A2B2C2的6号试验,即温度为30 ℃、pH为7.0、时间为30 min,具有最大螯合率,铁肽、锌肽、钙肽和镁肽螯合率分别为68.9%,65.7%,63.2%和42.3%。
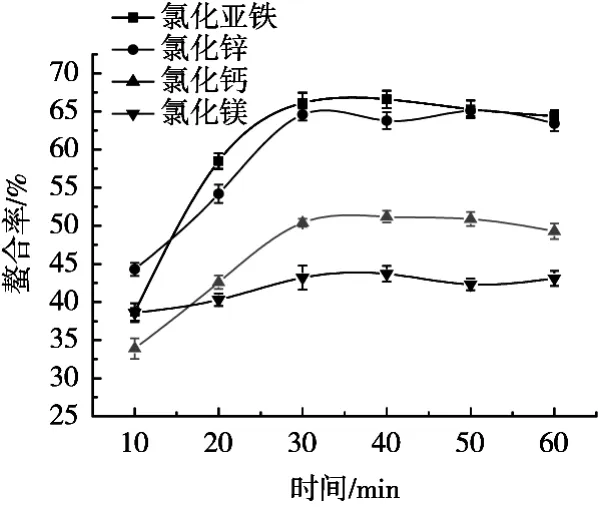
图3 时间对螯合率的影响

表1 因素与水平
进一步由方差分析(表3)可知,温度、pH和时间对4种水解肽-金属元素配合物螯合率的影响程度是不同的。铁肽和钙肽螯合率受pH影响最大,温度次之,受时间影响最小;但钙肽受pH、温度、时间影响程度的差别不大,而铁肽受pH、温度、时间影响程度的差别较大(p<0.05)。锌肽螯合率受pH影响最大,时间次之,受温度影响最小;pH的影响程度较显著,时间和温度影响程度的差别不显著(p>0.05)。镁肽受时间影响最大,温度次之,受pH影响最小,但三者影响程度的差别不显著(p>0.05)。
3 结论
试验探究木瓜蛋白酶酶解带鱼蛋白制得带鱼蛋白水解肽-金属配合物(铁肽、钙肽、镁肽和锌肽)最佳螯合工艺条件,得出以下试验结论:当金属元素添加量为2%时,带鱼蛋白水解肽-金属配合物(铁肽、钙肽、镁肽和锌肽)最佳螯合工艺条件为螯合时间30 min、pH 7.0、温度30 ℃,铁肽、钙肽、镁肽和锌肽最大螯合率分别为68.9%,63.2%,65.7%和42.3%。影响铁肽和钙肽螯合率的因素为:pH>温度>时间。影响锌肽肽螯合率的因素为:pH>时间>温度。影响镁肽螯合率的因素为:时间>温度>pH。

