超声引导肋下斜入路TAP对胃肠癌术后疼痛的影响
彭燕玲 郭尔萍 陈秋香
胃肠癌根治术后患者疼痛强烈、时间持续较长,易致肠梗阻、睡眠质量下降等。术后提供良好镇痛可有效减轻机体的应激反应,促进患者早日康复。静脉自控镇痛是目前最常见的镇痛方法,效果确切,但恶心、呕吐、呼吸抑制等不良反应时有发生。在多模式镇痛理念的引导下,越来越多的麻醉医生选择多种技术或药物联合的镇痛模式[1-2]。腹横肌平面(transversus abdominis plane,TAP)阻滞能够有效阻滞腹壁前侧的感觉神经,临床上镇痛效果满意[3]。侧路法和肋缘下法是目前最常用的TAP入路,均有局限性。前者仅适用于下腹部手术,而后者更适用于上腹部手术。本研究探讨超声引导下肋下斜入路TAP阻滞(同时阻滞上、下腹部的痛觉传入)用于腹腔镜胃肠癌根治术患者的镇痛效果。
1 资料与方法
1.1 一般资料
选择2018年2—10月择期行腹腔镜胃肠癌根治术患者60例,纳入标准:患者均无严重心脑肺肝肾疾病、神经精神疾病、有嗜酒及药物滥用史、局部麻醉药物过敏史等。随机分两组各30例,对照组(A组):术毕使用静脉患者自控镇痛(patient-controlled analgesia,PCA),男20例,女10例,年龄42~75岁,平均年龄(58.8±13.5)岁,胃癌16例,结肠癌14例,美国麻醉医师协会(American association of anesthesiologists,ASA)Ⅰ级15例、Ⅱ级10例、Ⅲ级5例;TAP组(B组):术毕实施TAP阻滞联合静脉PCA的多模式镇痛。男19例,女11例,年龄43~73岁,平均年龄(58.3±13.2)岁,胃癌14例,结肠癌16例,ASAⅠ级16例、Ⅱ级9例、Ⅲ级5例,均知情同意本研究,并经过医院伦理委员会批准。两组患者一般资料对比差异无统计学意义(P>0.05)。
1.2 方法
1.2.1 麻醉 两组常规术前准备,开放静脉通路,监测心率(HR)、血压(BP)、脉搏血氧饱和度(SpO2)、呼吸末CO2分压(ETCO2)。常规静注咪达唑仑0.05 mg·kg-1,舒芬太尼0.4 μg·kg-1,依托咪酯0.2 mg·kg-1,异丙酚 1 mg·kg-1,顺式阿曲库铵 0.15 mg·k-1麻醉诱导,气管插管行控制呼吸,ETCO2控制在35~45 mmHg,麻醉维持:泵注异丙酚 5 ~ 6 mg·kg-1·h-1、瑞芬太尼 0.15 ~ 0.2μg·kg-1·min-1、顺式阿曲库铵0.15~0.2 mg·kg-1·h-1,调整麻醉药用量及间断静脉注射舒芬太尼0.2 μg·kg-1。术毕停用麻药。A组不实施TAP阻滞,B组在患者清醒前,实施TAP阻滞,两组均待患者自主呼吸和意识恢复后拔除气管导管,生命体征平稳后开始PCA,其配方:舒芬太尼100 μg+地佐辛5 mg+格拉司琼3 mg,加生理盐水至100mL。参数设置:首次剂量2 mL,背景剂量2 mL/h,PCA泵1 mL/次,锁定时间30 min。
1.2.2 肋下斜入路腹横肌平面阻滞方法 仰卧位下麻醉医生行双侧TAP阻滞,于剑突位置斜行至同侧的髂嵴前部,T6~L1脊神经穿过阻滞区域,沿肋缘下两次进针多点推注药物。具体方法:将高频超声探头(6~13Hz)置于一侧肋缘下,找到腹横肌与腹直肌移行处,采用平面内技术插入22 G穿刺针至腹横肌与腹直肌之间,回吸无血液,将10 mL药物利用水分离技术逐渐向外推注并多点注入。拔出穿刺针,探头向外移至腋前线并清楚显示腹外斜肌、腹内斜肌、腹横肌后再次进针,采用相同技术将剩余10mL药物均匀推注于肋下斜入路TAP内,并使两处进针推注的药物连成一个平面,上至腹直肌内侧上极,下至髂嵴前部TAP内,每侧注入0.25%盐酸罗哌卡因20 mL。
1.3 观察指标
(1)两组苏醒期两个时间段:TAP阻滞前(T1)及TAP阻滞后(T2)的血流动力学:心率(heart rate,HR)、收缩压(systolic blood pressure,SBP)、舒张压(diastolic blood pressure,DBP);(2)安静及活动(翻身和蜷腿时)状态下两组患者术后2 h、6 h、12 h、24 h的疼痛视觉模拟评分(visual analogue scale,VAS)[4]:0分表示无痛,10分表示剧痛;(3)两组患者首次按压镇痛泵时间及镇痛泵按压次数;(4)术后24 h内镇痛泵舒芬太尼用量,及发生胸闷、呼吸抑制、恶心、呕吐等不良反应。
1.4 统计学分析
采用SPSS 19.0统计学软件。计量资料采用(均数±标准差)表示,组间比较采用t检验,计数资料采用(%)表示,组间对比采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 对比两组苏醒期的HR、SBP、DBP
所有患者手术顺利完成。两组苏醒期,T1时的HR、SBP、DBP无明显差异,A组T2时的HR、SBP、DBP比T1明显升高,差异有统计学意义(P<0.05),B组则变化差异无统计学意义(P>0.05),见表1。
2.2 对比两组术后不同时间的VAS评分
安静状态下,B组术后2 h、6 h、12 h、24 h的VAS评分低于A组,差异有统计学意义(P<0.05);活动状态下2 h、6 h、12 h、24 h的VAS评分均低于A组,差异有统计学意义(P<0.05),见表2。
2.3 对比两组患者首次按压镇痛泵时间及按压次数
B组首次按压时间明显长于A组、按压次数明显少于A组,两组间数据对比均差异有统计学意义(P<0.05),见表3。
2.4 对比两组患者舒芬太尼用量及不良反应
两组患者术后24 h内镇痛泵舒芬太尼用量A组为(68.0±10.4)μg、B组(54.0±8.8)μg,B组少于A组,差异有统计学意义(P<0.05);发生胸闷、呼吸抑制B组少于A组,差异有统计学意义(P<0.05),恶心、呕吐的发生率组间比较差异无统计学意义(P>0.05),见表4。
表1 两组患者不同时间点HR、SBP、SDP的变化(±s)

表1 两组患者不同时间点HR、SBP、SDP的变化(±s)
注:A组*P<0.05。
images/BZ_90_177_3017_2267_3151.pngA 组(n=30) 67.8±10.3 74.1±14.6* 127.2±19.4 136.6±18.3* 72.6±11.3 78.5±9.5*B 组(n=30) 67.5±10.5 70.5±12.3 130.1±20.6 131.2±17.8 75.2±14.3 75.4±15.1
3 讨论
胃肠癌根治术后疼痛可引起全身的应激反应,过度应激致患者出现一系列严重的并发症如心脑血管意外等,并延缓患者的恢复[5]。其疼痛主要表现为:内脏神经牵拉损伤致内脏痛、创伤造成炎症因子释放致炎性痛、腹部切口痛。切口痛属急性疼痛,术后24 h内疼痛明显,阻断切口痛觉传导显著减轻疼痛。腹部皮肤、肌肉、壁层腹膜的感觉神经主要由T6~L1神经前支控制,终末分支穿过侧腹壁,沿腹内斜肌和腹横肌之间的腹横肌平面分布,阻断该部位伤害性刺激从腹壁前侧感觉神经传入,有效防止外周和中枢敏化的形成,从而减轻腹部切口引起的疼痛[6],且不影响患者呼吸、循环和自主神经系统功能。随着超声引导技术的发展,TAP阻滞逐渐在临床上得以应用。Rafi在2001年首次提出了TAP阻滞[7],Finnerty等通过解剖证实了所以在腹横肌平面内注射局部麻醉药能阻断神经传导而提供有效镇痛[8]。故腹横肌平面注射局部麻醉药能有效阻滞神经传导,达到镇痛效果。目前普遍将髂嵴上方的侧路法TAP阻滞用于下腹部手术,将肋缘下TAP阻滞用于上腹部手术,均有其局限性。近来Mukherjee等[9]提出了一种新型改良入路即肋下斜入路TAP阻滞,既阻滞了上腹壁神经,也阻滞了大部分下腹壁神经,所以可用于上、下腹部的腹壁镇痛。TAP阻滞操作简单方便,不易导致交感阻滞和交感阻滞性低血压[10]。本研究TAP组苏醒期血流动力学更加平稳,降低心脑血管事件的发生。
表2 两组术后安静和活动状态下VAS评分比较(分,±s)
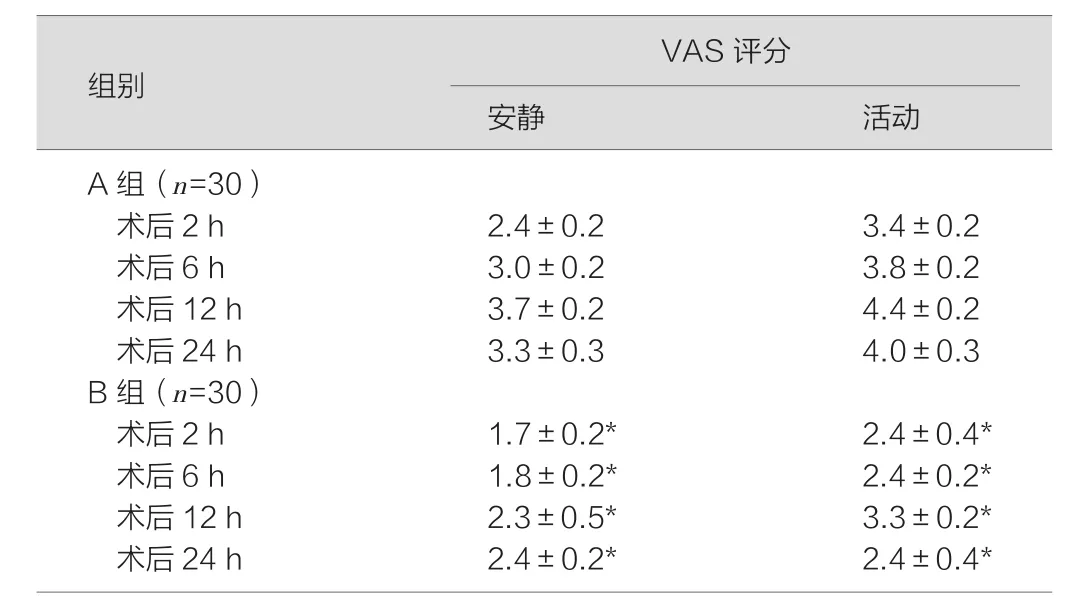
表2 两组术后安静和活动状态下VAS评分比较(分,±s)
注:与A组同时间点比较,*P<0.05。
images/BZ_91_213_414_1228_548.pngA组(n=30)术后2 h 2.4±0.2 3.4±0.2术后6 h 3.0±0.2 3.8±0.2术后12 h 3.7±0.2 4.4±0.2术后24 h 3.3±0.3 4.0±0.3 B组(n=30)术后 2 h 1.7±0.2* 2.4±0.4*术后 6 h 1.8±0.2* 2.4±0.2*术后 12 h 2.3±0.5* 3.3±0.2*术后 24 h 2.4±0.2* 2.4±0.4*
表3 两组患者首次按压镇痛泵时间及镇痛泵按压次数比较(±s)

表3 两组患者首次按压镇痛泵时间及镇痛泵按压次数比较(±s)
注:与A组比较,*P<0.05。
images/BZ_91_213_1193_1228_1251.pngA组 30 50.89±6.35 23.5±2.2 B 组 30 90.36±4.56* 7.5±1.6*
一般认为TAP阻滞是提供躯体镇痛,不提供内脏镇痛。但最近有研究认为TAP阻滞通过局麻药的椎旁扩散阻滞交感神经可对内脏疼痛产生影响[11]。本研究B组安静及活动状态下术后2 h、6 h、12 h、24 h的VAS评分均低于A组,说明TAP阻滞可以部分阻断壁层腹膜的疼痛;此外说明TAP没有大的血管和神经分布,使得注入的局部麻醉药可以长时间保持一定浓度和容量,维持持续的神经阻滞效果。且B组术后24h舒芬太尼的用量明显少于A组,呕吐两组发生率无统计学差异。
综上所述,超声引导双侧肋下斜入路TAP阻滞用于胃肠癌根治术后镇痛效果好,持续较长时间,减少了术后阿片类药物的用量,对患者全身影响小,有利于患者早期床边活动和体力恢复[12];与传统静脉镇痛相比患者术后镇痛效果更加完善,副作用有所减少该多模式镇痛对术后快速康复来说是有利的。

表4 两组患者术后胸闷、呼吸抑制、恶心、呕吐的发生率比较[例(%)]

