溶栓治疗急性心肌梗死的药物经济学研究
王雅楠 刘国恩,2* 黄润青 李子扬 盛亚楠 官海静
2017年,全球范围内约4110 万人死于慢性非传染性疾病(non-communicable diseases,NCDs),约占全部死亡人数的 73.4%,其中,心血管疾病(cardiovascular diseases,CVD)为NCDs 中造成死亡人数中最多的死因,占43.3%[1]。《中国心血管病报告(2017)》显示,CVD 为城乡居民死亡的首位原因,农村和城市CVD 死亡分别占居民疾病死亡构成的45.01%、42.61%,在中国CVD 发病率呈持续上升趋势,现患病人数约2.9 亿[2]。研究显示,心血管和循环系统疾病的疾病负担约为3 亿个伤残调整生命年(DALYs),约占全球疾病负担的11.8%,其中,缺血性心脏病的疾病负担最为严重,约为1.3 亿个DALYs,约占全球疾病负担的5.2%[3]。
急性ST 段抬高型心肌梗死(ST-segment elevation myocardial infarction,STEMI)是因心肌组织长时间缺血导致心肌细胞凋亡,主要由冠状动脉粥样硬化斑块破裂,引起血栓性阻塞所致,是冠状动脉粥样硬化性心脏病的主要类型[4]。临床常用治疗方案主要 包括溶栓治疗、经皮冠状动脉介入治疗(PCI)、冠状动脉旁路移植术(CABG)。相对于PCI 和CABG,尤其是在不具备PCI 条件的医院或从首次接触PCI明显延迟时,药物溶栓治疗快速方便,是临床上治疗STEMI 治疗的首选方案。
目前溶栓药物中,特异性纤溶酶原激酶是STEMI的诊断和治疗指南推荐优先选择的药物[4],包括注射用重组人组织型纤溶酶原激酶衍生物(通用名:瑞替普酶)和注射用重组人组织纤维蛋白溶酶原激活剂(通用名:阿替普酶)。本研究旨在基于真实世界数据,比较分析瑞替普酶与阿替普酶治疗STEMI 的成本-效果,为临床合理用药提供科学依据,也为优化医保目录和支付提供实证参考。
1 资料与方法
1.1 资料来源
从山东、山西、河北、黑龙江4 省16 家三甲医院回顾性收集STEMI 住院患者的相关信息。纳入标准:1)急性心肌梗死住院患者,年龄>18 岁,性别不限;2)使用瑞替普酶或阿替普酶进行溶栓治疗患者;3)就诊日期为2014年1月1日至2016年6月30日患者。排除标准:1)单次住院中使用两种或两种以上溶栓药物患者;2)合并恶性肿瘤、肝功能衰竭等严重疾病患者;3)数据不完整患者。
1.2 方法
本研究的成本指标为患者因STEMI 单次住院的总费用,包括药品费、检查费、床位费、护理费等;效果指标包括住院期间溶栓是否再通、是否发生不良事件等。通过设计研究记录表,收集患者信息包括人口学资料(年龄、性别、民族等);患者入院后溶栓治疗前的基本情况(如病情危急程度、心电图ST 段抬高值等);患者接受溶栓治疗后情况(开始溶栓治疗时间、心电图ST 段回落情况等);住院费用;药物治疗效果及安全性等。
收集的数据为观察性数据,两组并未通过随机化实现基线可比,因此相关混杂因素可能对分析结果造成影响。本研究采用倾向值匹配方法(Propensity Score Matching,PSM)控制患者人口学特征、疾病基线情况等混杂因素,以期得到药物对临床和经济结果的净效益。
采用logit 模型计算倾向值得分,控制变量通过逐步回归,保留对分组有显著影响的自变量。在基础分析中,倾向性评分匹配法采用卡钳1∶1 匹配,并将卡钳值设置为0.05。在敏感性分析中,通过其他几种匹配方式来检验模型的稳健性,包括1∶4 近邻匹配、1∶1 近邻匹配、卡钳1∶4 近邻匹配、kernel核匹配,设置卡钳值为0.01。
对匹配后的样本,分析两组患者成本和效果差异。根据《中国药物经济学评价指南》,如果试验组相比对照组效果更好,成本更低,则为优势方案;如果试验组相比对照组效果更好,成本更高,需计算增量成本-效果比(ICER)[5]。并根据世界卫生组织(WHO)推荐的标准判断药物的经济性。
此外,采用单因素敏感性分析评价结果的稳健性。为了得到一个更加保守的估计,本研究主要考虑的因素包括降低瑞替普酶的溶栓再通率(-10%、-15%、-20%)、降低阿替普酶组的次均住院总成本(-10%、-20%、-30%)、增加阿替普酶的溶栓再通率(10%、15%、20%)。
2 结果
2.1 样本特征
本研究纳入分析患者787 例,其中,瑞替普酶组385 例,平均年龄为59.1 岁,男性占80.8%,63.9%患者为居民医保。阿替普酶组402 例,平均年龄为57.5 岁,男性占81.3%,50.0%患者为居民医保。纳入匹配的协变量包括年龄、性别、民族、参保类型、既往病史个数、入院时危急情况、治疗前肌钙蛋白是否正常、治疗前心电图ST 段抬高值。匹配前,两组民族、医保类别、既往疾病史个数以及入院时危急情况方面比较差异均有统计学意义(均P<0.05);匹配后,两组上述指标比较差异均无统计学意义。见表1。
2.2 两组效果和成本分析结果
分析结果显示,瑞替普酶组患者单次住院总成本比阿替普酶组少7 876 元(37 202 比45 078,P<0.05);而瑞替普酶组患者的溶栓再通率比阿替普酶组高11.83%(88.98%比77.15%,P<0.05),差异均有统计学意义。同时,两组患者不良事件发生率和发生数比较差异均无统计学意义(均P>0.05)。1∶4 近邻匹配、1∶1 近邻匹配、卡钳1∶4 匹配、kernel 匹配等的结果与卡钳1:1 匹配的结果相近。见表2。
2.3 敏感性分析
当瑞替普酶组的溶栓再通率降低10%、阿替普酶成本降低10%、阿替普酶组的溶栓再通率升高10%~15%时,均不影响瑞替普酶,为成本更低、效果更好的优势方案;当瑞替普酶组的溶栓再通率降低15%~20%、阿替普酶组的溶栓再通率升高20%时,阿替普酶组的效果变得更好,但成本更高。阿替普酶组每提高一个百分点溶栓再通率需额外多支付1286~5050 元。溶栓率不变,而阿替普酶组的成本降低20%~30%时,瑞替普酶组效果仍然更好,但费用上升,即每提高一个百分点溶栓再通率需分别额外多支付96~477 元。见表3。
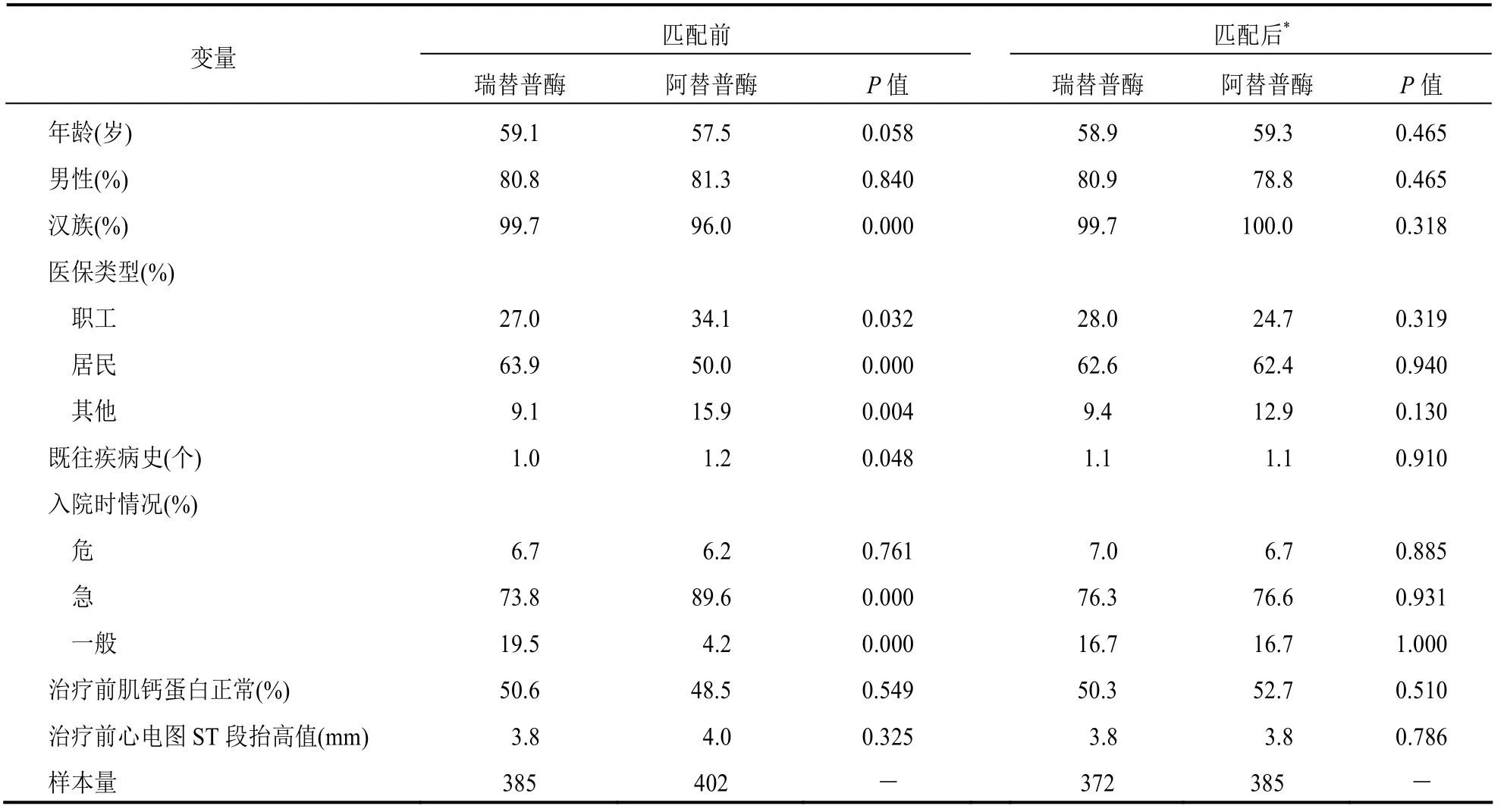
表1 两组匹配前后基线特征

表2 不同匹配方法匹配后的平均处理效应

表3 单因素敏感性分析
3 讨论
该研究基于中国4 省16 家三甲医院的真实世界数据,采用倾向性匹配方法,分析了单次住院期间瑞替普酶和阿替普酶治疗STEMI 的成本-效果。分析结果显示,瑞替普酶组的住院总成本比阿替普酶组低7 876 元,溶栓再通率比阿替普酶组高11.83%。根据溶栓再通率这一短期临床指标,瑞替普酶是成本更低、效果更好的优势方案。
目前,关于瑞替普酶与阿替普酶治疗STEMI 的临床及药物经济学研究较少。一项国际临床试验表明,瑞替普酶的溶栓再通率优于阿替普酶(出院时血管再通率分别为87.8%、70.7%)[6]。在成本效果研究方面,目前国内外尚无两种方案直接对比分析的的药物经济学文献发表。关于瑞替普酶与尿激酶的相比分析有一篇文献[7],其结果显示瑞替普酶的成本效果优于尿激酶。关于阿替普酶与其他药物治疗方案的经济性研究有4 篇,其中2 篇与重组人尿激酶原比较,阿替普酶不具有经济性[8-9];另外2 篇与尿激酶及链激酶同时比较,结果表明,阿替普酶也不具有经济性[10]。
从临床机制来看,瑞替普酶优于阿替普酶有一定基础。早期、快速和完全地开通梗死相关动脉是改善STEMI 患者预后的关键[11]。瑞替普酶在用药上采用的是两次静脉注射,两次间隔30 min,而阿替普酶在临床使用上则是采用90 min 加速给药法(首先静脉推注,随后持续静脉滴注90 min)。因此,相对于阿替普酶,瑞替普酶给药更快速方便,可缩短急救时间,从而降低潜在风险以及处置风险所需的资源费用。此外,瑞替普酶在2016年后药品价格下降了约6%,本研究数据采集期为2014—2016年。因此,本研究还有可能低估了瑞替普酶的成本效果优势。
该研究仍然存在一定局限性:1)该研究的样本相对较小,其代表性有限,需要在未来的研究中进一步核实完善。2)部分溶栓治疗前的临床指标缺失较多,如心肌酶检查结果、凝血检查结果等,主要由于这些指标并非所有医院在治疗前均会检查。3)在效果指标选择方面,STEMI 患者的治疗效果可依据肌钙蛋白、心肌酶或心电图ST 段抬高来判断,其中肌钙蛋白和心肌酶的特异性优于心电图,但由于在本数据收集中,有接近一半的样本在溶栓治疗后未进行以上几个指标的检查,因此,并未比较两组患者治疗后的肌钙蛋白和心肌酶水平。4)本研究基于患者单次住院的短期成本效果数据。两种方案的长期成本效果情况,有待进一步研究验证。

