川南地区乳腺癌患者HER-2基因状态及其蛋白表达与临床病理特征的关系分析*
李 昕,阮思蓓,唐晓琴,罗斯译,高子清,杨志惠,,肖秀丽,,刘 勇,,唐明希△
(1.西南医科大学,四川泸州 646000;2.西南医科大学附属医院病理科,四川泸州 646000)
人表皮生长因子受体-2(human epidermal growth factor receptor-2,HER-2)是定位于人染色体17q11.2~q12、编码Her-2/neu蛋白的基因,正确评估HER-2状态与判断乳腺癌的分子分型、生长、侵袭、转移及患者的治疗预后密切相关[1-2]。目前,使用最普遍的方法是荧光原位杂交(fluorescence in situ hybrizization,FISH)和免疫组织化学(immunohistochemistry,IHC)法。本文根据《乳腺癌HER-2检测指南(2014版)》再次评价FISH和IHC检测的一致性、相关性及与乳腺癌患者临床病理特征的关系,为临床正确评估HER-2状态提供参考。
1 资料与方法
1.1一般资料 收集2010年11月至2018年2月泸州、内江、宜宾、自贡等四川南部地区来西南医科大学附属医院病理科进行FISH和IHC检测的898例浸润性乳腺癌患者的石蜡标本。所有病理均有完整的IHC[雌激素受体(ER)、孕激素受体(PR)、Her-2/neu、Ki-67]及临床病理特征(患者年龄、肿瘤大小、淋巴结转移、肿瘤分级)资料,通过复阅切片及FISH报告分别统计新旧标准下FISH结果及其差异。
1.2试剂与探针 IHC中ER、PR和Her-2/neu检测使用罗氏公司抗体(ER克隆号:SP1;PR克隆号:1E2;Her-2/neu克隆号:4B5);Ki-67使用北京中杉金桥公司生物技术有限公司产品(克隆号:MIB.I)。FISH检测使用北京金普嘉公司HER-2基因扩增试剂盒。
1.3方法
1.3.1FISH法 FISH法按北京金普嘉公司HER-2基因扩增试剂盒说明书操作,参考文献[3]。
1.3.2IHC法 IHC采用EnVision法,ER、PR及HER-2蛋白表达如PANIWANI等[4]所述。
1.4结果判定
1.4.1FISH结果判定 参考ASCO-CAP检测指南[2]所建议的方法进行再评价:(1)浸润癌区域HER-2信号连接成簇状,判读为阳性;(2)随机计数20个浸润癌细胞的红绿双色信号数目。阳性:HER2/CEP17 Ratio≥2.0或者HER2/CEP17 Ratio<2.0,平均HER2拷贝数/细胞大于或等于6.0;阴性:HER2/CEP17 Ratio<2.0且平均HER2拷贝数/细胞小于4.0;可疑:HER2/CEP17 Ratio<2.0且平均HER2拷贝数/细胞≥4.0~<6.0;可疑状态的判定需要增加细胞计数或者另一位判读者单独计数细胞且结果一致。
1.4.2IHC结果判定 根据《乳腺癌HER-2检测指南(2014版)》[5]进行评价。
1.5统计学处理 使用SPSS19.0软件进行统计学分析,两种方法检测的一致性分析采用Kappa检验,HER-2基因状态及Her-2/neu蛋白表达与各临床病理特征关系分析的组间比较用秩和检验及Speaman等级相关分析,以P<0.05为差异具有统计学意义。
2 结 果
2.1IHC与FISH检测HER-2的结果比较 在898例浸润性乳腺癌病理标本中,IHC染色结果为-,+,++,+++(图1)。FISH新旧标准下与IHC检测结果的一致性见表1。新标准下,FISH检测HER-2基因扩增率为30.96%(278/898),可疑率为5.57%(50/898),阴性率为63.47%(570/898),见图2。FISH与IHC检测符合率如下:IHC(-/+)为93.79%(151/161),IHC(++)为7.17%(44/614),IHC(+++)为60.98%(75/123)。一致性检验显示FISH与IHC一致率为46.77%,结果存在一致性(Kappa=0.132,P=0.000)且呈正相关(r=0.351,P=0.000),见表1。
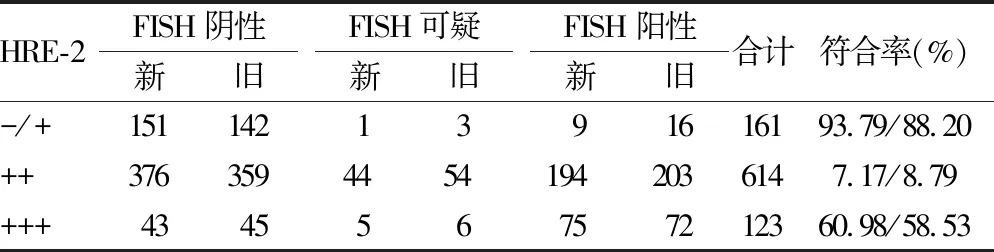
表1 FISH及IHC检测HER-2基因状态新旧标准比较
新:根据《乳腺癌HER2检测指南(2014版)》;旧:根据《乳腺癌HER2检测指南(2009版)》

A:IHC,-无染色(×200);B:IHC+,>10%的浸润癌细胞呈不完整的、微弱的细胞膜染色(×200);C:IHC++,>10%的浸润癌细胞呈不完整和中等强度的细胞膜染色(×200);D:IHC+++,>10%的浸润癌细胞呈现强而完整的细胞膜染色(×200)
图1 IHC评分结果图片
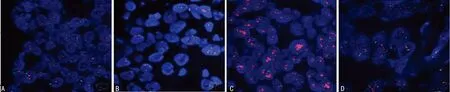
A:阴性;B:可疑;C、D:阳性
图2 FISH结果判读图片(CEP17为绿色信号,HER-2为红色信号)
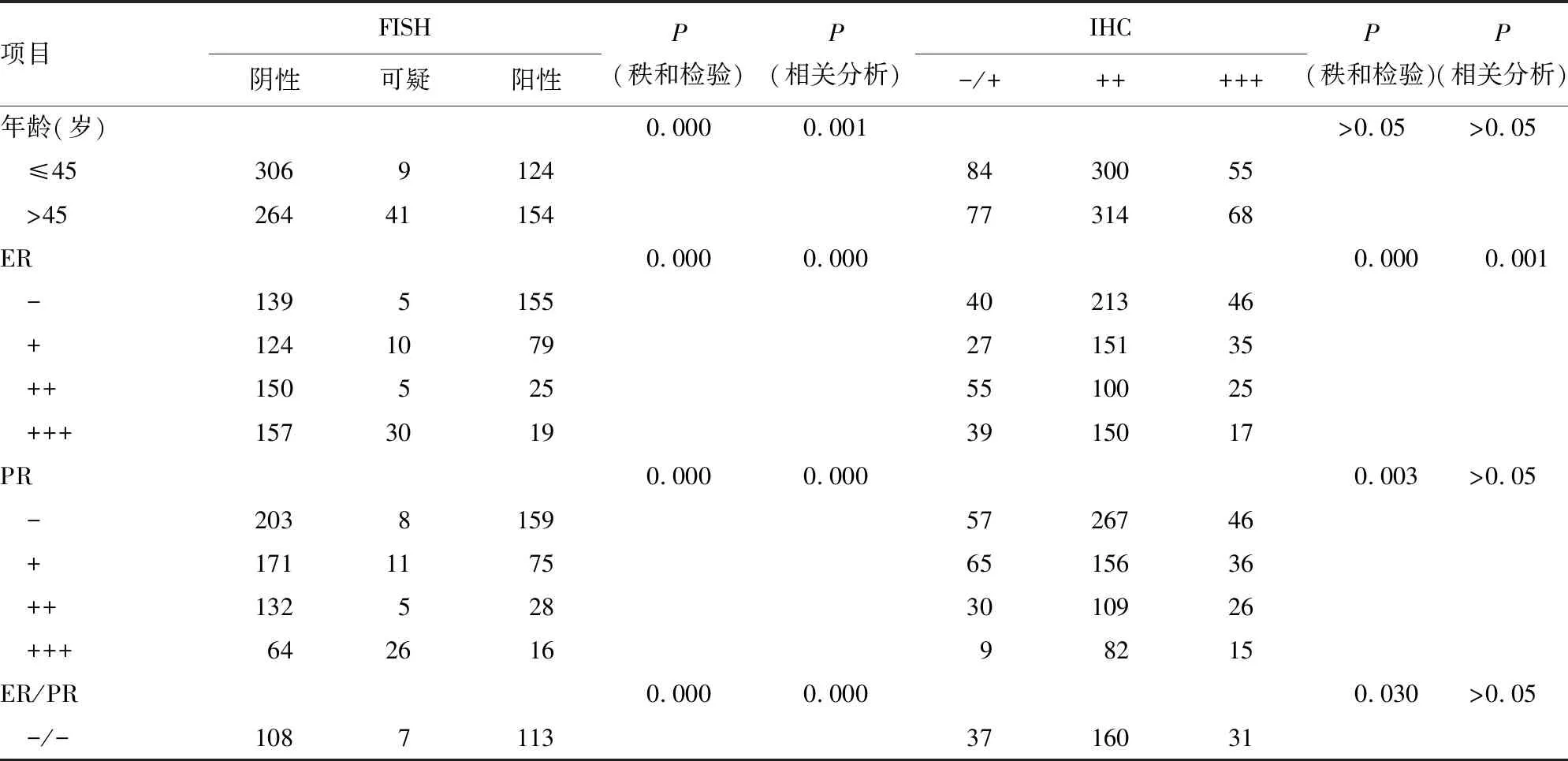
表2 Her-2/neu蛋白表达、HER-2基因状态与临床病理特征的相关性

续表2 Her-2/neu蛋白表达、HER-2基因状态与临床病理特征的相关性
2.2HER-2基因扩增及蛋白表达与临床病理特征的关系 ER、PR、ER/PR表达状态、肿瘤大小及组织学分级与HER-2基因扩增(χ2=164.939,P=0.000;χ2=127.342,P=0.000;χ2=65.146,P=0.000;χ2=30.711,P=0.001;χ2=17.786,P=0.001)及Her-2/neu蛋白表达间差异均有统计学意义(χ2=34.578,P=0.000;χ2=19.706,P<0.01;χ2=19.624,P<0.05;χ2=67.255,P=0.000;χ2=12.047,P<0.05),年龄和淋巴结转移状态与HER-2基因扩增间差异具有统计学意义(P<0.05),而与Her-2/neu蛋白表达间差异无统计学意义(P>0.05)。ER表达与HER-2基因扩增及蛋白表达呈负相关(r=-0.322,P<0.01;r=-0.114,P<0.01),PR表达及ER/PR状态与HER-2基因扩增呈负相关(r=-0.177,P<0.01;r=-0.234,P<0.01),与HER-2蛋白表达无关(P>0.05)。另外,年龄、淋巴结转移状态与HER-2基因扩增状态相关,而肿瘤大小和组织学分级与HER-2蛋白表达有关(表2)。
3 讨 论
乳腺癌患者的HER-2状态是临床筛选用药的重要指标。美国临床肿瘤学会/美国病理学家学会(ASCO/CAP)于2013年颁布了最新的乳腺癌HER-2检测指南,我国也同步采用新版《乳腺癌HER-2检测指南(2014版)》。本文运用该指南再次评价IHC及FISH检测结果的一致性、相关性及其与临床病理特征的关系。
HER-2基因扩增及其受体蛋白的过表达被认为与预后不良相关,乳腺癌患者HER-2状态的评价对其治疗和预后判断具有重要的指导作用[6-7]。本研究再次表明,新标准下FISH和IHC(-/+)的一致性为93.79%,与本文旧标准结果(88.20%)及本课题组之前报道的87.50%[3]和93.67%[8]基本一致,也与大多数报道相符[4,9-11]。新标准下的FISH和IHC(++)一致性为7.17%,低于本文旧标准判读结果的8.79%、STOSS等[12]报道的8.20%及MURTHY等[13]报道的16%~29%,说明FISH与IHC(++)一致性有所降低,提示IHC(++)者应常规行FISH检测,才能更准确地评估HER2扩增状态。新标准下,FISH和IHC(+++)检测一致性为60.98%,略高于之前报道的58.80%[3],但仍然明显低于其他研究者的报道100.00%[4,9]、84.80%[11]。这也是本文FISH与IHC总符合率(46.77%)较低的主要原因,可能与IHC(+++)样本量较少,以及样本固定、IHC抗原修复方法、17号染色体多体等因素有关。另外,新旧指南均将IHC(+++)作为HER-2扩增可直接行曲妥珠单抗治疗。但本研究结果表明,IHC(+++)仍有一定比例患者HER-2基因无扩增,基于MASS等[14]报道IHC(++)和(+++)患者中,HER-2基因扩增患者应用靶向药物治疗的总有效率及长期生存率显著高于无基因扩增患者,同时,许多临床及科研工作者也推荐FISH作为应用曲妥珠单抗治疗的金标准[2,5]。因此,笔者认为IHC(++)及(+++)者都应进一步行FISH检测,以此完善诊断,指导治疗和判断预后。最新指南首次考虑了平均HER-2基因拷贝数对结果评价的影响,提高了FISH与IHC检测的一致性,但是,临床上究竟以IHC检测HER-2/neu蛋白表达,还是以FISH检测HER-2基因扩增作为应用靶向药物的最终依据,以及17号染色体多体对乳腺癌患者治疗预后的影响,还有待长期、大量、多中心的临床治疗效果的判读、研究及分析来得以完善和解决。
本文结果显示ER表达与HER-2基因扩增及HER-2/neu蛋白表达呈负相关,PR表达、ER/PR状态与HER-2基因扩增呈负相关,这与NING等[11]及刘琪等[15]的结论基本一致。提示ER、PR表达与HER-2基因扩增间可能存在共同的信号转导通路,使其相互影响。因此,ER、PR和ER/PR状态可以间接推测HER-2基因扩增情况,且有报道ER- PR-患者预后较差[16],这可能与其HER-2基因扩增率高相关。此外,年龄和淋巴结转移状态与HER-2基因扩增呈正相关,肿瘤大小和组织学分级与HER-2蛋白表达呈正相关,这可能与HER-2基因扩增后调控肿瘤细胞增殖,使肿瘤体积增大、组织学分级增高、淋巴结出现转移有关,但与汪波等[16]报道的年龄和淋巴转移与HER-2基因扩增和Her-2/neu蛋白表达无关不同,其原因可能与不同的统计病例数等有关,其相关性仍需多中心、长期、大样本分析。
综上所述,IHC是检测乳腺癌患者HER-2/neu蛋白表达的首选方法。但是FISH仍然是评价HER-2/neu蛋白IHC(++)及IHC(+++)基因扩增的标准方法。最新HER-2检测指南提高了FISH和IHC检测的一致性,避免了部分假阴性及假可疑的存在。

