Al2O3-SiO2-CaO-FeO四元体系煤灰结构及流动性关系的实验和理论研究
代 鑫, 白 进, 李东涛, 袁 苹, 颜婷珪, 孔令学, 李 文
(1. 首钢技术研究院, 北京 100043;2. 绿色可循环钢铁流程北京市重点实验室, 北京 100043;3. 中国科学院山西煤炭化学研究所 煤转化国家重点实验室, 山西 太原 030001;4. 清华大学 山西清洁能源研究院, 山西 太原 030032;5. 贵州大学 化学与化工学院, 贵州 贵阳 550025)
煤炭是中国最为重要的化石能源,随着中国能源发展的战略需求和日益严苛的环境要求,发展煤炭清洁高效利用和转化技术也越来越受到关注,而以煤气化为核心的煤炭气化联合循环过程可有效提高煤炭使用效率,降低污染物排放。高温高压的气流床气化炉具有易大型化、煤种适应性广及碳转化率高等优势,已成为大规模气化的主要发展方向之一[1,2]。在高温条件下,不同煤中有机质反应性及速率的差异很小,此时煤中矿物质的流动性成为决定气化过程运行参数和稳定的关键[3]。
煤灰的流动性是表征煤灰在加热过程熔融状态变化的重要指标,对于煤气化操作温度的确定及稳定运行有重要意义[4]。煤灰的黏温特性是高温条件下灰渣黏度与温度的关系,是定量描述高温下煤灰流动性的重要参数,也是决定液态排渣气化炉操作温度的重要依据[5]。对于液态排渣的气流床气化炉,其灰渣的黏度在操作温度范围内应稳定保持在2-25 Pa·s;如果灰渣黏度过高,容易导致气化炉排渣不畅,排渣口易堵渣;反之,熔渣易侵蚀气化炉壁。此外,煤灰黏度在操作温度范围内波动过大也不利于气化炉的长期、稳定运行[6,7]。对于煤灰黏温特性的研究内容主要集中在其化学组成及外界因素的影响[8-10]。煤灰渣的化学组成中最为主要的成分为CaO、SiO2、Fe2O3和Al2O3等,为研究灰渣流动性的影响因素,通常将煤灰体系简化为CaO、SiO2、Fe2O3和Al2O3,大量的实验研究采用该方法研究了组分变化对其流动性影响规律[11],但对于其微观结构变化对流动性影响的研究尚不够深入[12-15]。
本研究利用分子动力学模拟的方法研究SiO2-Al2O3-CaO-FeO四元体系,主要讨论碱性组成对氧键结构和流动性的影响,研究发现,不同碱性组分破坏网格结构的能力不同,且同类化学键存在竞争作用,例如Ca-O和Al-O,因此,在四元体系中也可能存在Ca-O和Fe-O的竞争作用,因此,本研究主要从四元体系中的钙铁比(CaO/FeO, 简称C/F)出发,采用分子动力学计算、热力学计算和实验结合的方法来探索四元体系中碱性组分的作用机制及可能存在的协同和抑制作用对流动性的影响。
1 实验部分
1.1 样品的制备
本研究测定四元体系的流动性实验采用SiO2、Al2O3、CaO和Fe2O3四种氧化物进行配灰实验,所用的试剂均为百灵威试剂公司生产的分析纯试剂。为保证样品在实验过程中无烧失,首先将试剂进行灼烧,从室温至1123 K,恒温2 h,再升温至1823 K,恒温10 min,自然降温至室温。将焙烧后的样品研磨至200目以下,并按照表1进行混配,混配过程采用球磨机保证样品充分混合均匀。

表1 煤灰样品的组成
1.2 黏温特性测定
测定前需将粉状样品进行预熔,首先将装有样品的刚玉坩埚置于高温电炉中预熔以保证样品呈现均匀状态,并在高温电炉中放置足量的活性炭以保证预熔过程中样品处于还原性气氛;预熔温度比黏度测试的最高温度高80 K,并在该温度下恒温10 min,待样品自然冷却至室温后,破碎后取出样品用于黏温特性测定。采用程序降温法测定煤灰的黏温特性,测试气氛为弱还原气氛(CO∶CO2= 4∶6),降温速率为1 K/min[8]。
1.3 矿物质组成分析
Bruke-AXS D2型X射线分析仪(德国布鲁克公司)主要用于定性和定量分析不同温度下煤灰中的矿物质。仪器采用铜靶(40 kV, 40 mA),10°-90°扫描,扫描步长是0.02°。采用压片法制样,测试样品均研磨至200目以下,并采用布鲁克配套的物相分析软件EVA进行数据分析。
1.4 煤灰结构分析
Bruker AVANCE III 600 MHz型全数字化超导核磁共振波谱仪(德国布鲁克公司)主要用于煤灰中分析铝元素配位变化,仪器配有超屏蔽磁体,磁场强度为14.09 T,5 mm CPTCI三共振反式超低温探头,高分辨BBO正相观察宽带探头,4 mm的布鲁克魔角自旋探头。采用单脉冲程序测试均匀装入直径为4 mm的氧化锆转子中的样品,自旋速率为14 kHz,27Al的化学位移以0.0处的Al(NO3)3为参考。
2 模拟计算
2.1 模拟方法
分子动力学模拟采用LAMMPS (https://lammps. sandia. gov/)。模拟过程如下:将初始的模型在NPT(恒温恒压)系综下升温至3000 K并平衡200 ps以达到热力学平衡,然后以10 K/ps的降温速率降温至300 K,并在NVT(正则)系综下,平衡200 ps,然后在NPT系综下将所得模型以1 K/s的升温速率由300 K升温至2000 K;不同系综下均采用Nose-Hoover方法控制温度及压力,采用Ewald方法计算静电相互作用力,长程作用力及短程作用力的截断半径分别为1.2 nm和0.8 nm;分子动力学模拟采用BMH势函数,势函数参数详见表2[16,17]。
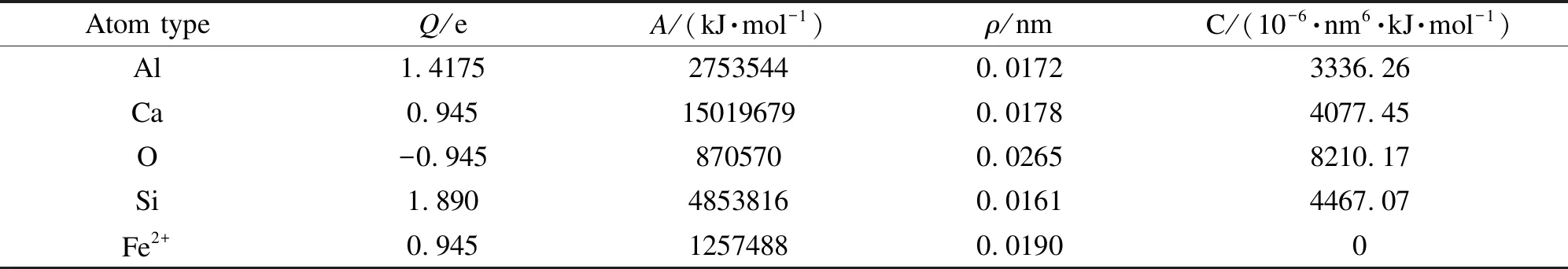
表2 Bertrand等拟合的适合不同四元体系势函数参数[16,17]
2.2 热力学计算
本研究主要利用FactSage中的Equilib和Phase Diagram模块计算多元煤灰组成体系在不同温度下组成变化情况[18-20]。针对研究的研究内容,主要选取纯物质数据库(FactPS)和氧化物数据库(FToxid)。这两个数据库基本包括了煤灰组成(SiO2、Al2O3、CaO、FeO、Fe2O3、MgO、Na2O、K2O 及TiO2)的相关体系的热力学性质数据,可满足灰渣结构和流动性相关的研究[21]。
3 结果与讨论
3.1 钙铁比对煤灰黏温特性的影响
图1为Al2O3-SiO2-FeO-CaO四元体系中钙铁比对黏度的影响。由图1可知,Al2O3-SiO2-FeO-CaO四元体系(体系硅铝比均为2)中所选五组样品(R4-R8)的黏度随着钙铁比的增加而减少,临界黏度温度随钙铁比的增加而降低。样品的临界黏度温度依次为1826、1811、1772、1767和1762 K。体系的黏度取决于体系的结构,当体系温度高于临界黏度温度时,不同样品的体系结构差异较小,温度对结构和黏度的影响均不显著,当体系温度升高,体系结构被进一步破坏导致黏度小幅降低;当体系的温度低于临界黏度温度时,从宏观角度分析体系形成固液两相,从微观角度分析体系结构随温度发生显著变化,温度变化对结构改变的程度决定了体系黏度变化幅度。随体系的钙铁比增加,结构对温度的敏感程度增加,温度降低导致黏度数值增加幅度显著增大,从宏观性质来看,样品的黏温曲线类型由结晶渣变为玻璃渣。样品R4(C/F=0.66)和R5(C/F=1.14)的黏温曲线存在明显拐点,温度降低到1833和1813 K时体系的黏度急剧增加;样品R7(C/F=4.00)和R8(C/F=14.00)的黏温曲线无明显拐点,体系黏度随温度降低而平缓增加;样品R6(C/F=2.00)的黏度受温度影响程度介于以上两种情况之间,黏度平稳增加和快速增加范围存在一个过渡段。

图 1 Al2O3-SiO2-FeO-CaO四元体系中钙铁比对黏度的影响Figure 1 Viscosity variation for Al2O3-SiO2-FeO-CaO quaternary system as a function of calcium oxide and ferrous oxide ratio
利用热力学软件FactSage中的Equilib模块计算得到不同温度下五组样品的固液相组成,如图2所示,当温度低于全液相温度时,样品R4(C/F=0.66)在1862 K析出第一个固相莫来石,在1599 K析出第二个固相石英,两者析出温度差距较大。随体系钙铁比的增加,首个析出固相莫来石含量逐渐减少,体系中无定形结构增加;当体系的钙铁比为14时,首个析出固相矿物质为熔点温度较低的钙长石,且固相含量降低,这时体系黏度受温度的影响程度降低,黏温曲线发生变化,灰渣类型由结晶渣转变为玻璃渣。

图 2 Al2O3-SiO2-FeO-CaO四元体系不同钙铁比样品黏温曲线及不同温度下的固液相组成
通过XRD分析黏度测试后灰渣的物相组成,具体见图3。当钙铁比大于2时,XRD谱图中几乎无晶体衍射峰,说明样品主要为无定形矿物质,体系的结晶趋势较弱,体系的黏温曲线为玻璃渣类型;当钙铁比小于2时,体系的莫来石晶体含量较高,样品结晶趋势明显,因此,体系的黏温曲线呈现结晶渣类型。当钙铁比等于2时,体系中含有少量莫来石晶体和无定形矿物质,此时体系的黏温曲线类型呈现塑性渣类型。

图 3 Al2O3-SiO2-FeO-CaO四元体系中不同钙铁比样品黏度测试后灰渣的XRD谱图
3.2 钙铁比对四元体系结构的影响
体系的结构对黏度具有决定性作用,为从微观角度认识钙铁比对煤灰结构及黏度的影响,本部分将实验表征与分子动力学模拟方法相结合研究钙铁比对灰渣结构的影响。
Al 2p的XPS能谱结果分析体系中Al离子配位的变化,将XPS谱图分峰拟合对Al的配位情况进行半定量分析,图4(a)是不同钙铁比煤灰的XPS能谱结果,图4(b)为XPS能谱分峰结果,图4(c)为对不同XPS图谱分峰结果汇总。当钙铁比小于2时,钙铁比增加导致体系中六配位[AlO6]9-含量由75%降低至60%,四配位[AlO4]5-含量由25%增加至40%;此时,钙铁之间的竞争作用明显,主要体现Ca和Fe对Al配位情况的改变,进而影响Ca-O和Fe-O稳定性;而当钙铁比大于2时,钙铁比增加对体系中Al的六配位及四配位含量几乎无影响,说明此时钙铁比变化几乎不改变体系的结构,这也解释了降温过程中体系黏度增加幅度的差别是钙铁比对结构影响不同导致的。

图 4 Al2O3-SiO2-FeO-CaO四元体系中不同钙铁比样品的XPS谱图Figure 4 XPS analysis for various C/F Al2O3-SiO2-FeO-CaO quaternary systems: [AlO4]5-; : [AlO6]9-
通过27Al的固体核磁对体相中Al的配位情况进行定性分析,如图5所示。27Al的固体核磁结果化学位移(δ)处于50附近说明四配位Al存在,化学位移为0附近属于六配位的Al。随着钙铁比增加,化学位移为50附近的峰逐渐增强,化学位移为0附近逐渐减弱,说明钙铁比增加导致体系中的部分铝由六配位向四配位转变,这与XPS结果一致。
利用分子动力学计算可进一步从四元体系的氧键类型分析钙铁比对黏度的影响。图6为Al2O3-SiO2-FeO-CaO四元体系中不同钙铁比样品的氧键含量。由图6可知,所研究的四元体系中氧键主要是桥氧和非桥氧,而团簇氧的含量较少。当钙铁比小于2时,体系中桥氧和非桥氧含量相差不大,R4(C/F=0.66)和R5(C/F=1.14)的体系结构类型相似;当钙铁比大于2时,体系中非桥氧含量增加,桥氧含量降低。钙铁比为2是体系氧键变化的分界点,钙铁比小于2,体系稳定性较高,宏观上表现为结晶渣,而当钙铁比大于2,体系稳定性较低,宏观上表现为玻璃渣。

图 5 Al2O3-SiO2-FeO-CaO四元体系中不同钙铁比样品的NMR谱图

图 6 Al2O3-SiO2-FeO-CaO四元体系中不同钙铁比样品的氧键含量
图7为不同钙铁比的Al2O3-SiO2-FeO-CaO四元体系桥氧和非桥氧组成。由图7可知,在Al2O3-SiO2-FeO-CaO四元体系中桥氧包括Al-O-Al、Al-O-Si和Si-O-Si三种类型,非桥氧中包括Al-O和Si-O两种类型。随着钙铁比增加,桥氧中Al-O-Si含量减少,而Al-O-Al含量增加,非桥氧中Al-O含量增加,Si-O含量减少。这与宏观上Al配位变化情况一致,Al-O-Si和Si-O-Si稳定性高于Al-O-Al,Al-O-Si含量降低,因此,体系的稳定性降低,黏度降低。

图 7 不同钙铁比的Al2O3-SiO2-FeO-CaO四元体系桥氧和非桥氧组成
3.3 Al2O3-SiO2-FeO-CaO四元体系流动性的预测
在硅酸盐体系中,团簇氧和桥氧均可提高体系的稳定性,因此,定义体系的稳定性系数(Stability Coefficient, SC)如下:
SC=BO +μTO
(1)
μ=(BO+TO)/(NBO+TO)
(2)
式中,μ指的是聚合程度系数,BO、TO、NBO分别指的是体系的桥氧、团簇氧和非桥氧的含量。体系的聚合程度越高,稳定性越高,则黏度越大;反之,则黏度越小。通过氧键为桥梁,建立了稳定性系数与煤灰黏度间的定量函数关系。图8为Al2O3-SiO2-CaO-FeO四元体系的黏度与稳定性系数的关系。由图8可知,尝试将Al2O3-SiO2-FeO-CaO四元体系的稳定性系数与黏度数值进行拟合,获得如下函数关系:
η=e0.041×SC
(3)
式中,η指的是体系的黏度,单位为Pa·s,SC指的是体系的稳定性系数。

图 8 Al2O3-SiO2-CaO-FeO四元体系的黏度与稳定性系数的关系
此外,钙铁比与体系中氧化钙含量变化趋势一致,体系的稳定性系数与氧化钙含量存在如下函数关系,具体见图9。
SC=-1.68×CaO+99.20
(4)
式中,SC为体系的稳定性系数,CaO为体系中氧化钙的含量,单位为%。
将上述两个函数关系联立并整理可得到体系的黏度和钙铁比间的定量关系如下:
lnη=4.07-0.069×CaO
(5)
式中,η指的是体系的黏度,单位为Pa·s, CaO指体系中氧化钙的含量,单位为%。

图 9 Al2O3-SiO2-CaO-FeO四元体系的稳定性系数与钙铁比的关系
4 结 论
在Al2O3-SiO2-CaO-FeO四元体系中,钙铁比增加,黏度下降,黏温曲线类型由结晶渣转变为玻璃渣,钙铁比为2时为黏温特性转变的拐点。
当钙铁比小于2时,体系降温过程中生成晶体矿物较多,当钙铁比大于2时,体系以无定形矿物质为主;从微观角度分析,钙铁比增加导致体系中Al由六配位([AlO6]9-)转变为四配位([AlO4]5-),钙铁两种原子对体系中六配位铝的影响存在竞争作用。同时,体系中的桥氧含量降低,导致体系的聚合程度和稳定性降低。
通过四元体系的氧键为桥梁,建立了碱性组分(CaO)含量与黏度的函数关系,即lnη=4.07-0.069×CaO。

