“关-开”型碳量子点荧光探针测定左旋多巴的研究
马红燕, 武文波, 张越诚, 田 锐, 张会芳
(延安大学化学与化工学院,延安市分析技术与检测重点实验室,陕西延安 716000)
碳量子点(CQDs)是一种新型的碳纳米功能材料,尺寸一般为1~10 nm,其具有生物毒性低、荧光稳定、水溶性好、容易制备和生物相容性好等优点[1]。目前CQDs的制备主要以人工制备的含碳化合物为原料,其制备过程繁琐,反应条件苛刻[2]。近年来,一些利用天然生物物质,如枫树叶[3]、枸杞[4]为原料制备CQDs的方法被相继报道。
左旋多巴(Levodopa,LDOPA)是一种抗震颤麻痹类物质,其经过血脑屏障进入中枢,经多脱羧酶变成多巴胺后产生作用,可用于治疗帕金森综合症[5]。现已报道测定LDOPA的方法,主要有薄层色谱法[6]、毛细管电泳法[7]、高效液相色谱法[8]、电化学发光法[9]和分光光度法[10 - 11]等。这些方法有的仪器设备昂贵,有的操作过程繁琐,有的线性范围窄、检出限高。因此,进行LDOPA灵敏、准确、快速测定新方法的研究显得尤为必要。
实验发现,选用淀粉为碳源,通过一步水热法可合成强荧光的CQDs。在研究淀粉CQDs发光性能的过程中,发现KMnO4的加入可使CQDs的荧光猝灭,荧光信号“关闭”;当继续加入LDOPA后,CQDs的荧光恢复为“打开”状态,可构建“关-开”型荧光探针,据此提出了基于CQDs荧光探针测定LDOPA的新方法。该方法成本低廉、灵敏度高、检出限低。该研究为LDOPA的检测提供了新方法,同时也拓展了CQDs的应用范围。
1 实验部分
1.1 仪器与试剂
FLSP920型瞬态稳态荧光光谱仪(英国,爱丁堡);F-4500型荧光分光光度计(日本,日立);IR Prestige-21型傅里叶变换红外光谱仪(日本,岛津);8453型紫外-可见分光光度计(美国,安捷伦)。
LDOPA溶液:准确称取0.0237 g LDOPA对照品(中国药品生物制品检定所),用10.0 mL 1.0 mol/L的HCl溶解后,以水定容到100 mL,浓度1.0×10-3mol/L,使用时逐级稀释。KMnO4溶液:1.0×10-3mol/L。所用其它试剂均为分析纯,实验用水为超纯水。
1.2 实验方法
1.2.1 CQDs的合成称取8.00 g淀粉于25 mL聚四氟乙烯反应釜中,再加3.0 mL乙二胺、10.0 mL超纯水后,于180 ℃恒温加热18 h,将反应釜自然冷却至室温,得深棕色溶液,经滤纸粗过滤后,再用孔径为0.22 μm微孔滤膜过滤,滤液定容至100 mL容量瓶中,稀释100倍后使用。
1.2.2 LDOPA的测定依次移取1.0 mL CQDs溶液,2.0 mL KMnO4溶液,2.0 mL 1.0 mol/L HCl,适量LDOPA 溶液于10 mL比色管中,用水稀释至刻度,摇匀。60 ℃恒温水浴加热30 min,流水冷却5 min,于荧光分光光度计上,在λex/λem=397/452 nm处测定体系的荧光强度F和试剂空白的荧光强度F0,其中光谱狭缝均为5.0 nm,并计算体系荧光强度变化ΔF(ΔF=F-F0)。
2 结果与讨论
2.1 CQDs光学性质分析
2.1.1 CQDs的荧光光谱图1为不同激发波长下CQDs的荧光光谱,由图可知该CQDs的发射峰强度和位置具有激发波长依赖性。当激发波长由380 nm增加到420 nm,发射波长由442 nm红移至483 nm,荧光强度先增大后减小,当激发波长为397 nm时,发射波长为452 nm,荧光强度达到最大。
2.1.2 CQDs的红外光谱CQDs的红外光谱图如图2所示,2 930 cm-1处可能是-CH2的特征吸收峰,2 360 cm-1处的吸收亦或是-C≡C、-CN等的伸缩振动,2 000 cm-1为R′-C≡C-R的吸收峰。1 648 cm-1可能为-C=O的特征吸收峰,1 558 cm-1处的吸收峰可能为-C=C-的伸缩振动。1 210 cm-1可能是C-OH的吸收峰也可能是酚的吸收峰。1 080 cm-1为C-N的伸缩振动吸收,而876 cm-1附近也有吸收峰,可能为C-C键骨架振动。由此分析得,该CQDs表面含有-OH、-C=O、-COOH等亲水性基团,因此,CQDs具有良好的水溶性。

图1 不同激发波长下CQDs的荧光光谱图Fig.1 Fluorescence spectra of CQDs with different excitation wavelengths
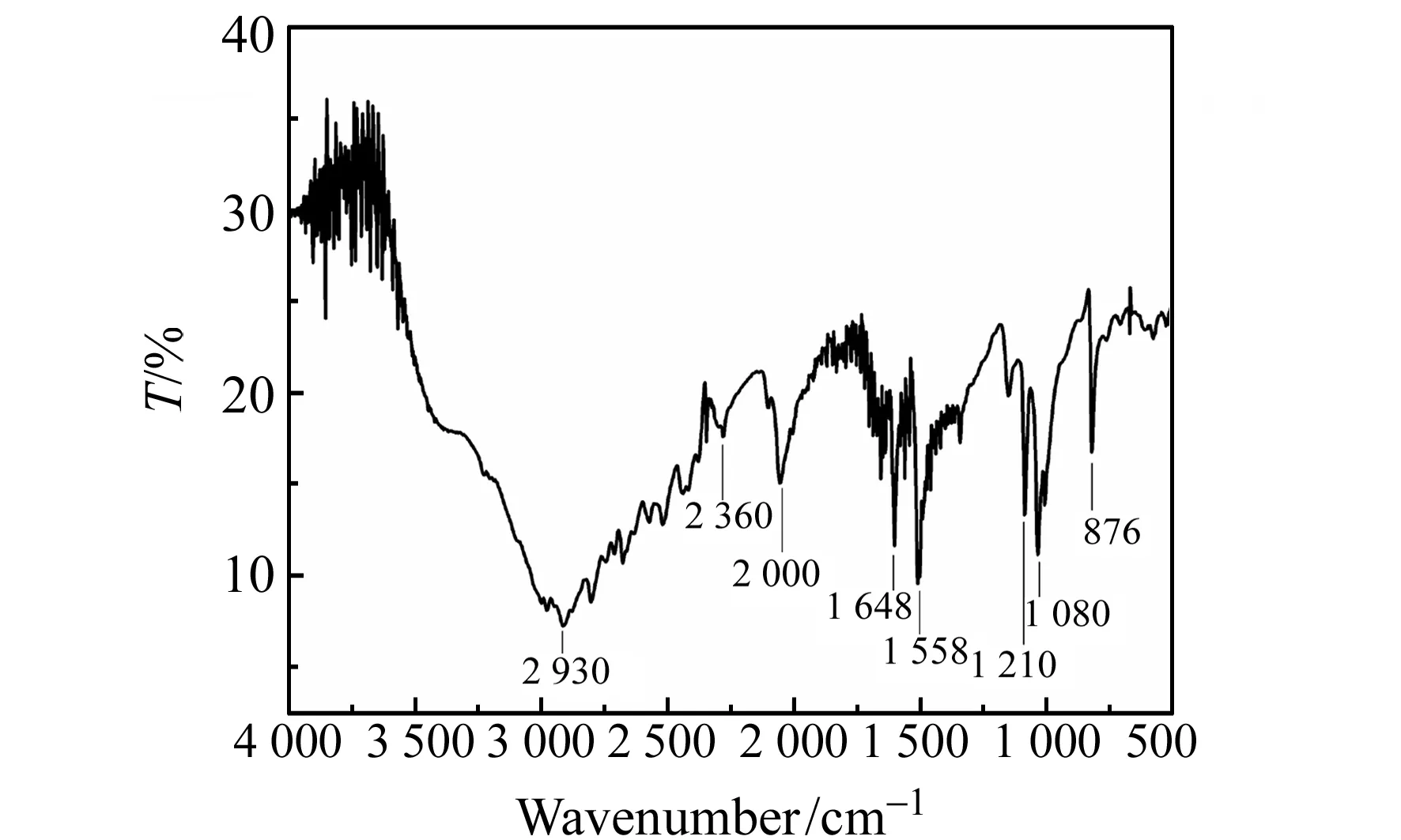
图2 CQDs的傅里叶变换红外(FT-IR)光谱图Fig.2 The FT-IR spectrum of CQDs

图3 CQDs的紫外-可见(UV-Vis)吸收光谱Fig.3 UV-Vis absorption spectrum of CQDs
2.1.3 CQDs的紫外-可见吸收光谱图3为CQDs的紫外-可见吸收光谱图,CQDs在282 nm波长处有一中等强度的吸收峰,在353 nm处有一较强的吸收峰,此为CQDs典型的紫外-可见吸收峰,其归因于共轭碳碳双键的π-π*跃迁所形成[12]。
2.1.4 CQDs的荧光寿命和量子产率通过瞬态稳态荧光光谱仪对CQDs的荧光寿命进行测定,其加权平均荧光寿命[13]为7.26 ns。采用参比法,以硫酸奎宁为标准物质[14],测得CQDs的荧光量子产率为10%。
2.1.5 CQDs“关-开”型荧光探针的构建室温下,扫描体系在激发波长λex=397 nm下的荧光光谱,如图4(A)所示。KMnO4的加入对CQDs的荧光有明显的猝灭作用,使其荧光信号“关闭”;LDOPA加入后,CQDs荧光恢复,荧光信号“打开”。在该激发波长下,LDOPA无明显荧光,LDOPA与KMnO4的产物也无明显荧光,LDOPA对CQDs的荧光也没有直接的猝灭作用,故对实验结果不会造成影响。由图4(B)可知,CQDs的荧光信号恢复值随着LDOPA浓度的增加有规律的增加,据此可用于LDOPA的测定。

图4 (A)可行性实验;(B)随左旋多巴浓度增加荧光信号恢复图Fig.4 (A) Feasibility of experiment;(B) Fluorescent signal recovery with increasing levodopa concentration
2.2 实验条件优化
2.2.1 酸度的影响研究了酸度对体系ΔF的影响,结果表明在2.0 mL 1.0 mol/L HCl中,体系荧光恢复值ΔF最大且稳定。
2.2.2 CQDs用量的选择试验了0.5~5.0 mL CQDs溶液对ΔF的影响,结果表明CQDs溶液的用量为1.0 mL时,体系的ΔF达到最大值。
2.2.3 KMnO4用量的选择KMnO4的浓度会直接影响检测LDOPA的背景值和线性范围。实验研究发现,KMnO4的用量少,CQDs猝灭效率低,荧光背景高,LDOPA检测的线性范围窄。而随着KMnO4浓度的增加,CQDs的猝灭作用加强。但是KMnO4浓度不能过大,若KMnO4浓度过大,加入的LDOPA会首先与游离的KMnO4反应,会降低LDOPA的有效浓度,影响荧光恢复效率。综合考虑,实验选择加入2.0 mL 1.0×10-3mol/L KMnO4溶液。
2.2.4 温度、加热时间和稳定性实验CQDs与KMnO4混合后,CQDs荧光猝灭信号至少在12 h内保持稳定。相比于CQDs-KMnO4体系的稳定性,LDOPA加入后,CQDs-KMnO4-LDOPA体系信号的“打开”在常温下进行的比较缓慢,故采用加热来加快反应速率。分别研究了不同加热时间、不同温度对ΔF的影响,结果表明在60 ℃恒温水浴中加热30 min后,荧光恢复程度达到最大。
2.3 共存物质的影响
在选定的实验条件下,研究了常见共存物对1.5×10-5mol/L LDOPA溶液测定结果的影响。相对误差控制在±5%范围内,1 000倍的Ca2+、Mg2+、K+、Al3+、Ba2+、Zn2+、D -果糖、蔗糖、糊精、淀粉,500倍的葡萄糖、Ag+,50倍的Cu2+不干扰测定。可见该方法具有较好的选择性。
2.4 线性范围、检出限和精密度
在优化的条件下,测定LDOPA浓度与ΔF之间的关系。结果表明,当LDOPA浓度在1.0×10-7~1.5×10-5mol/L范围内时,荧光强度恢复值与其浓度呈良好的线性关系,线性回归方程为:ΔF=2.2×107c+29.30,相关系数r为0.9980,该方法的检出限(3σ/k)为4.5×10-8mol/L。对浓度为1.5×10-5mol/L的LDOPA标准溶液平行测定5次,其相对标准偏差为1.3%。
2.5 样品测定
随机抽取同一批号的LDOPA药片10片,准确称取适量研磨后的粉末(相当于0.0237 g LDOPA)用10.0 mL 1.0 mol/L HCl溶解,超声10 min后移至100 mL的容量瓶中,以水定容,摇匀后静置10 min,将其过滤,弃去初滤液,移取一定量续滤液,按照实验方法测定,同时进行加标回收实验,结果见表1。其中样品1购于北京曙光药业有限责任公司,产品批号:161201,规格:250 mg;样品2购自湖南恒伟药业股份有限公司,产品批号:湘01070005,规格:250 mg。

表1 样品测定结果及回收率实验(n=5)
2.6 反应机理初探
将KMnO4溶液加入到CQDs后,CQDs的荧光发生强烈猝灭,体系荧光信号“关闭”;再将LDOPA加入上述CQDs-KMnO4体系中后,CQDs荧光得到恢复,体系的荧光信号呈“打开”状态。推测其机理如下:KMnO4具有强的氧化性,当KMnO4加到CQDs溶液中后,KMnO4通过与CQDs表面基团的作用而结合于CQDs表面,即KMnO4通过电子转移的方式占据CQDs表面,使CQDs的表面激发态以一种非辐射电子转移方式释放其能量,CQDs的荧光猝灭,使得荧光信号“关”。当LDOPA加入到CQDs-KMnO4体系中后,由于LDOPA强的还原性,更易于与KMnO4作用,把KMnO4从CQDs表面移除下来,荧光信号“开”,使CQDs的荧光得到恢复,其可能机理如图5所示。
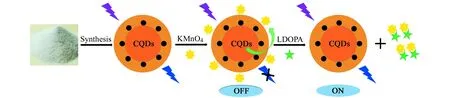
图5 CQDs的荧光“关-开”机理图Fig.5 The mechanism of CQDs quenching and fluorescence recover
3 结论
通过一步水热法合成了CQDs并对其发光性能进行了研究。在HCl介质中,基于LDOPA对被KMnO4已猝灭的CQDs的荧光有恢复作用,建立了高灵敏度“关-开”型荧光探针对LDOPA定量检测的荧光分析新方法。该研究拓展了CQDs在药物荧光分析中的应用范围,为临床测定LDOPA提供了新方法。

