马鞭草的化学成分研究
马金华,杨勇勋
(1.西昌学院资源与环境科学学院,四川 西昌 615000 2.西昌学院动物科学学院,四川 西昌 615000)
马鞭草科马鞭草属植物在全世界约有250 种,除2 -3 种产东半球外,全部产于热带至温带美洲;我国仅有一野生种,即马鞭草Verbena officinalis L.[1]. 马鞭草,又名铁马鞭、马鞭稍,在我国作为一种传统中药与民族药应用.本品性味苦、凉,具活血散瘀、解毒、利水、退黄、截疟的功效,用于治疗癥瘕积聚、痛经经闭、喉痹、痈肿、水肿、黄疸、疟疾[2].此外,马鞭草还是一味世界传统药物,并被收载入多国药典,如收载入英国草药典.马鞭草在欧洲一些国家作为一种促进睡眠、抗焦虑的药物使用,并且在前期的研究中揭示马鞭草水提液具有神经保护作用,而且较多的研究证实其药效物质就是马鞭草中的特征性环烯醚萜苷类成分,如马鞭草苷[3-4].但是,近年来的研究也证实自然界普遍存在的黄酮类成分也具有神经保护、抗抑郁等方面的作用,而且黄酮类化合物还是苯并二氮受体、GABAA受体的良好配体[5].因此,鉴于马鞭草植物在四川省凉山地区资源的丰富性,以及为寻找、开发天然抗抑郁活性物质、阐明马鞭草的神经保护、促进睡眠、抗抑郁的药效物质基础,本课题组对马鞭草全草进行了前后两次的化学成分研究,前期研究分离得到了马鞭草苷[6],本次研究再从中分得另一特征性环烯醚萜苷主要成分——戟叶马鞭草苷,以及低极性的黄酮、蒽醌、苯丙素等类型的7 个化合物,此为马鞭草的药效物质基础研究及抗抑郁新药的开发打下了一个良好的基础.
1 仪器与材料
DRX-500 MHz 核磁共振仪(瑞士Bruker 公司);Agilent MSD-Trap-XCT 低分辨质谱仪(美国Agilent公司);Rp-C18硅胶为40 ~60 μm(Daiso 公司);MCI gel CHP 20P(日本三菱公司);Sephadex LH -20(GE公司);柱色谱用硅胶(200 ~300 目)和薄层色谱用硅胶(10 ~40 μm,青岛海洋化工有限公司);D101 大孔吸附树脂(成都科龙化工厂);溶剂均为分析纯.
马鞭草药材采集于2016 年9 月,采集地为四川省西昌市.药材经作者鉴定为马鞭草科马鞭草Verbe-na officinalis L. 植物的全草.
2 提取与分离
水煎煮,提取2 次,每次1h,纱布滤过,合并滤液,上D101 大孔吸附树脂. 吸附速度大约以每秒1 滴的流出速度进行,吸附终点以流出液显浅黄色时为止. 树脂依次用50%与95%乙醇洗脱,洗脱液减压浓缩回收溶剂,分别得50%与95%部位(Fr. 1 ~2).
Fr.1(50%乙醇部位,150 g)用硅胶拌样,上硅胶柱,用石油醚-乙酸乙酯、乙酸乙酯-甲醇系统梯度洗脱,点板合并,分成三段(A -C). 取A 段用RP -C18硅胶(甲醇-水0∶100→100∶0)洗脱,分成15 个亚流分(Fr. A.1 ~A.15).合并A.10 -A.14,用Sepha-dex LH-20 凝胶柱色谱纯化(甲醇为流动相),再分成三段,其中的第二段再用Sephadex LH -20 凝胶柱色谱纯化(甲醇为流动相),以及制备TLC(石油醚∶乙酸乙酯=3∶1),得化合物2-4;制备TLC(三氯甲烷:甲醇=10∶0.5),得化合物5-7;取B 段,用MCI 柱分离(甲醇水系统10% -40%为流动相),分成三段(B1 -B3).将B2 用Sephadex LH -20 凝胶柱色谱(甲醇为流动相)纯化,将其中一个在254 nm 下有荧光熄灭暗斑的点作为分离目标,再经硅胶柱(三氯甲烷:甲醇:乙酸=10∶0.6∶0.1%),制备TLC(三氯甲烷:甲醇:乙酸=10∶3∶0.1%)分离,得化合物1.以上化合物的结构见图1.
新鲜马鞭草全草,晒干,切碎(10 kg),用3 倍量
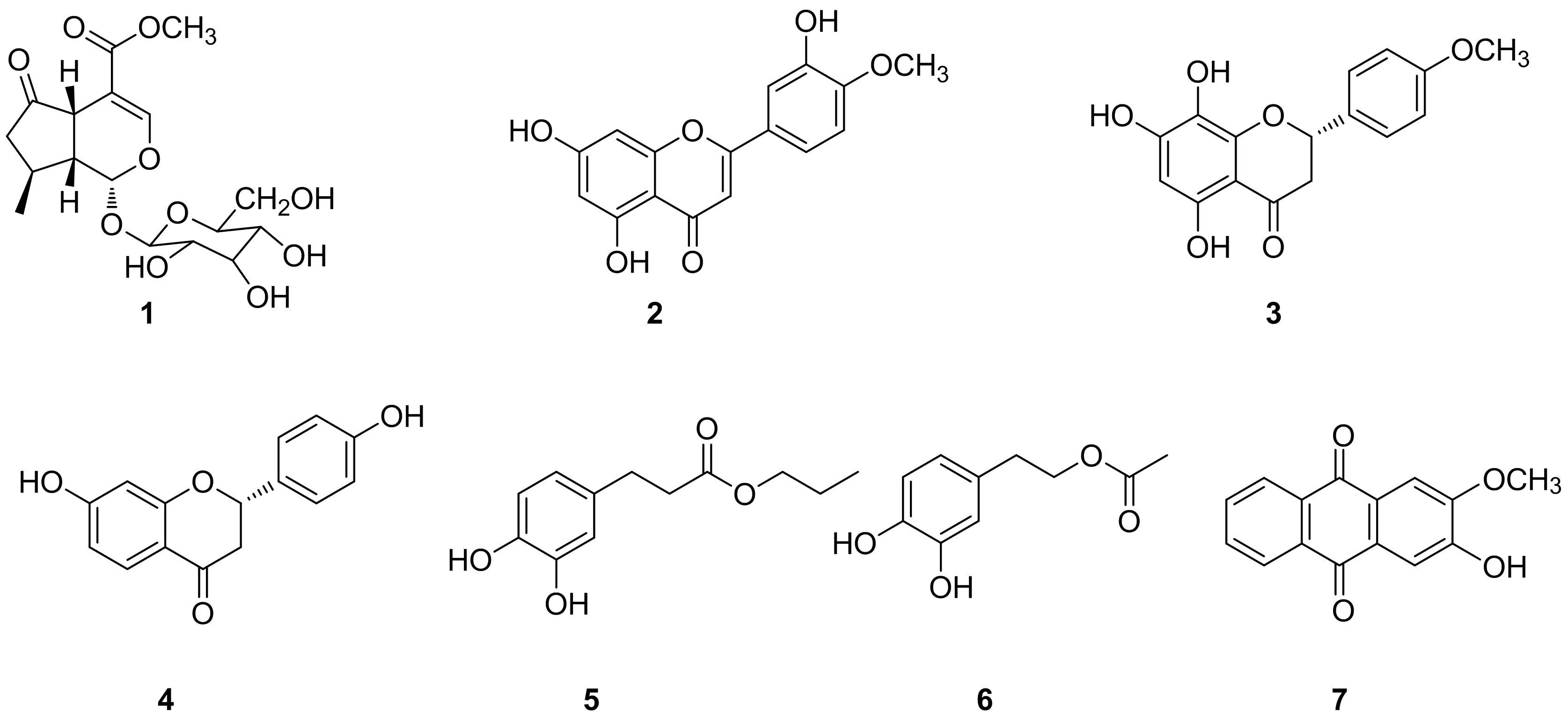
图1 化合物1-7 的化学结构Fig.1 Chemical structures of 1-7
3 结构鉴定
化合物1 无色油状.在254nm 下有荧光熄灭暗斑,硫酸乙醇显黑色,再加之极性大小,以及在本植物中的量较大,提示本化合物可能是马鞭草的特征性环烯醚萜苷类成分马鞭草苷. 进一步采用NMR 测定本化合物的1D NMR 谱,图谱显示出特征的马鞭草苷的结构信息.如在1H-NMR 谱中,在δ 3.2 -4.6 之间有多个多重峰,其中δ 4.6(J =7.9 Hz)的一个双重峰显示出分子中含有一个葡萄糖结构. 另外,在δ 3.67的一个3H 单峰,说明分子中具有一个甲氧基.以及在低场的烯氢δ7.65 单峰均提示本化合物可能是马鞭草苷.但一个重要的缩醛氢δ 5.86 (1H,d,J =1.4 Hz,H-1)的偶合常数,揭示了本化合物应是马鞭草苷的差向异构体- - 戟叶马鞭草苷. 进一步的13C NMR 及DEPT 谱也证实了我们的推断.具体的波谱数据如下:1H-NMR (CD3OD,500 MHz) δ:1.17 (3H,d,J =6.5 Hz,H -10),1.89 (1H,dd,J =8.1,18.7 Hz,H-7a),1.98(1H,m,H-8),2.16 (1H,d,J =10.4 Hz,H -9),2.72 (1H,dd,J =8.8,18.9 Hz,H -7b),3. 23 (1H,m,H -2'),3. 34(1H,m,H-4'),3.40 (1H,m,H-3'),3.67 (3H,s,OCH3-12),3.71(1H,dd,J =4.5,12.0 Hz,H-6'b),3.88 (1H,dd,J =1.7,12.0 Hz,H-6'a),4.60(1H,d,J =7.9 Hz,H -1'),5.86 (1H,d,J=1.4 Hz,H-1),7.65 (1H,s,H-3);13C -NMR(CD3OD,125 MHz) δ:211.5 (C -6),166.5 (C -11),155.7 (C-3),101.1 (C-4),99.6 (C -1'),93.6 (C-1),77.3 (C -5'),76.4 (C -3'),73.2(C-2'),72. 4 (C - 5),70. 5 (C - 4'),61. 9(C-6'),52.4 (C-9),51.8 (OCH3-12),40.7 (C-7),26.4 (C -8),19.8 (C -10). 以上数据与文献[7]对照基本一致,故鉴定化合物1 为戟叶马鞭草苷.
化合物2 黄色针晶(甲醇).1H -NMR(DMSO-d6,500 MHz)δ:13.1 (1H,s,5 -OH),10.6 (1H,s,7 -OH),10.3 (1H,s,3'-OH),7.88(1H,dd,J=8.5,2.3 Hz,H -6'),7.53(2H,m,overlapped,H-2',6'),6.91(1H,d,J =7.4 Hz,H-5'),7.53(1H,s,H-3),6.74(1H,d,J =2.0 Hz,H-8),6.57(1H,d,J =2.0 Hz,H-6),3.75(3H,s,4'-OCH3);13C-NMR(DMSO-d6,125 MHz)δ:182.5(C-4),164.2(C-7),161.6(C -2),157.6(C -5),153.2(C-9),152.8(C-4'),151.1(C -3'),131.7(C -1'),128. 8(C -6'),121. 6(C -2'),116. 4(C-5'),104.5(C-10),103.2(C-3),102.8(C -6),94.6(C-8),60.4(4'-OCH3).以上数据与文献[8]对照基本一致,故鉴定化合物2 为香叶木素.
化合物3 无色油状.1H - NMR(CD3OD,500 MHz)δ: 2.68 (1H,dd,J =2.9 and 17.1 Hz,H -3a), 3.08 (1H,dd,J =13.0 and 17.1 Hz,H -3b),3.78 (3H,s,4'-OCH3),5.25 (1H,dd,J =2.8 and 13.0 Hz,H -2),5.95 (1H,s,H -6),6.81 (2H,d,J =8. 5 Hz,H -3'and H -5'),7. 29(2H,d,J =8.5 Hz,H -2'and H -6');13C -NMR(CD3OD,125 MHz)δ:198.5(C-4),160.7(C -4'),160.2(C-7),159.0(C -5),156.5(C -9),131.0(C-1'),130.2(C -8),129.0(C -2'and C -6'),116.3(C-3'and C-5'),103.5(C -10),96.2(C -6),80.6(C-2),61.0(4'-OCH3),44.0(C-3).以上数据与文献[9]对照基本一致,鉴定化合物3 为8-羟基-柚皮素-4'-甲基醚.对于C-3 位的手性问题,可从H-2,H-3 大的偶合常数来判断,即通过δ:2.68 (1H,dd,J =2.9 和17.1 Hz,H -3a), 3.08 (1H,dd,J =13.0 和17.1 Hz,H -3b)大的偶合常数,可确定B 环处于热力学稳定的平伏键,即处于面下,其绝对构型为S -构型[10](见图1),而且现代的研究也证实所有S -构型的二氢黄酮化合物均为左旋体[10-11].
化合物4 无色油状.1H - NMR(CD3OD,500 MHz)δ: 3.06 (1H,dd,J =13.0,17.1 Hz,H -3a),2.68 (1H,dd,J =2.8,17.1 Hz,H-3b),5.26 (1H,m,H-2),5.88 (2H,m,H-6,8),6.80(2H,d,J =8.5 Hz,H -3'and H -5'),7.27 (2H,d,J =8.5 Hz,H -2'and H -6');13C - NMR (125 MHz,CD3OD) δ: 196.5 (C -4),167.0 (C -7),164.0 (C-9),163.4 (C-4'),129.7 (C-1'),129.0 (C-5),127.6 (C -2',6'),114.9 (C -3',5'),101.9 (C-10),95.7 (C-6),94.9 (C -8),42.6(C-3),79.0 (C-2).以上数据与文献[12]对照基本一致,鉴定化合物4 为甘草素.根据以上文献[10 -11],以及本化合物H - 3 大的偶合常数δ: 3. 06(1H,dd,J =13.0,17.1 Hz,H -3a),2.68 (1H,dd,J =2.8,17.1 Hz,H-3b),确定本化合物C-3的手性仍为S-构型.
化合物5 无色油状.1H - NMR(CD3OD,500 MHz)δ: 6. 68 (1H,d,J =8. 0 Hz,H -5),6. 65(1H,d,J =2.0 Hz,H-2),6.53 (1H,d,J =8.0,2.0 Hz,H-6),2.76 (2H,t,J =7.0 Hz,H -8),2.26 (2H,t,J =7.3 Hz,H-7),4.19 (2H,t,J =7.0 Hz,H-1'),1.59 (2H,m,H -2'),0.90 (3H,t,J =7.4 Hz,H -3');13C -NMR (125 MHz,CD3OD) δ:130.7 (C -1),116.3(C -2),144.9(C -3),146.2(C -4),117.0(C -5),121.2(C -6),35.5(C-7),37.0(C -8),175.4(C -9),66.4(C-1'),19.4(C-2'),13.6(C -3').以上数据与文献[13]对照,鉴定化合物5 为二氢咖啡酸丙酯.
化合物6 无色油状.1H - NMR(CD3OD,500 MHz)δ: 6. 68 (1H,d,J =8. 0 Hz,H -6'),6. 65(1H,d,J =2.1 Hz,H -2'),6.53 (1H,dd,J =2.1,8.0 Hz,H -5'),4.19 (2H,t,J =7.1 Hz,H -1),2.76 (1H,t,J =7.1 Hz,H-2),2.01 (3H,s,H-2'');13C-NMR (125 MHz,CD3OD) δ:172.9 (C-1''),146. 3 (C - 4'),144. 9 (C - 3'),130. 7(C-1'),121.2 (C-2'),116.9 (C -5'),116.4 (C-6'),66.6 (C-1),35.4 (C -2),20.8 (C -2'').以上数据与文献[14 -15]数据对照基本一致,鉴定化合物6 为2 -(3,4 -二羟基苯基) -乙醇乙酸酯.
化合物7 红色粉末.1H - NMR(CD3OD,500 MHz)δ:7.24 (1H,dd,J =1.7,7.8 Hz,H-8),7.11 (1H,td,J =1.7,7.8 Hz,H-5),6.86 (2H,m,H-6,7),6.82 (2H,s,H-1,4),3.86 (3H,s,3-OCH3);13C -NMR (125 MHz,CD3OD) δ: 155.1(C-3),148.9 (C-2),135.7 (C-8a,10a),131.5 (C-6,7),131.0 (C -9a,4a),130.1 (C -5),129.0 (C-8),117.0 (C-1),108.0 (C-4),56.8(3 -OCH3).以上数据与文献[16]对照基本一致,鉴定化合物7 为2 -羟基-3 -甲氧基蒽醌.
4 讨论与结论
从马鞭草中分离得7 个化合物,其中6 个化合物为首次从本种植物全草中分离得到,它们的化学结构类型涉及环烯醚萜苷类、二氢黄酮类、黄酮类、蒽醌类和苯丙素等,此为马鞭草的药效物质基础研究及神经保护、抗抑郁等药物的开发奠定了基础.

